リチウムイオン電池用の高性能アノードとしての窒素ドープカーボンナノチューブ上のNiCo2S4ナノ結晶
要約
近年、高エネルギー密度のリチウムイオン電池(LIB)の開発は、電気自動車やスマートグリッド技術のニーズを満たすための重要な研究の方向性の1つになっています。今日、従来のLIBは、容量、サイクル寿命、および安定性の点で限界に達しており、著しく強化された特性を備えた代替材料のさらなる改善と開発が必要になっています。バイメタル硫化物(NiCo 2 )用の窒素含有カーボンナノチューブ(N-CNT)ホスト S 4 )は、LIBの魅力的な電気化学的性能を備えたアノードとしてこの研究で提案されています。準備されたNiCo 2 S 4 / N-CNTナノコンポジットは、改善されたサイクリング安定性、速度性能、および623.0 mAh g –1 の優れた可逆容量を示しました。 0.1 A g –1 で100サイクル後 0.5 A g –1 で高容量とサイクリング安定性を維持しました 。複合材料の優れた電気化学的性能は、充電-放電プロセス中の体積膨張を軽減しながら、Liイオンの拡散性を効果的に高めることができる独自の多孔質構造に起因する可能性があります。
背景
リチウムイオン電池(LIB)は、携帯型電子機器、電気自動車、および再生可能エネルギー貯蔵で使用される主要な電池技術です[1、2]。したがって、エネルギー密度の高いLIBの開発は、経済や産業のさまざまなセクターの持続可能な開発に不可欠な研究の方向性になっています[3,4,5]。たとえば、市販のグラファイトアノード材料の比エネルギー密度は、理論容量372 mAh g –1 に達しました。 、これは、新しい電子機器や電気自動車技術の性能要件を満たすために、さらに強化する余地をあまり残していません[6、7]。その結果、現代社会のニーズを満たすために、LIB用の代替アノード材料を開発することが不可欠です。
遷移金属硫化物(TMS)は、従来の電極材料よりも著しく高い比容量を提供します[8、9、10、11、12]。最近、TMSは優れた導電性と触媒活性を備えたアノードとして報告されています。その中で、二元ニッケル-コバルト硫化物(NiCo 2 S 4 )は高い理論比容量(703 mAh g –1 )を示します )、優れた電子伝導性(1.26×10 6 S m –1 )、およびより豊富なレドックス反応部位[13、14、15、16、17]。 NiCo 2 の報告された一般的な充電/放電メカニズム S 4 リチウム(Li)を使用すると、次の反応が発生します。
$$ {\ text {NiCo}} _ {2} {\ text {S}} _ {4} + 8 {\ text {Li}} ^ {+} + 8 {\ text {e}} ^ {{- }} \ to {\ text {Ni}} + {\ text {Co}} + 4 {\ text {Li}} _ {2} {\ text {S}} $$(1)$$ {\ text { Ni}} + x {\ text {Li}} _ {2} {\ text {S}} \ leftrightarrow {\ text {NiS}} _ {x} + 2x {\ text {Li}} ^ {+} + 2x {\ text {e}} ^ {{-}} $$(2)$$ {\ text {Co}} + x {\ text {Li}} _ {2} {\ text {S}} \ leftrightarrow {\ text {CoS}} _ {x} + 2x {\ text {Li}} ^ {+} + 2x {\ text {e}} ^ {{-}} $$(3)ただし、NiCo 2 のLiストレージ容量が大きいにもかかわらず S 4 、付随する体積変化による充電/放電プロセスの低い可逆性に関連する問題がまだあり、材料の崩壊とその結果としての深刻な容量低下につながります[18]。もう1つの深刻な問題は、電解質への多硫化リチウム(LPS)の溶解によって生成される多硫化物のシャトル効果に起因し、容量保持も低くなります[19、20]。
NiCo 2 の問題を克服するため S 4 体積変化とLPS溶解に関連するアノード、ナノ構造化、炭素質添加剤の使用、炭素ベースのホストなどのさまざまなアプローチが開発され、有望な結果が得られています。ナノ構造化とその炭素/グラフェンネットワークとの組み合わせにより、電極と電解質の界面接触面積が増加し、Liイオン経路が短縮され、比容量が高くなります[18]。したがって、この研究では、NiCo 2 のその場での成長が報告されています。 S 4 水熱法を使用したカーボンナノチューブ(CNT)構造へのナノ粒子。さらに、電極材料の電気活性を高めるために、窒素(N)ヘテロ原子がCNTマトリックスに組み込まれました。このような処理により、N-CNTがより助長され、NiCo 2 が均一に成長します。 S 4 したがって、NiCo 2 の結晶化度が向上します。 S 4 / N-CNTアノード。このユニークな構造では、CNTは弾性マトリックスを形成し、構造の安定性を高め、複合材料のイオン伝導性を向上させ、NiCo 2 の体積変化を緩和します。 S 4 粒子。 NiCo 2 S 4 / N-CNT材料は、サイクリング中に良好な容量保持を維持し、電圧フェージングを大幅に抑制します。 NiCo 2 S 4 / N-CNT複合アノードは、1412.1 mAh g –1 の初期放電容量を示します。 0.1 A g –1 で 、および放電容量は623.0 mAh g –1 のままです。 100サイクル後。
メソッド
NiCoの合成 2 S 4
まず、0.074 gのCo(AC) 2 ・4H 2 Oおよび0.037gのNi(Ac) 2 ・4H 2 Oを40mLのエタノールに溶解しました。溶液を水浴上で80°Cで2時間、室温でさらに2時間撹拌しました。次に、0.078 gのチオ尿素を混合物に添加し、さらに20時間連続して攪拌してから、反応混合物を100mLオートクレーブに移しました。水熱反応は170°Cで3時間実施しました。室温まで冷却した後、生成物を脱イオン水で数回洗浄し、減圧下で凍結乾燥させた。
NiCoの合成 2 S 4 / N-CNTナノコンポジット
まず、68mgの穏やかに酸化されたCNTを40mLのエタノールに超音波分散させました。次に、0.074 gのCo(AC) 2 ・4H 2 Oおよび0.037gのNi(Ac) 2 ・4H 2 Oを加え、混合物を80℃の水浴上で2時間撹拌した。次に、2mLのNH 3 ・h 2 Oと0.078gのチオ尿素を溶液に加え、反応混合物を2時間撹拌しました。反応混合物を50mLオートクレーブに移し、170°Cで3時間熱水反応させました。生成物を室温に冷却し、脱イオン水で数回遠心分離し、凍結乾燥させた。 NiCo 2 S 4 / CNTは同じ方法で合成されましたが、NH 3 は追加されていません。 ・h 2 O。
材料の特性評価
合成されたままのサンプルの結晶構造は、粉末X線回折(XRD、D8 Discover Bruker)によって特徴づけられました。 X線光電子分光法(XPS)を実行して、K-Alpha1063アナライザーを使用してサンプルの元素組成を分析しました。サンプルの形態は、走査型電子顕微鏡(SEM、JSM-7100F、JEOL)および透過型電子顕微鏡(TEM、JEM-2100F)を使用して研究されました。サンプルの比表面積は、N 2 に基づくBrunauer–Emmett–Teller(BET)法を使用して計算されました。 V-Sorb2800Pを使用して得られた吸着-脱着等温線。熱重量分析(TGA)は、10°Cmin -1 の加熱速度で空気中で実施されました。 。
電気化学的測定
NiCo 2 の電気化学的性能 S 4 / N-CNTサンプルは、CR2032コイン型セルで評価されました。電極スラリーを調製するには、70 wt%のNiCo 2 S 4 / N-CNT複合材料、15 wt%のカーボンブラック(Super P)、および15 wt%のポリフッ化ビニリデン(PVDF)バインダーを1-メチル-2-ピロリドン(NMP)に混合しました。ドクターブレード技術を使用して、スラリーをCu箔上に均一に広げ、70°Cで8時間空気中で乾燥させました。乾燥後、円形のディスク電極を切断し、セルを高純度のArガス(99.9995%)を満たしたグローブボックス(MBraun)に組み立てました。 NiCo 2 の質量負荷 S 4 電極内の/ N-CNTは約2mg cm –2 。参照電極と対極には純Li箔を使用し、セパレーターにはミクロポーラスポリプロピレンCelgard2300を使用しました。電解質は1mol L –1 でした LiPF 6 (アラジン、CAS番号:21324-40-3)エチレンカーボネート(EC、アラジン、CAS番号:96-49-1)とジメチルカーボネート(DMC、CAS番号:616-38-6)の混合物1:1の比率。定電流充電/放電測定は、マルチチャネルバッテリーテストシステム(Neware BTS4000)を使用して、電位窓0.01〜3.00 V(vs。Li + )で実施されました。 / Li)。サイクリックボルタンメトリー(CV)および電気化学インピーダンス分光法(EIS)は、電気化学ワークステーション(Princeton、VersaState4)を使用して実行されました。
結果と考察
スキーム1は、NiCo 2 の準備ルートを示しています。 S 4 / N-CNTコンポジット。最初に、CNTの表面はNi 2+ の溶液で前処理されました。 およびCo 2+ 。次に、NiCo 2 を使用しながら、170°Cで熱水反応を介してN原子をCNTにドープしました。 S 4 CNTの表面でその場で成長させた。 NiCo 2 の結晶構造 S 4 、NiCo 2 S 4 / CNT、およびNiCo 2 S 4 / N-CNT複合材料は、XRDによって特徴づけられました(図1a)。 NiCo 2 の特徴的な回折ピーク S 4 (JCPDS 20-0728)は、3つのサンプルすべてで観察されました。さらに、NiCo 2 のピーク S 4 / N-CNTは、NiCo 2 よりも顕著でシャープでした S 4 / CNT [21]。 N-CNTは、NiCo 2 の均一で高密度の成長を促進するためのアクティブな核形成サイトとして使用できると考えられています。 S 4 [22]。図1bは、NiCo 2 のBET結果を示しています。 S 4 / N-CNTナノコンポジット。 NiCo 2 の比表面積 S 4 / N-CNTナノコンポジットは62.67m 2 g -1 。 TGA分析データ(図1c)に示されているように、NiCo 2 S 4 / N-CNTナノコンポジットは、400〜600°Cの温度範囲で重量の減少を示しました。これは、CNTの燃焼によって引き起こされました。したがって、NiCo 2 のコンテンツ S 4 NiCo 2 で S 4 / N-CNTコンポジットは〜30 wt%と決定されました。
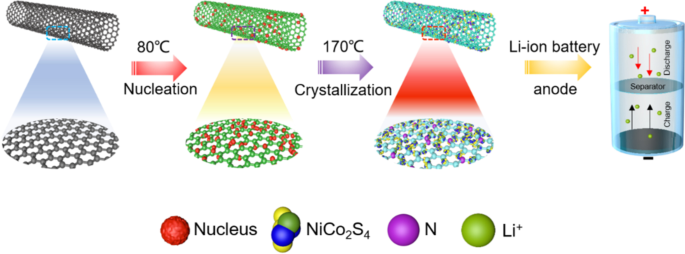
NiCo 2 の概略図 S 4 / N-CNTコンポジット
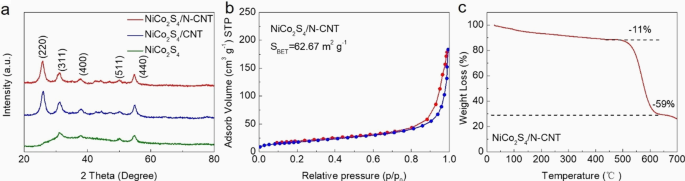
a NiCo 2 のXRDパターン S 4 、NiCo 2 S 4 / CNT、およびNiCo 2 S 4 / N-CNT; b N 2 NiCo 2 の吸着-脱着等温線 S 4 / N-CNT; c NiCo 2 のTGA S 4 / N-CNT
サンプルのSEM結果を図2a、bに示します。合成されたままのNiCo 2 S 4 ナノ粒子はより密に詰まって凝集しているように見えます。一方、CNTとN-CNTの導入により、NiCo 2 S 4 ナノ粒子は均一に分布し、堆積してNiCo 2 を形成しました S 4 / CNTコンポジット(図2c、d)およびNiCo 2 S 4 / N-CNT(図2e、f)。ただし、NiCo 2 の密度 S 4 NiCo 2 のN-CNT表面上のナノ粒子 S 4 / N-CNTはNiCo 2 よりも有意に高かった S 4 / CNTコンポジット。これは、CNTへのN原子の導入がNiCo 2 のより高密度の成長を促進することを確認します。 S 4 ナノ粒子。

a のSEM画像 、 b NiCo 2 S 4 ; c 、 d NiCo 2 S 4 / CNT;および e 、 f NiCo 2 S 4 / N-CNT
図3aのTEM画像は、NiCo 2 S 4 粒子の平均直径は〜5 nmで、N-CNTの表面に均一に分布しています。 NiCo 2 の高分解能TEM(HRTEM)画像 S 4 / N-CNTを図3bに示すと、直径約5 nmのナノ粒子は、NiCo 2 の(220)面に対応する0.35nmの明確な格子縞を示します。 S 4 。その上、多くの曲がったグラファイト格子縞がナノ粒子の周りに観察されました。図3bの高速フーリエ変換(FFT)と格子間隔プロファイルにより、NiCo 2 の組み込みがさらに確認されました。 S 4 N-CNT構造へのナノ粒子。
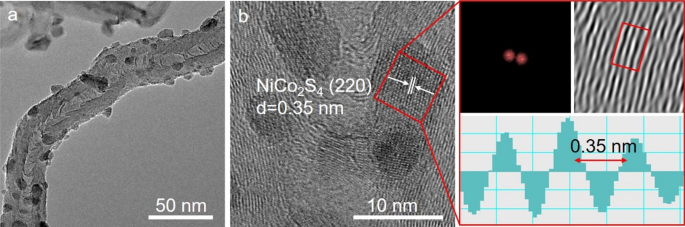
a TEM画像; b NiCo 2 のHRTEM画像 S 4 / N-CNT
さらに、XPSを使用して、NiCo 2 の結合特性と表面化学組成を決定しました。 S 4 / N-CNT。 Co 2 p スペクトル(図4a)は、Co 3+ に対応する778.8eVと793.0eVの2つのピークに分割できます。 およびCo 2+ 、それぞれ[23、24]。 N 1 s スペクトル(図4b)では、398.3、399.7、および400.9 eVのピークを、それぞれピリジニック、ピロリック、およびグラファイトのNに割り当てることができます[25、26]。 S 2 p のXPSスペクトル (図4c)、S 2 p 3/2 およびS2 p 1/2 それぞれ161.2および163.1eVで明確に観察でき、163.8 eVのピークは金属-硫黄結合に対応します[27、28]。図4dに示すように、衛星のピークに加えて、Ni 2 p の結合エネルギー 854.6および856.9eVを中心とするのは、Ni 2 p に対応します。 3/2 、および871.1および875.5eVのものはNi2 p に対応します 1/2 。これは、Ni 3+ の両方が存在することを示しています およびNi 2+ サンプル[29、30]。図4eに示すように、3つのフィッティングピークがC1sプロファイルの284.9、285.7、および290.4 eVに存在します。これは、それぞれC–C、C–N、および–C =O結合に起因する可能性があります。要約すると、NiCo 2 のXPS S 4 / N-CNTは、NiCo 2 の高度に秩序化された結晶構造の形成を示しました。 S 4 化合物の構造へのN元素の導入の成功を実証しました。
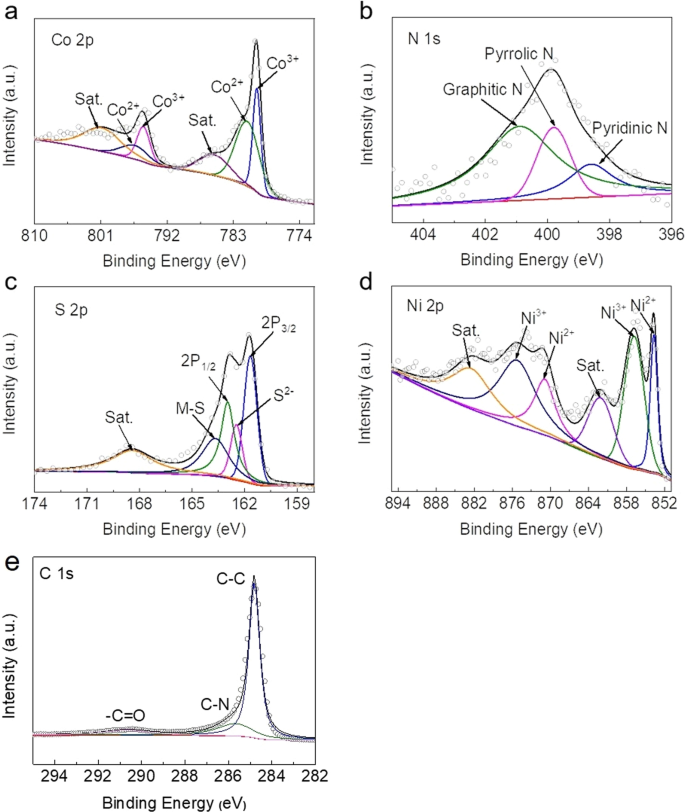
a のXPSスペクトル Co 2 p 、 b N 1 s 、 c S 2 p 、 d Ni 2 p 、および e C 1 s NiCo 2 で S 4 / N-CNT
NiCo 2 の電気化学的特性 S 4 Liストレージ用の/ N-CNTは、図5に示すように、0.01〜3.00 Vの電位範囲でCVと充電-放電サイクルによって評価されました(vs. Li + / Li)。陰極プロセスは、1.71 V、1.33 V、および0.70 Vに位置する3つの還元ピーク(図5a)で構成されていました。最も強いピークは1.33 Vに位置し、2つの弱いピークはNiCo 2 S 4 比較すると、1.71Vと0.70Vのピークは、Li 2 の形成に対応します。 それぞれSとSEIフィルム。陽極プロセスでは、1.33Vと2.05Vの酸化ピークは、金属CoのCoS x への酸化に起因する可能性があります。 。さらに、金属NiおよびCoのNiS x への酸化反応に起因する、2.32Vに強いピークがあります。 およびCoS x 、 それぞれ。曲線の形状、ピーク位置、およびピークの強度は、次のサイクルで比較的安定しており、NiCo 2 S 4 / N-CNTは優れた安定性と可逆性を備えています。
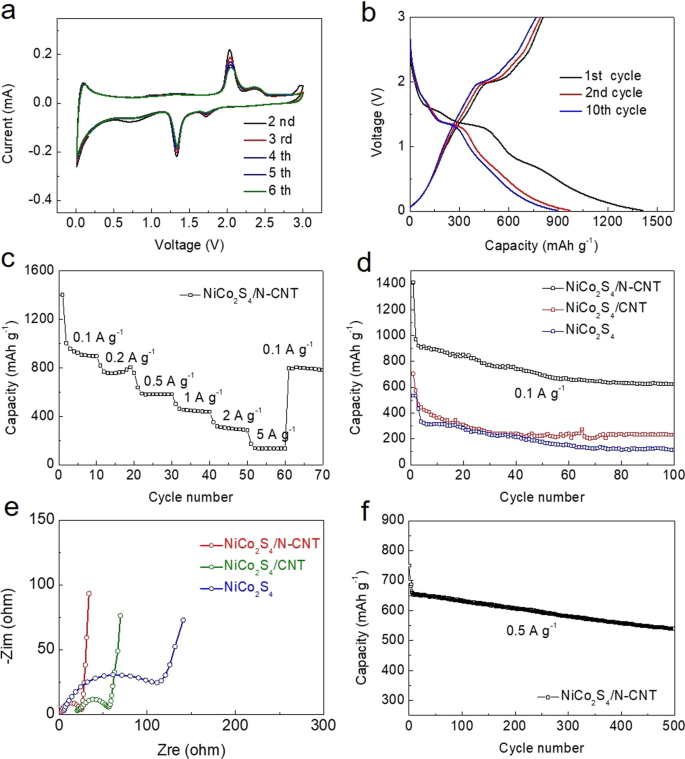
a NiCo 2 のCV S 4 / N-CNT、スキャン速度0.1 mV s -1 Li + に対して0.01〜3.0V / Li; b NiCo 2 の充電/放電曲線 S 4 / N-CNT、0.1 A g -1 ; c NiCo 2 のレート機能 S 4 さまざまな電流レートでの/ N-CNT電極。 d NiCo 2 のサイクリングパフォーマンス S 4 / N-CNT、NiCo 2 S 4 / CNT、およびNiCo 2 S 4 0.1 A g –1 で; e NiCo 2 のEISプロット S 4 / N-CNT、NiCo 2 S 4 / CNT、およびNiCo 2 S 4 ; f 0.5 A g -1 の電流密度でのサイクリング性能
図5bは、NiCo 2 の充放電曲線を示しています。 S 4 / N-CNT、0.1 A g –1 1回目、2回目、および10回目のサイクル。 NiCo 2 の最初の充電および放電容量 S 4 / N-CNT電極は807.6および1412.1mAh g –1 に達しました それぞれ、初期クーロン効率は57.2%です。 2番目と10番目のサイクルの放電容量は970.7mAh g –1 および891.1mAh g –1 、 それぞれ。充電/放電プロセスの可逆性は、クーロン効率の向上を伴うサイクル数で向上しました。得られたCVプロファイルは、NiCo 2 の充電/放電曲線に対応しています。 S 4 / N-CNT。
NiCo 2 の電気化学的性能をさらに研究するには S 4 / N-CNT、レート能力は、0.1〜5 A g –1 の電流密度で評価されました。 (図5c)。結果は、NiCo 2 の容量が S 4 / N-CNTは、電流密度の増加とともに減少しました。電流密度が0.1Aに戻ったときg -1 、NiCo 2 の容量 S 4 / N-CNTは796.1mAh g –1 の値に戻りました 、約84%の容量保持を示し、NiCo 2 S 4 / N-CNTは優れたレート性能を示します。 NiCo 2 のサイクリングパフォーマンスデータ S 4 / N-CNT、NiCo 2 S 4 / CNT、およびNiCo 2 S 4 0.1 A g –1 で100サイクル 図5dに示されています。最初の50サイクルでは、アノードの容量がわずかに低下します。次に、NiCo 2 S 4 / N-CNTアノードは、残りのサイクルでその容量を安定させ、623.0 mAh g –1 の値を示しました。 100サイクル後。これらの結果は、NiCo 2 と比較して S 4 / CNTおよびNiCo 2 S 4 電極、NiCo 2 S 4 / N-CNT電極は、著しく高い放電比容量と優れたサイクル安定性を示しました。図5eは、EISデータを示しています。ナイキスト線図の高周波半円は、電荷移動抵抗( R )に対応します。 ct )電極の。 NiCo 2 S 4 / N-CNT電極は明らかに最低の R を示します ct 値は、著しく強化された電荷/物質移動速度を示唆しています。図5fは、NiCo 2 のサイクリングパフォーマンスを示しています。 S 4 / N-CNT電極(0.5 A g -1 ) 500サイクル以上。 NiCo 2 S 4 / N-CNT電極は、750.2 mAh g -1 の初期比放電容量を提供します 539.3 mAh g -1 の可逆容量を維持します 500サイクル後、リチウム電池用のこの大容量アノードの優れたサイクリングおよびレート能力をさらに確認します。
結論
要約すると、NiCo 2 S 4 / N-CNT複合材料は、ワンポットの簡単な水熱合成ルートを使用して調製されました。 N原子をCNT構造に導入することにより、NiCo 2 が均一に分布します。 S 4 粒子サイズが減少したナノ粒子が得られた。 NiCo 2 で組み立てられたセル S 4 / N-CNTアノードは、約623.0 mAh g –1 の高い比容量を示しました。 0.1 A g –1 での優れたサイクリング安定性 100サイクル後。さらに、この電極は0.5 A g -1 で優れたサイクル特性を示しました。 500サイクル以上、高い電流密度で高性能を維持する能力を確認。私たちの研究は、この合成方法がNiCo 2 を成長させるための実行可能な方法であることを示しています S 4 LIBの高性能アノードとしてのCNT基板の表面に均一に分布しているナノ粒子。
データと資料の可用性
この調査中に生成または分析されたすべてのデータは、この公開された記事に含まれています。
略語
- LIB:
-
リチウムイオン電池
- CNT:
-
カーボンナノチューブ
- NiCo 2 S 4 :
-
二元ニッケル-コバルト硫化物
- PVDF:
-
ポリフッ化ビニリデン
- NMP:
-
N -メチル-2-ピロリドン
- XRD:
-
X線粉末回折
- SEM:
-
走査型電子顕微鏡
- CV:
-
サイクリックボルタンメトリー
- EIS:
-
電気化学インピーダンス分光法
- N-CNT:
-
窒素含有カーボンナノチューブ
- TMS:
-
遷移金属硫化物
- LPS:
-
多硫化リチウム
- XPS:
-
X線光電子分光法
- TEM:
-
透過型電子顕微鏡
- HRTEM:
-
高分解能透過型電子顕微鏡
- ベット:
-
ブルナウアー–エメット–テラー
- TGA:
-
熱重量分析
- EC:
-
エチレンカーボネート
- DMC:
-
炭酸ジメチル
- FFT:
-
高速フーリエ変換
- N:
-
窒素
- Li:
-
リチウム
ナノマテリアル
- 将来のバッテリーのためのスズナノ結晶
- リチウムイオン電池用の再生可能なPVDFグレード
- リチウムイオン電池の電気化学的性能が向上したLiNi0.8Co0.15Al0.05O2 /カーボンナノチューブの機械的複合材料
- リチウムイオン電池用の高性能アノード材料としてMWNTに固定されたSiO2 @ Cナノ粒子の容易な合成
- リチウムイオン電池用の効率的なアノード材料としての数層のMoS2 /アセチレンブラック複合材料
- PPy被覆MnO2ハイブリッドマイクロ材料の調製とリチウムイオン電池のアノードとしてのそれらの改善されたサイクル性能
- リチウムイオン電池用の金属酸化物アノードの電気化学的性能に及ぼす異なるバインダーの影響
- 水性ナトリウムイオン電池用の高電気化学的性能材料としてのNa4Mn9O18 /カーボンナノチューブ複合材料
- リチウムイオン電池のアノード材料としてのマグネシウム-熱還元によって製造された埋め込みSi /グラフェン複合材料
- 高性能リチウム硫黄電池用のポリアニリン被覆活性炭エアロゲル/硫黄複合材料
- リチウムイオン電池用の高性能フレキシブルカソードとしてシード支援水熱プロセスを介して炭化繊維上に成長した3D相互接続V6O13ナノシート



