植物化学的に合成されたグリーン(ZingiberofficinaleおよびAlliumsativum)還元された酸化ニッケルナノ粒子は殺菌および触媒の可能性を確認しました
要約
化学的毒性が低減された植物合成ナノ粒子(NP)は世界的に注目されており、最近ではナノテクノロジーの不可欠な要素となっています。繊維産業で合成殺菌剤および触媒剤を置き換えるために、緑の植物化学物質(生姜およびニンニク)を減らしたNiO-NPを準備しました。 NPは、紫外可視分光法(UV-Vis)、X線回折(XRD)、X線光電子分光法(XPS)、フーリエ変換赤外分光法(FTIR)、エネルギー分散型X線分光法(EDS)を使用して特性評価されました。 )、走査型電子分光法(SEM)、および透過型電子分光法(TEM)。 NPの合成は、350 nmで強い吸収を示すXRDおよびUV-Visによって確認されました。サイズは、ショウガの場合は16〜52 nm、ニンニクの場合は11〜59nmの範囲でした。走査型および透過型電子顕微鏡法により、立方体およびより球形のNPによる多形性が確認されました。さらに、NiO-NPを合成するために組み込まれたニンニクとショウガの抽出物の正確な量(1:3.6 ml)は、FTIRによって正常に確認されています。ニンニクによって植物化学的に還元されたNPは、多剤耐性の黄色ブドウ球菌に対して強化された殺菌活性を示しました。 濃度を上げて(0.5、1.0 mg /50μl)、メチレンブルー(MB)色素を効率的に分解しました。結論として、グリーン合成されたNiO-NPは、薬剤耐性を解決するための差し迫った活動家であり、産業規模で選択される可能性のある環境に優しい触媒剤です。
はじめに
ナノテクノロジーの物質は、少なくとも1つの寸法サイズ1〜100 nmで影響を及ぼし、サイズを制御することによって材料を設計する能力を提供します[17]。 NPは、医学を含むさまざまな分野で独自の化学的、物理的、生物学的特性を備えているため、大きな注目を集めています。それらの特性は、ナノメートルスケールでサイズを変更することで簡単に変更できます[47]。
ニッケル(Ni)および酸化ニッケル(NiO)NPは、エネルギー技術、磁性、生物医学、および電子工学における特定の磁気的、触媒的、および電子的特性のために非常に重要です[9、26、35]。 3.6〜4.0 eVのワイドバンドギャップと立方格子構造を持つNiOは、p型半導体によるポテンシャルを持っています。高い化学的安定性、超静電容量特性、電子伝達能力、および電気触媒作用を有するこれらのNPは、生物医学および光触媒、抗炎症、および抗菌活性で使用されています[8、10、11、45]。感染症、特に抗生物質耐性(MDR)の出現は、世界中の公衆衛生を破壊しました。一般に、病原性グラム陽性菌(G + ve)とグラム陰性菌(G -ve)の両方が、公衆衛生上の主要な脅威の1つです。
乳業では、牛乳腺炎は、乳汁の化学的、微生物学的、および物理的変化と乳房腺組織の病理学的変化を特徴とする大きな経済的影響を与える主要な問題のある病気です[6、19]。乳腺炎の病因には、細菌、ウイルス、真菌などの感染性病原体が含まれ、最も重要なのは細菌で、2つのグループに分けられます:主要な(連鎖球菌、黄色ブドウ球菌 、 Corynebacterium pyogenes 、および大腸菌群 )およびマイナーな病原体( Corynebacterium bovis およびコアグラーゼ陰性ブドウ球菌 )[25]。多剤耐性グラム陽性菌とグラム陰性菌の出現は、公衆衛生に重大な脅威をもたらします[23、32]。
Zingiber officinale (生姜)はアーユルヴェーダとウナニの重要な成分であり、中国の漢方薬は、ジンジベロール、モノテルペン、セスキテルペン、セスキテルペン炭化水素[12、13、43]。ただし、 Allium sativum (ニンニク)には、有機硫黄成分、すなわち、硫化アリル基、アリイン、アホエン、アリルシステイン、アリシン、およびその医学的特性を方向付けるビタミン、リン脂質、フラボノイド、アミノ酸、脂肪酸などの他の成分が含まれています[14、24]。 。 MDR( S. aureus )に対する植物化学的に還元されたNi金属酸化物NPの殺菌作用を評価することを目的としました。 )、牛乳腺炎の分離株であり、これは上記の薬剤に関する獣医研究分野でのパキスタンからの最初の報告となります。
メソッド
現在の研究は、MDR( S. aureus )に対する植物化学的に還元されたNiO-NPの殺菌作用を調査することを目的としていました。 )、牛乳腺炎の分離株。
資料
硝酸ニッケル[Ni(NO 3 ) 2 ]、水酸化ナトリウム(NaOH)、メチレンブルー(MB)、および水素化ホウ素ナトリウム(NaBH 4 )分析グレードはSigma-Aldrich®から購入し、新鮮なショウガとニンニクの根は地元の市場から収集しました。根を日陰で乾燥させて、さらなる処理のために一定の重量を達成した。抗生物質ディスクはBioanalyse®(トルコ)から購入しました。使用した細菌増殖培地は、TM Media(Titan Biotech Ltd、India)による分析グレードのものでした。
水性抽出物の調製
生姜とにんにくの根は、電動グラインダーを使って細かく砕き、プラスチック容器に保存しました。粉砕した根の粉末を、70°Cで30分間激しく攪拌しながら、制御した量の蒸留水-DIW(1:10)と混合しました。抽出物を冷却し、Whatman No.1濾紙で濾過し、さらに使用するまで4°Cで保存しました(図1)。
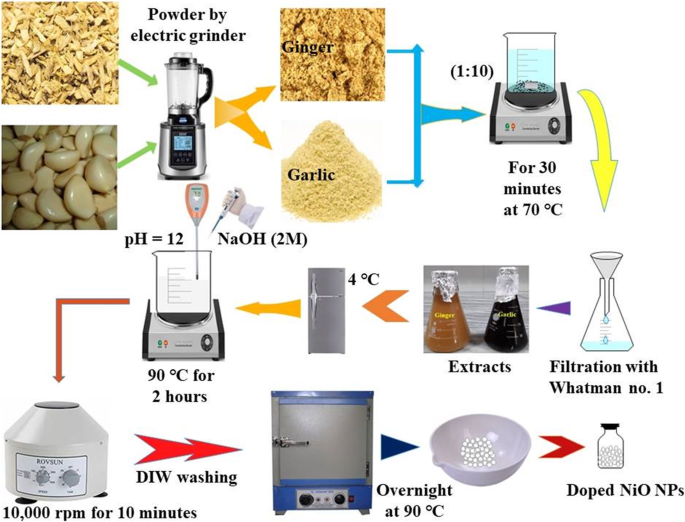
生姜とニンニクの抽出および植物化学的に還元されたNiO-NPの合成スキーム
NiO-NPのグリーン合成
さまざまな比率(1.2、1.8、2.4、3.0、3.6、および4.2 ml)のショウガとニンニクの水性抽出物を、連続的に攪拌しながら硝酸ニッケル(0.1 M)に添加しました。撹拌溶液のpH12は、NaOH(2 M)を使用して90°Cで2時間維持しました。形成された沈殿物を10,000rpmで10分間遠心分離し、DIWで洗浄し、図1に示すように90°Cの熱風オーブンで一晩乾燥させました。
特性評価
吸光度の最大値(ƛ max )合成されたNPは、UV-Visible分光光度計(Genesys 10 S)によって200〜800nmの波長でスキャンされました。相組成と構造情報は、λのCuKα1放射線を備えた2θ範囲(10–80°)のX線回折(XRD)BUNKERD2フェーザーによって分析されました。 =1.540Å。緑で合成されたNiO-NP官能基は、フーリエ変換赤外分光法(ATR-FTIR)を使用して記録されました。 NPのサイズ、形状、および元素分析は、電界放出電子顕微鏡(FESEM)および透過型電子顕微鏡Hitachi H7100FA(TEM)によって分析されました。対応するバンドギャップを持つサンプル組成は、X線光電子分光法(XPS)によって調査されました。
MDR Sの分離と識別。アウレウス
Sの分離。アウレウス
パキスタンのパンジャブにある民間および公的部門の獣医病院および農場から収集された臨床的に陽性の牛乳サンプルは、5%羊血液寒天培地で培養され、37°Cで24〜48時間培養されました。得られた特徴的なコロニーをさらにマンニット食塩寒天培地(MSA)TM Media(Titan Biotech Ltd、India)にトリプレットでストリークして、精製された Sを単離した。アウレウス 。
MDR Sの識別。アウレウス
細菌コロニーの同定は、バージーの決定的細菌学のマニュアルの説明に従って、形態学的特徴、グラム染色、および生化学的手順(コアグラーゼおよびカタラーゼテスト)を通じて行われました。
特徴的なコロニーの抗生物質感受性は、MDR Sの分離に関する臨床検査標準協会(NCCLS)のガイドラインに基づくディスク拡散試験によって評価されました。アウレウス 。オキシテトラサイクリン(30μg)、タイロシン(30μg)、ゲンタマイシン(10μg)、シプロフロキサシン(5μg)、およびトリメトプリム+スルファメトキサゾール(1.25μg+23.75μg)を含む抗生物質ディスクをミューラーに無菌的に塗布(Titan Biotech Ltd、インド)1×10 8 CFU / mlは37°Cで24時間維持されました[7]。少なくとも3つの抗生物質に耐性があることがわかった細菌はMDRと宣言されました[28]。
抗菌作用
植物化学的に還元されたNiO-NPのinvitro抗菌作用電位は、MDR Sの10の代表的な分離株に対して寒天ウェル拡散法によって評価されました。アウレウス 乳腺炎のミルクから収集。ペトリ皿を1.5×10 8 で拭きました CFU / ml(0.5マクファーランド標準)MDR S。アウレウス MSAで。滅菌コルクボーラーを使用して、直径6mmのウェルを形成しました。ショウガ、ニンニク、およびグリーン合成(植物化学的に還元された)NiO-NPの個々の水性抽出物のさまざまな濃度が適用されました。水性抽出物は、(10 mg /100μl)および(50 mg /100μl)およびNiO(0.5 mg /50μl)および(1.0 mg /50μl)の濃度で使用されました。シプロフロキサシン(0.005 mg /50μl)をポジティブコントロールとして使用し、DIWをネガティブコントロール(50μl)として使用しました。
統計分析
抗菌効果は阻害ゾーン(mm)のサイズで計算され、阻害ゾーンの直径はSPSS 20を使用した一元配置分散分析(ANOVA)によって統計的に分析されました。
触媒作用
合成された抽出物NiOの触媒評価のために、新たに調製した水素化ホウ素ナトリウム水溶液(300μl)を3 mlのメチレンブルー(0 。)と混合しました。 03×10 −3 M)ソリューション。続いて、300μlの所望の濃度のコロイドサンプルを溶液に加えました。図2に示すように、メチレンブルー色素(MB)の水色が消え、ロイコメチレンブルーへの色素分解を表しています。UV-Vis分光光度計を使用して200〜800nmの間に吸収が認められました。
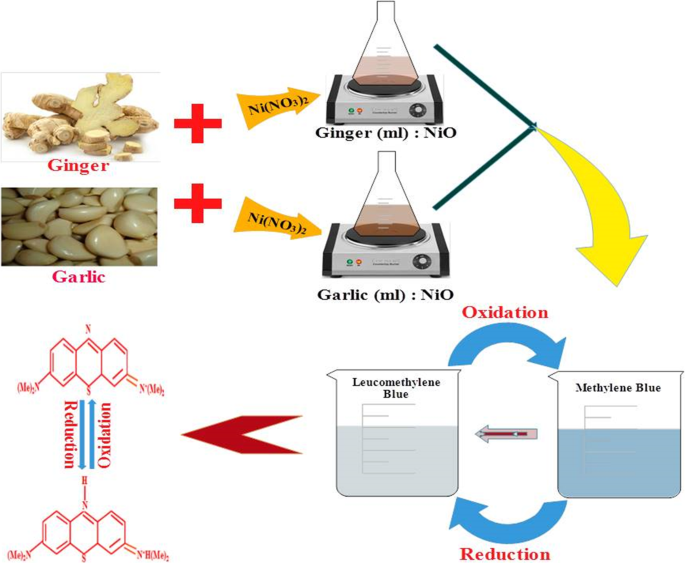
グリーン合成NPによるMBからLMBへの触媒還元の概略図
結果と考察
200〜600nmのショウガおよびニンニクの水性抽出物によって植物化学的に還元されたNiOの光学特性を図3a、bに示します。最大吸光度(λ max )NiO-NPでは、350 nm(1:3.6 ml)付近で観察され、青方偏移を伴う抽出物濃度とともに増加しました。ショウガとニンニクの抽出物の吸収ピークは、それぞれ275nmと280nm付近に現れました。根抽出物を組み込んだ後、反応混合物の急激な色の変化がワインレッドからライトグリーンに見られた。ピーク幅は、強い吸収帯によって明らかにされたように、粒子の凝集と、NiO中の抽出物濃度による価電子帯から伝導帯への電子遷移を示しました[20]。したがって、図3aでは、bの結果は、最適化された値(1:3.6 ml)を超えて抽出物の量を増減すると、合成されたNPの吸収が減少することを示しています。バンドギャップは、Taucのプロット(式1)を使用して計算されました。
$$ \ left(\ alpha hv \ right)=B {\ left(hv- {E} _g \ right)} ^ {\ raisebox {1ex} {$ 1 $} \!\ left / \!\ raisebox {-1ex } {$ 2 $} \ right。} $$(1)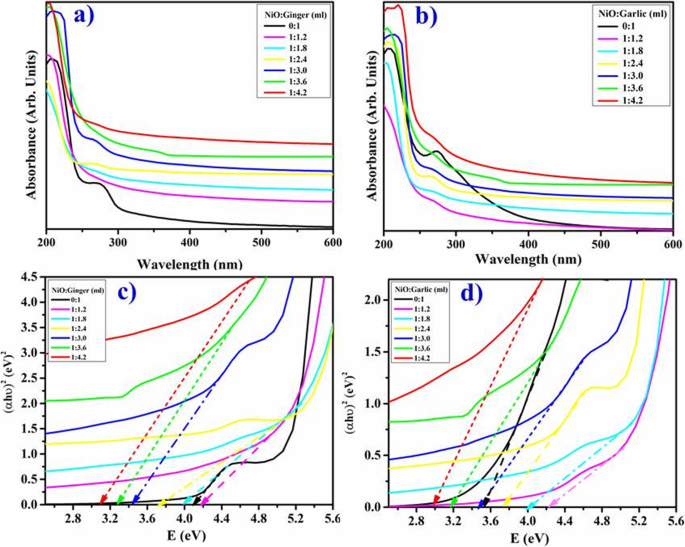
a – d 生姜を用いた緑色合成NiO-NPの吸収スペクトル( a )とニンニク抽出物( b )。生姜による植物化学的に還元されたNiOのバンドギャップ( c )とニンニク( d )それぞれ
ここでα は吸収係数、 h プランク定数 B 定数です、υ 光子周波数として知られ、 E g エネルギーバンドギャップです。 (αhʋのプロットから、生姜とニンニクによって植物化学的に還元されたNiOの推定バンドギャップ ) 1/2 光子エネルギーに対して(hʋ )。 x への接線の切片 図3c、dに示すように、サンプルのバンドギャップエネルギーを提供する軸が記録されました。バンドギャップエネルギーの変動は、NiOにショウガを4.15〜3.1 eVで、ニンニクを3.5〜3.0 eVでそれぞれドーピングしたときに測定されました(図3c、d)。
NiO-NPの結晶化度、サイズ、および相組成は、図4 a、bに示すようにXRDによって確認されました。 2θ値37.10°、43.32°、62.81°、および76.51°のピークは、(111)、(200)、(220)、および(311)に対応します(JCPDSカード番号:00-047-1049)(図4a 、b)[30]によって参照されます。ピーク強度は、 D によって計算された平均サイズ32.9nmの六角形および面心立方(fcc)NiOを示します。 =生姜の場合は0.9λ/βcosθ、ニンニクの場合は29.92nmで植物化学的に還元されたNiO-NP。広いピークは、サンプルに酸素空間と局所的な格子の乱れが存在することを示しています[38]。キャッピング剤として作用する生姜のさまざまな植物化学物質(フラボノイド、アルカロイド、タンニン、およびサポニン)およびニンニク水性抽出物(アリシン、硫化アリル、アリイン、脂肪酸、糖脂質、フェノール、アミノ酸、およびフラボノイド)は、金属酸化物NP [14、46]。
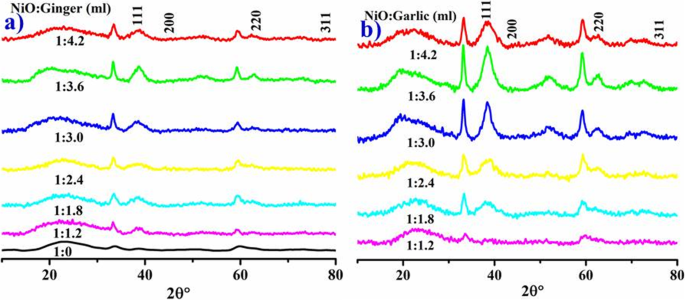
生姜によって植物化学的に還元されたNiOの異なる濃度のXRDパターン( a )とニンニク( b )および標準NiO( c )
ショウガとニンニクの根から生合成されたNiOの記録されたFTIRスペクトルを図5a、bに示します。 3380 cm -1 での精巧な幅広い吸収 OHに対応し、ピーク幅は(N-H)アミン伸縮頻度を持つカルボニル基を示します[50]。 2313 cm -1 での鋭い吸収 CO 2 の伸縮振動を示します 空中またはCO 2 NPグレインの内側。大気中のCO 2 の急速な吸収 材料の表面積が大きいことを示します[18]。 1629 cm -1 での幅広い吸収 C =C芳香族環伸縮と1392および1064cm -1 の鋭いピークに対応します C–N脂肪族アミンの伸縮振動に対応します[48]。 978 cm -1 の強いピーク NiOの確認された金属酸素伸縮周波数[44]。
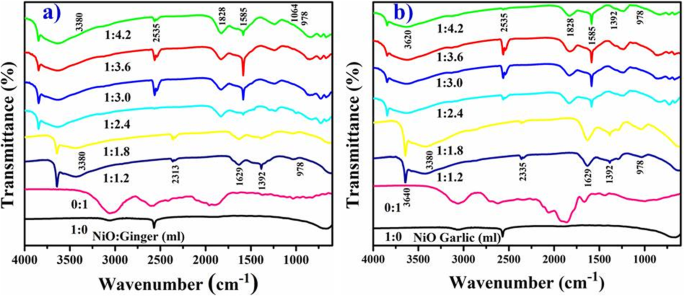
NiOに対するショウガ抽出物のFTIRスペクトル( a )とニンニク( b )
NiOの生物還元後に観察されたピークシフトは、2535–2313、1828–1629、および1585–1392 cm -1 植物化学物質、テルペノイド、フラボノイド、ポリオール、および生体還元におけるキレート化とキャッピングに関与するケトン、アルコール、カルボン酸、およびアミン官能基を持つタンパク質を示します[42]。
植物化学的に還元されたNiO-NPの表面形態とサイズは、図6a–fに示すように、電界放出走査型および透過型電子顕微鏡を使用して決定されました。 NiO-NPは、わずかな凝集を伴う立方体およびより球形(<50 nm)の多形性を示しました[40]。 NPの凝集は、ポリマーの付着と粒子間の磁気相互作用から明らかである可能性があります[49]。
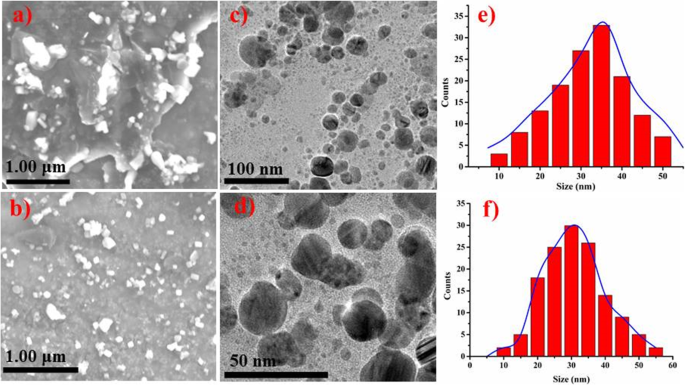
a – f 生姜による植物化学的に還元されたNiOのSEM画像( a )とニンニク( b )。生姜で植物化学的に還元されたNiOのTEM画像( c )とニンニク( d )および生姜による植物化学的に還元されたNiOのサイズ分布( e )とニンニク( f )
元素分析と合成されたNiO-NPのさらなる特徴は、図7a、bに示すように、純粋なNiO相を確認したエネルギー分散型X線分光法(EDS)によって説明されました。 EDSスペクトルにより、1〜10kVのテストサンプルに存在する高純度のNiに直接関連する3つのピークが確認されました。 Ni、O、C、およびZnのスペクトルで観察された原子質量のパーセンテージは、それぞれ54.69、27.81、18.06、および-0.55です。
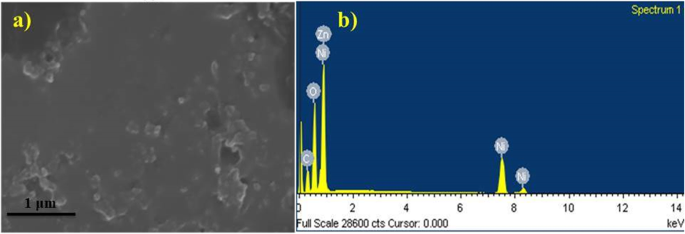
a 、 b 緑で合成されたNiO-NPのEDSスペクトル
XPSはC1 s を表示しています 、O1 s 、およびNi2 p 図8a–dの植物化学的に還元されたNiO-NPのスペクトルは、合成されたサンプルの化学的性質と結合状態を示唆しています。 284.8および286.2eVで最も強いピークは、C1 s を示しています C–CおよびC–OH / C–O–Cに対応するスペクトル(図8b)[21]。 O1 s 530.8 eVのピーク(図8c)は、酸素原子のヒドロキシル基、ニッケル空孔に隣接する酸素原子、または酸素結合炭素原子C =Oに割り当てることができます[1、15、37]。 532.2 eVにある寄与は、吸収された水分子(NiOH)の酸素原子に起因します[31、41]。 Ni2 p Ni2 p を含むスペクトル 3/2およびNi2 p 1/2ピークは、ガウス-ローレンツ関数を使用して5つの成分に分離できます(図8d)。 872.72および855.82eVで最も強いピークは、Ni2 p に属します。 1/2およびNi2 p 3/2で、対応する衛星ピークはそれぞれ879.36と861.57eVです[16]。 Ni間のスピン軌道相互作用(2 p 1/2)およびNi(2 p 3/2)およびNiO-NPコアレベルは17.28 eVであり、以前のレポート[33、34]とよく一致しています。
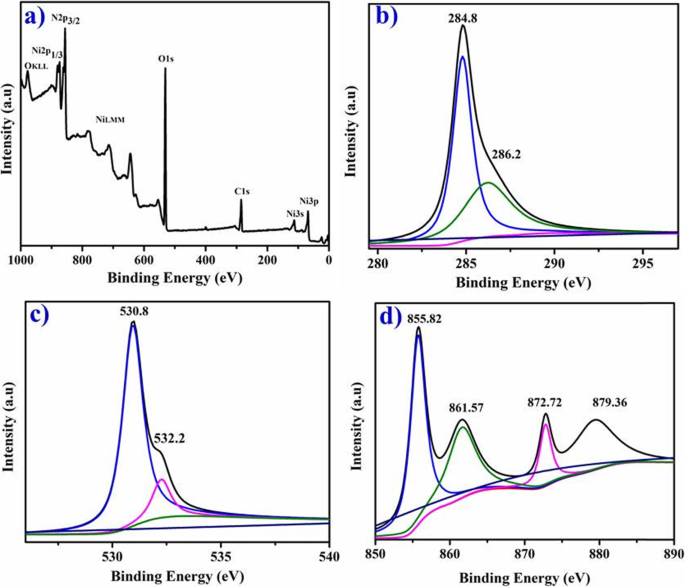
a – d 植物化学的に還元された粒子のXPS調査( a )、C1 s 軌道( b )、O1 s NiOのスペクトル( c )、およびNi2 p ( d )
図9a〜dおよび表1に示すように、ショウガおよびニンニクの根の抽出物と緑色/植物化学的に還元されたNiO-NPの抗菌/殺菌作用を、阻害ゾーン測定(mm)による寒天ウェル拡散アッセイを使用して評価しました。 NP濃度と阻害ゾーン(mm)の間。重要な抑制ゾーン(mm)( P <0.05)は、サンプル1(1.2 ml:1)、2(1.8 ml:1)、3(2.4 ml:1)、4(3 ml:1)、5(3.6 ml:1)、および6( 4.2 ml:1)低濃度および高濃度で(3–4.9 mm)および(3.05–5.2 mm)の範囲で生姜によって植物化学的にNiO-NPを減少させ(図9c、d)、(3.15–5.3 mm)および(3.75– 5.9 mm)MDR Sに対してニンニクで植物化学的に還元されたNP。アウレウス (図9e、f)。 ショウガの根の水性抽出物はゼロの効力を示し(図9a)、ニンニクの根は低濃度と高濃度でそれぞれ2.65mmと5mmの阻害ゾーンを示しました(図9b)。すべての結果を、ネガティブコントロールのDIW(0 mm)およびポジティブコントロールのシプロフロキサシン(12.55 mm)と比較しました。全体として、ニンニクで植物化学的に還元されたNiO-NPは有意な( P <0.05)MDR Sに対する強化された殺菌作用。アウレウス。
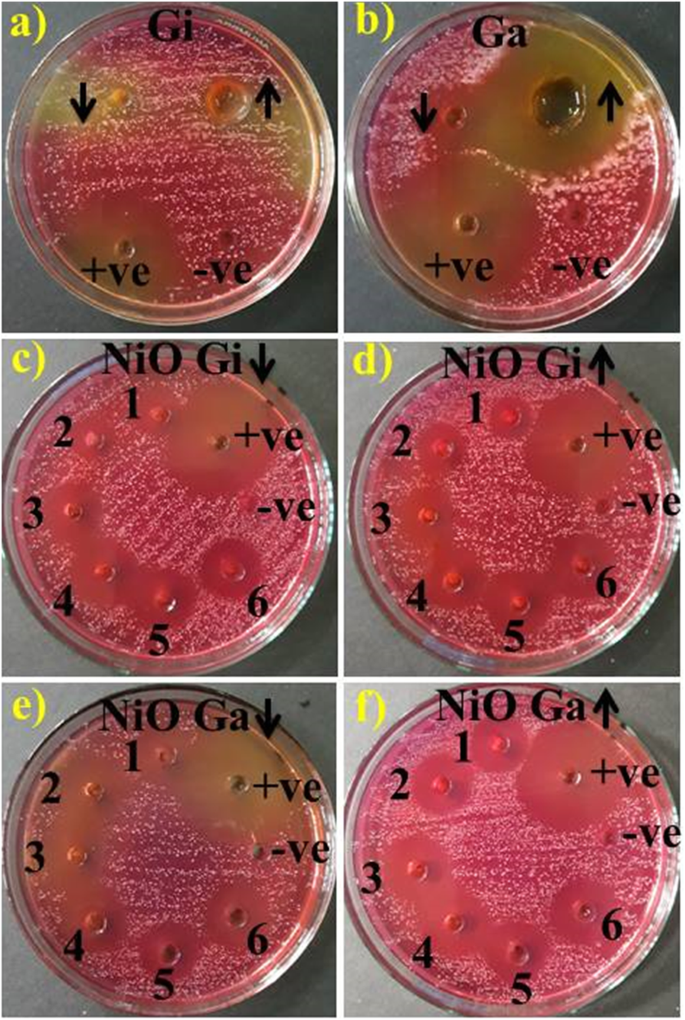
a – f ショウガ水性抽出物のinvitro抗菌活性( a )、にんにく( b )、および低用量および高用量でショウガ抽出物によって植物化学的に合成されたNiO-NP( c 、 d )とにんにく( e 、 f )
酸化ストレス耐性の違いは、抗菌作用電位に推測的な役割を果たす合成ナノ材料の表面積、形態、粒子サイズなどのさまざまな要因に依存します[29、36]。細菌株とナノスケールの材料との間の静電相互作用により、細菌の細胞死の原因となる活性酸素種が生成されます[2、3、4、5、22]。陽イオンNi 2+ の強い相互作用を含む、細菌株とのナノマテリアル反応の可能性があることがわかった2つの反応 バクテリア細胞の負に帯電した部分が崩壊し、2番目の反応がNiO表面に光を照射すると価電子帯から伝導帯への電子励起を引き起こします。 O 2 とのさらなる電子反応 O − を生成します 2 H 2 をもたらすラジカル O 2 製造。・OHの生成はh + の反応で発生しました 水で。したがって、結果として得られるO - 2 ・および・OH種は、細菌細胞の外表面に存在する脂質またはタンパク質分子の分解に重要な役割を果たしました[39]。
触媒作用
図10a〜eは、室温で根抽出物と緑色/植物化学的に還元されたNiO-NPの存在下でのMB触媒還元を示しています。図10aは、従来のルートで合成されたNiO-NPの触媒ポテンシャルを示し、(図10b、c)は、ショウガとニンニクの根の水性抽出物の触媒ポテンシャルを示しています。植物化学的に還元されたNiO-NPの触媒能力を図10dに示します。 NiOと植物の根の抽出物は、メチレンブルーの還元に15、21、38分を消費していたため、効率的なナノ触媒ではないことは明らかです(図10a–c)。生姜で植物化学的に還元されたNPは急速な分解を示しました(λ max =8 min)MBからロイコメチレンブルーへの効率的な変換(図10d)。ニンニクを介したNiO-NPは、5分で100%の色素還元の同様のパターンを示しました(図10e)。
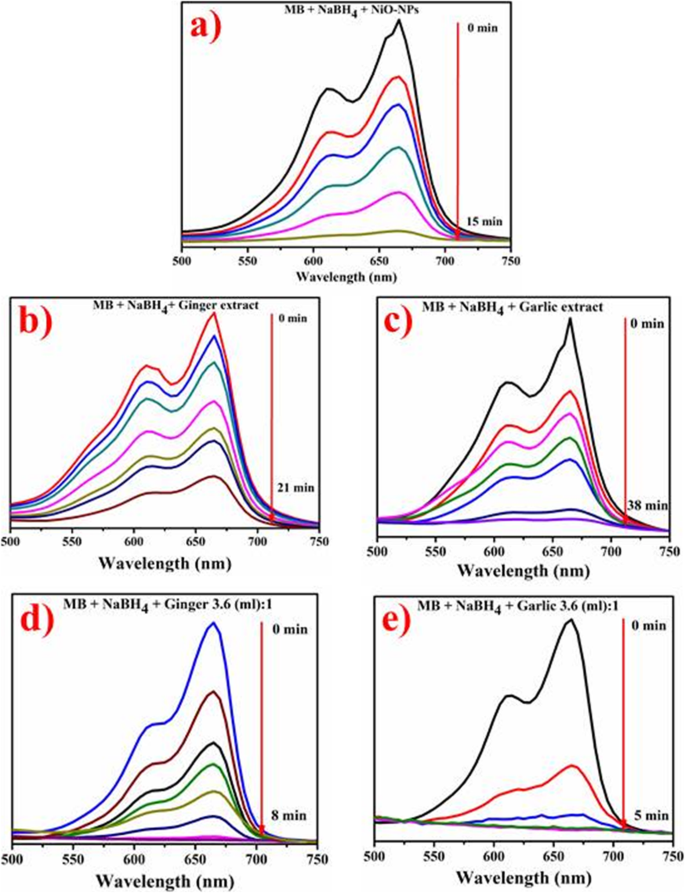
a – e NiOの触媒活性( a )、生姜エキス( b )、ニンニク抽出物( c )、生姜によって植物化学的に還元されたNiO( d )、ニンニクはNPを減らしました( e )
グリーン/植物化学的に還元されたNPは、ドナー種(BH 4 )から電子を移動させることにより、触媒作用による色素の大幅な分解を行います。 )アクセプター(MB)に接続し、活性化エネルギーを減らしてシステムを安定させます[27]。データは、従来のNPおよび個々の抽出物と比較して効率的なナノ触媒として緑色のNPを明らかにしました。
結論
ショウガとニンニクの根の抽出物を含むNiO-NPは、優れた殺菌剤および触媒剤として機能しました。植物化学基を有する根抽出物の取り込みは、FTIRによって明らかにされた成功したNiO-NP合成をもたらした。 XRDピークは、NiOの六方晶および面心立方(fcc)格子を確認し、SEMは、平均サイズ16〜52(生姜ドーピング)および11〜59 nm(ニンニクドーピング)のNPの立方晶およびより球形の形態を伴う多形性を確認しました。ただし、元素分析では、EDSとXPSによって分析された化学的性質と結合状態が明らかになり、ニッケルと酸素の実際の割合が示されました。一方、UV分析では、350 nmの範囲での吸収ピークの違いが確認され、より多くのドーパントでブルーシフトが導入されました。高濃度の植物化学的にニンニクで還元されたNiOは、MDR Sに対するショウガで還元されたNPと比較してより強力であることがわかりました。アウレウス MBを効率的に削減します。したがって、ニンニクの根の抽出物からの緑色/植物化学的に還元されたNiOは、抗生物質耐性の代わりとして先進医療で、そして環境に害のない触媒剤として繊維産業で採用される可能性があります。
データと資料の可用性
すべてのデータは制限なしで完全に利用可能です。
略語
- EDS:
-
エネルギー分散型X線分光法
- fcc:
-
面心立方
- FTIR:
-
フーリエ変換赤外分光法
- G + ve:
-
グラム陽性
- G –ve:
-
グラム陰性菌
- JCPDS:
-
粉末回折標準に関する合同委員会
- MB:
-
メチレンブルー
- Ni:
-
ニッケル
- NiO:
-
酸化ニッケル
- nm:
-
ナノメートル
- NP:
-
ナノ粒子
- SEM:
-
走査型電子顕微鏡
- TEM:
-
透過型電子顕微鏡
- UV-Vis:
-
紫外可視分光法
- XPS:
-
X線光電子分光法
- XRD:
-
X線回折
ナノマテリアル
- 生体適合性FePO4ナノ粒子:ドラッグデリバリー、RNA安定化、および機能的活性
- Escherichia coliに対する酸化銅ナノ粒子の生体合成、特性評価、および抗菌力の評価
- Sb /パリゴルスキー石(PAL)ナノ粒子の調製と強化された接触水素化活性
- 従来の抗生物質の殺菌効果を活性化するための排出ポンプおよびバイオフィルム阻害剤としてのナノ粒子
- Agで装飾されたSnO2ミクロスフェアのワンポットグリーン合成:4-ニトロフェノールの還元のための効率的で再利用可能な触媒
- マウスにおける二酸化チタンナノ粒子の潜在的な肝臓、脳、および胚の毒性
- 炭化水素中の金ナノ粒子のサイズ制御と安定化のための分散剤としての修飾ハイパーブランチポリグリセロール
- 表面分光分析を使用した遷移金属をドープしたTiO2ナノ粒子の触媒活性の決定
- 光熱治療および光音響イメージングのためのポリピロール被覆鉄-白金ナノ粒子の合成およびinvitro性能
- 銅ナノ粒子の合成と安定化におけるグリーン熟達度:触媒、抗菌、細胞毒性、および抗酸化活性
- ラットにおける腹腔内および静脈内投与経路による生合成された銅および酸化亜鉛ナノ粒子の比較invivo精査



