導電性アモルファスLLTO薄膜による電極の表面改質による4.5VでのLiCoO2の改善されたサイクル安定性
要約
LiCoO 2 の安定性の問題 高電圧でのサイクルは、高エネルギー密度と長いサイクル寿命を備えたリチウムイオン電池の開発にとって非常に重要な問題の1つです。 LiCoO 2 のサイクリング性能を改善することは効果的ですが 個々のLiCoO 2 のコーティングを介して 別の金属酸化物またはフッ化物を含む粒子の場合、一般的なコーティング材料は導体が貧弱であるため、一般にレート容量が低下します。ここで、アモルファスLi 0.33 La 0.56 TiO 3 最も成功した固体電解質の1つである、は、構成されたLiCoO 2 の表面に直接堆積されました。 マグネトロンスパッタリングによる電極。構成されたLiCoO 2 に固有の導電性ネットワークだけでなく 電極は保持されましたが、Li + バルクおよびカソード-電解質界面を横切る輸送が強化された。さらに、サイクルされたLiCoO 2 の表面化学分析 電極は、安定性の問題のほとんどがアモルファスLi 0.33 の堆積によって対処できることを示唆しています。 La 0.56 TiO 3 。最適化された堆積時間で、LiCoO 2 Li 0.33 によって修飾された電極 La 0.56 TiO 3 カットオフ電圧が2.75〜4.5 V vs で0.2Cで150mAh / gの安定した可逆容量を実行しました。 Li + / Liと、元の状態のものと比較して5 Cで84.6%の容量増加。
はじめに
リチウムイオン電池(LIB)は、携帯型電子機器、電気自動車、および定置型電源でのエネルギー貯蔵需要の増加に伴い、高エネルギー密度、高レート機能、および長いサイクル寿命が求められています[1,2,3]。 LIBのエネルギー密度を高める最も直接的な方法は、より高い容量および/またはより高い動作電圧を備えたカソード材料を適用することです[4、5、6、7、8]。 LiCoO 2 を含むLIB (LCO)カソードは、過去30年間、特に携帯用電子機器の電源として大きな商業的成功を収めており、その高い比容量、高い酸化還元電位、および長いサイクル寿命の恩恵を受けています[9、10、11、12]。ただし、LCOの一般的に使用される比容量は140 mAh / gにしか達することができず、理論容量の272 mAh / gの約半分であり、上限カットオフ電圧は4.2V対Li + / Li [11,12,13]。理論的には、カットオフ電圧を上げることにより、利用される比容量を改善することができます。ただし、カットオフ電圧が4.2V対Li + を超えると、LCOのサイクル安定性が低下します。 / Li [1]。さらに、4.5V未満のLCOの容量減衰対Li + / Liは主に、Cacoethic副反応、Co溶解、およびLiPF 6 間の液固界面でのHF腐食によるものです。 ベースの有機電解質とLCOカソード[14、15]。したがって、4.5V対Li + で安定したカソード-電解質界面を実現するために多大な努力が払われてきました。 / LiはLCOの表面改質を介して[16,17,18]。
構造的特徴の観点から、表面改質は2つのタイプに分けることができます。あるタイプでは、電極をキャストする前に、修飾層を個々のLCO粒子にコーティングします[16、17、18]。他のタイプでは、修飾層は、構成されたLCO電極の表面に堆積されます[19、20]。個々のLCO粒子の表面修飾は、そのサイクル安定性を改善するのに効果的であり[16、17、18]、低コストの湿式化学経路を介して簡単に実現できます[21、22、23、24]が、いくつかの欠点があります。そのアプリケーションを制限します。たとえば、粒子の修飾層は、スラリーの混合および電極のカレンダリング中の深刻な機械的衝撃により破損する可能性があります[13]。さらに、個々の粒子の修飾層は、電極の大部分でイオン伝導率と電子伝導率のバランスを崩す可能性があります[1]。あるいは、LCO造粒、スラリー混合、および電極カレンダーの後に実行され、電極の表面に修飾材料の薄層のみを導入する、構成されたLCO電極の表面修飾は、上記の問題に対処する可能性があります[ 13、19、20、25]。
材料化学の観点から、表面修飾はフッ化物(AlF 3 )を含む不活性化合物によって実現できます。 、CeF 3 、LaF 3 など)[21、22]および酸化物(Al 2 O 3 、MgO、ZrO 2 、ZnOなど)[23,24,25,26]、これらは一般的に貧弱なLi + およびe − Li + の導体またはイオン導体 (LiAiO 2 、Li 4 Ti 5 O 12 、Li 3 PO 4 、Li 2 CO 3 、など)[13、19、20、27]。不活性化合物による表面修飾は、高電圧でLCO-電解質界面を安定させるのに役立ちますが[27]、電荷の輸送と移動は低導電性コーティング層によって制限されるため、LCOカソードのレート能力を損なう可能性があります[27]。 19、27]。一方、Li + による表面修飾 導体はカソードのバルク導電性ネットワークを大幅に減衰させることはありませんが、界面の安定性を向上させることができます[20、25]。特に、Li + -導電性界面層はLi + を助けます LiPF 6 間の移行 ベースの電解質とLCOカソードにより、望ましい小さな界面インピーダンスが得られます[28]。
ここで、アモルファスLi 0.35 La 0.56 TiO 3 最も成功した固体電解質の1つである(α-LLTO)[29、30]は、マグネトロンスパッタリングによって構成されたLCO電極の表面に直接堆積されました(図1a)。スパッタ蒸着されたα-LLTOは、高温熱処理を必要とせず、高いイオン伝導性(1.54×10 -5 )を実行します。 室温でS / cm)。 α-LLTOによる電極レベルの表面修飾は、LCOカソードのバルク伝導を損なうだけでなく、レート容量に有利なLCO-電解質界面での電荷移動速度を向上させることも刺激的です。さらに、堆積したα-LLTOは、LCO-電解質界面でのCo溶解、HF腐食、およびその他の副反応を効果的に防止します。 LCO-LLTO-電解質構成は、比較的安定した界面分極をもたらします。その結果、提示されたα-LLTOによる電極の表面改質により、LCOは、4.5 V vs の上限カットオフ電圧で100サイクル以上安定して動作することができます。 Li + / Liおよび0.2Cで150mAh / gの可逆容量。
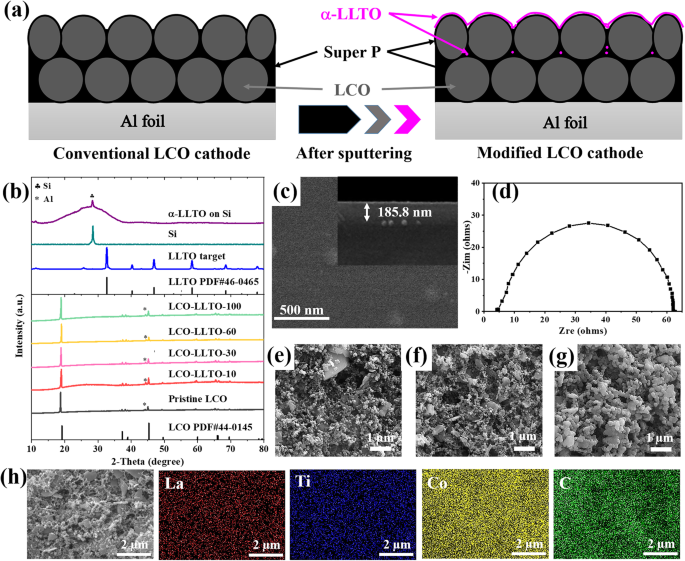
a 従来のLCO電極とα-LLTO修飾層を備えたLCO電極の概略図。 b LLTOターゲット(青線)、Si基板(濃いシアン線)、Si基板上のα-LLTO薄膜(紫線)、元のLCOカソード(黒線)、およびα-LLTO修飾LCO電極のXRDパターンLLTOの異なる堆積時間(赤の線は10分、ピンクの線は30分、黄色の線は60分、緑の線は100分)。 c Si基板上のLLTO薄膜の上面および側面のSEM画像。 d Si基板上のLLTO膜のEIS硬化; e – g e の上面SEM画像 手付かずのLCO、 f LCO-LLTO-10、および g LCO-LLTO-100; h LCO-LLTO-10の表面のEDSマッピング
材料と方法
α-LLTOによるLCOカソードの準備と表面改質
LCO電極は、よく混合された市販のLCO粉末(アラジン、〜2μm、99%、80 wt%)、アセチレンブラック(MTI KJグループ、10 wt%)、およびPVDF(アルケマ、10 wt%)をAl箔の表面。 N-メチルピロリドンを溶媒として使用してスラリーを形成した。鋳造したままのLCO電極を動的真空中で110°Cで一晩乾燥させ、カレンダリング後に溶媒と微量の水を除去しました。鋳造されたLCOカソードの統計的厚さは約40μmであり、これはスクリューマイクロメータによって決定されます。 LiCoO 2 の負荷密度 活物質は4.96mg / cm 2 (0.97 mAh / cm 2 4.5〜2.75V対Li / Li + の最初の放電 )。 α-LLTOは、マグネトロンスパッタリングによってSi基板またはLCO電極の表面に堆積されました。空洞は5×10 -4 に排気されました Pa以下。 LCO電極は、閉じ込められた水分と空気を除去するために、真空中で120°Cで30分間予熱されました。 Li 0.33 La 0.56 TiO 3 ターゲットを5分間事前にスパッタリングして、表面のほこりや異物を取り除きました。ターゲットと基板の間の距離は15cmでした。スパッタリングパワーは120Wでした。使用圧力は1Paでした。アルゴンと酸素の比率は70:30(sccm)でした。基板温度は120℃に保った。異なる厚さの改質層を得るために、スパッタリング時間を10、30、60、および100分に設定した。 α-LLTOの堆積時間が異なるサンプルは、それぞれLCO-LLTO-10、LCO-LLTO-30、LCO-LLTO-60、およびLCO-LLTO-100と表記されました。 α-LLTOの堆積後、得られたサンプルを真空下で24時間乾燥させて、使用前に閉じ込められた水分を除去しました。 α-LLTOのイオン伝導度を測定するために、平らなSi基板上に堆積させました。堆積プロセスのパラメータは、堆積時間が240分であったことを除いて、LCO電極の表面改質と同様でした。
材料の特性評価
Si基板上のLLTO膜の厚さは、断面走査型電子顕微鏡(SEM)を使用して決定されました。位相分析は、CuKα放射線を使用したX線回折(XRD)によって実行されました。 LCO電極の表面形態をSEMで観察した。 Co、C、La、およびTiの元素分布は、エネルギー分散型分光計(EDS)によって分析されました。 X線光電子分光法(XPS、Thermo Fisher Escalab Xi +)を使用して、電極の表面化学組成を分析しました。
電気化学的測定
LCO電極を直径12mmの円形に打ち抜き、動的真空中で80°Cで一晩乾燥させて、空気から吸収された微量の水を除去しました。セパレーター(ポリプロピレン、Celgard 2400)を50℃で一晩真空乾燥しました。サンプルの電気化学的特性は、リチウム金属アノードを備えた2032コイン電池でテストされました。液体電解質は1M LiPF 6 でした。 EC:DMC:EMC(v / v / v =1:1:1)溶媒を混合した溶液。すべてのセルは、Arを充填したグローブボックスで製造されました。サイクリングテストは、2.75〜4.5V対Li + で実行されました。 バッテリーテスト装置(NEWARE CT-3008)による室温でのさまざまな充放電率の/ Li。サイクリックボルタンメトリー(CV)および電気化学インピーダンス分光法(EIS)は、Princeton VersaSTAT3F電気化学アナライザーによって実行されました。 EIS測定の場合、振幅電圧は10 mV、周波数範囲は0.1 Hz〜100kHzでした。
結果と考察
エネルギー密度とレート能力は、カソード技術の2つのコア要件です。それは、LCOカソードの表面改質の課題を提起します。 Li + の電極内の導電性ネットワーク およびe − LCO-電解質界面は、不活性物質の導入をできるだけ少なくすることで安定化されますが、維持する必要があります。図1aに示すように、マグネトロンスパッタリングにより、作製したLCO電極をα-LLTOでコーティングすることを提案します。スパッタ堆積したα-LLTOは、LCO電極の表面に、コンフォーマルで密度が高く、非常に薄い表土を形成します。以下のメリットが期待できます。第一に、電極の準備プロセス中の修飾層への潜在的な損傷が回避されます。第二に、修飾電極中のα-LLTOの質量分率は非常に小さい。第三に、LCOと電解質の間の望ましくない相互作用を効果的に抑制することができます。最後に、そして最も重要なことに、堆積したα-LLTOはLi + の輸送経路を損なうことはありません およびe − 主に電極の上面近くに存在するため、電極内にあります。
Li 0.35 に由来するX線回折ピーク La 0.56 TiO 3 ここで使用されているターゲットは、結晶性LLTO(PDF#46-0465)とよく似ています(図1bの青い線)。しかし、結晶性LLTOに属する回折ピークは、Si基板上のLLTO薄膜のXRDパターンでは観察できません(図1bの紫色の線)。 28.48°の回折ピークはSi基板に起因するはずです。堆積したままのLLTO薄膜はアモルファスであると結論付けるのが妥当です。図1cに示すように、堆積したままのLLTO薄膜は均質で緻密であり、結晶粒がなく、アモルファスであることをさらに確認できます。 α-LLTO薄膜のイオン伝導度は、Z re の切片によって決定されるバルク抵抗に基づいて計算されます。 EIS曲線の軸(図1d)とその厚さは側面SEM画像(図1cに挿入)で決定されます。堆積したままのα-LLTO薄膜は、1.54×10 -5 のイオン伝導度を発揮します。 室温でのS / cm。これは、α-LLTO薄膜固体電解質の報告値に匹敵します[31、32]。さらに、以前の文献は、α-LLTO薄膜固体電解質が優れた化学的および電気化学的安定性を備えていることを示しています[30]。したがって、LCO電極の表面にα-LLTOを堆積させることにより、安定性と導電性の高いLCO-電解質界面を構築できる可能性があります。
LCO電極へのα-LLTOのコンフォーマルコーティングは、スパッタリング蒸着によって実現できます。図1eに見られるように、元のLCO電極は多孔質の微細構造を持っています。 α-LLTOを10分間堆積させることによる表面改質は、電極の表面形態を大きく変化させません(図1f)。堆積時間を100分に延長すると、α-LLTO粒子の蓄積と凝集による表土が観察されます(図1g)。しかし、EDSマッピング画像(図1h)で観察されたLaとTiの分布は、LCO電極が10分間の堆積後にα-LLTOによって均一かつコンフォーマルに覆われていることを示唆しています。 CoとCは、表面組成分析によっても検出されます。これは、堆積したα-LLTOの厚さがEDSのプロービング深度(〜1μm)よりもはるかに薄いことを示しています。 α-LLTO修飾がある場合とない場合のLCO電極のXRDパターンは類似しており、LLTOの堆積時間が100分(緑、黄、図1b)のピンク、赤、黒の線。これは、堆積したままのLLTOがアモルファスの形であるという事実と一致しています。
多孔質LiCoO 2 の表面のため、多孔質LCO電極上のLLTO層の厚さを直接決定することは困難です。 電極が粗い。ただし、同じ処理パラメータを使用して平坦な基板上に堆積されたLLTO薄膜の厚さは、有用な基準となるはずです。したがって、シリコンウェーハ上にLLTO薄膜を堆積し、プロフィロメータを使用して厚さを決定しました。 10 min、30 min、60 min、100 minのスパッタリングで堆積したLLTO薄膜の厚さは、それぞれ11 nm、24 nm、52 nm、80 nmです(図S1)。
LCOのサイクル安定性とレート容量は、構成された電極にα-LLTOを堆積させることで効果的に改善できます(図2)。 α-LLTOコーティングの有無にかかわらず、LCO電極は、2.75〜4.5 V vs の範囲のカットオフ電圧でサイクルされました。 Li + さまざまなサイクリングレートでの/ Li。高電圧での初期充電/放電サイクルでは、容量の減衰は不可逆的な相転移とLCOの結晶構造の破壊によって支配されます[33、34、35、36、37]。一方、LiCoO 2 のサイクリング性能に対する望ましくない副反応の悪影響 界面反応の反応速度が遅いため、後の充電/放電サイクルでますます顕著になります。 LLTO表面改質は、主にLiCoO 2 での望ましくない副反応に対処します。 -電解質界面。したがって、すべてのサンプルは、0.2 Cで同様の初期放電容量(〜195 mAh / g)を示します。また、図2aに示すように、最初の20サイクルでの容量保持は閉じています。連続サイクルでは、堆積したα-LLTOのプラスの効果が徐々に現れます。 100サイクル後、元のLCOの放電容量は108 mAh / gに低下します。容量保持率は、初期放電容量と比較してわずか55.4%です。一方、LCO-LLTO-10は、100サイクル後に150 mAh / gという高い安定した放電容量を示し、76.9%の容量保持率に相当します。ただし、多孔質電極の表面の表土が厚くなると、界面インピーダンスが増加します(図S2)。 100サイクル後のLCO-LLTO-30、LCO-LLTO-60、およびLCO-LLTO-100の放電容量は、元のLCOとLCO-LLTO-10の間にあり、122、124、および123 mAh / gです。それぞれ。後のサイクルでは、LCO-LLTO-10はそれ以降、優れた容量保持を実行し、この研究では、サイクルの安定性とカソード-電解質界面での電荷キャリア輸送のバランスを最適化できる可能性があります。
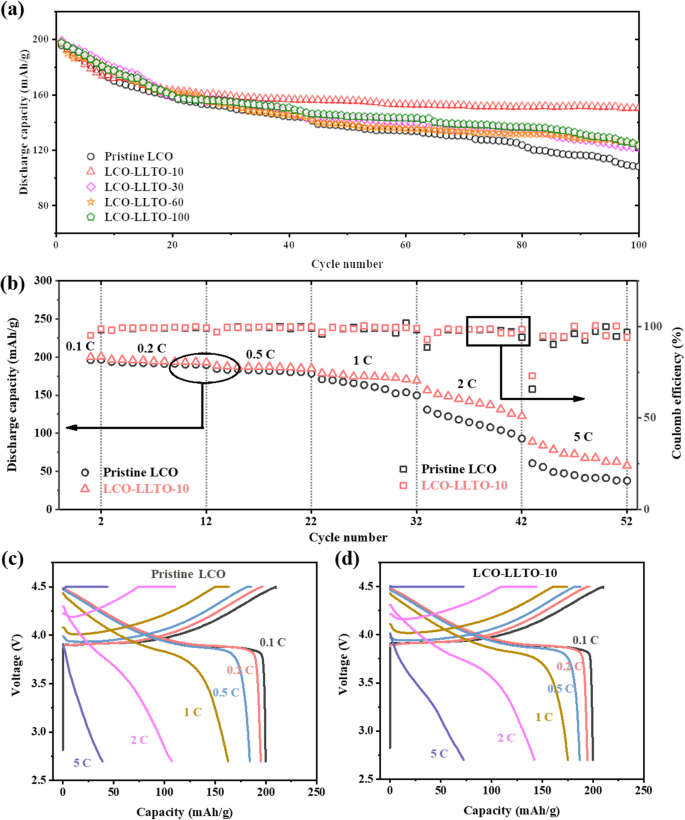
a 手付かずのLCOに基づく電極と、異なる堆積時間でα-LLTOによって変更された電極のサイクル性能。 b 手付かずのLCOおよびLCO-LLTO-10のパフォーマンスを評価します。 c 、 d c の電圧対容量のプロット 手付かずのLCOと d さまざまなサイクリングレートでのLCO-LLTO-10
容量のかなりの低下が図2aで観察できることに注意する必要があります。これは、LCOの不可逆的な相転移と結晶構造の破壊に起因するはずですが、提示された研究では、電極レベルのLLTOコーティングが高電圧でのLCOのサイクル安定性。他方、外来元素のドーピングによって高電圧でサイクルされるLCOの構造安定性を改善する努力は、最近大きな進歩を遂げた[38,39,40]。 LiCoO 2 のパフォーマンスを促進するための戦略を開発することは有望です。 コーティングとドーピングの相乗効果に基づく高電圧で。
サイクリングレートが増加するにつれて、α-LLTO修飾のプラスの効果はますます顕著になります(図2b)。異なるサイクル速度での元のLCOとLCO-LLTO-10の平均放電容量を表1に示します。0.1Cで2回の活性化サイクルの後、元のLCOの比容量はわずかに低くなりますが、LCO-LLTOの比容量に非常に近くなります。 -0.2Cおよび0.5Cで-10。ただし、LCO-LLTO-10は、サイクリング速度が1 Cを超えると、元のLCOよりも著しく高い容量を示します。たとえば、LCO-LLTO-10の放電容量は5で72 mAh / gに達します。 Cは、元のLCO(39 mAh / g)よりも84.6%高くなっています。さらに、元のLCOの放電電圧プラットフォームは2 Cでほとんど消失しました(図2c)。これは、電荷移動速度が制限されているために界面分極が悪化していることを示しています。一方、LCO-LLTO-10は、2 Cで観測可能な放電電圧プラットフォーム(〜3.76 V)を実行します(図2d)。 LCO-LLTO-10の優れたレート容量は、適切なα-LLTO堆積時間による表面改質が、Li + の導電性ネットワークを保持するだけではないことを示しています。 およびe − 電極内だけでなく、何らかの形でその電荷輸送および/または移動を強化します。
<図>レート性能のテストに使用されたセルは、最初の20サイクルで急速な容量低下を示さなかったことに注意する必要があります(図2b)。これは、図2aに示されている傾向とは著しく異なります。レート性能テストの前に、0.1 Cでの2つの活性化サイクルに起因するはずです。これらの2つのサイクルは、均一で高密度のカソード電解質中間相(CEI)層を形成するのに役立つ可能性があるためです。
堆積したα-LLTOがLCO電極の伝導に及ぼす影響を調べるために、元のLCOおよびLCO-LLTO-10のEIS測定を、カソード-液体電解質-リチウム金属構成を使用して室温で実施します(図3a)。 Z のさまざまな切片 re それらのEIS曲線の軸は、LCO-LLTO-10を使用してテストしたセルは、元のLCOを使用したセルよりもはるかに小さい総抵抗を持っていることを示しています。低周波数での傾斜線は、Li + に関連するWarburgインピーダンスから導き出されます。 LCO電極内の拡散[41]。 Li + 拡散係数\({D} _ {Li ^ {+}} \)は、次の式で計算できます。 1 [42]:
$$ {D} _ {Li ^ {+}} =0.5 \ times {\ left(\ frac {RT} {AC \ updelta {F} ^ 2 {n} ^ 2} \ right)} ^ 2 $$( 1)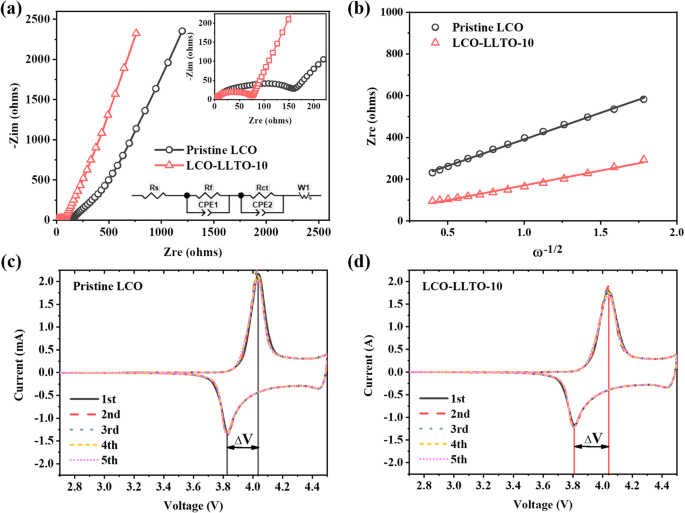
a 手付かずのLCOおよびLCO-LLTO-10と等価回路モデルの電気化学的インピーダンススペクトル。 b Z re 間の相関 およびω −1/2 手付かずのLCOおよびLCO-LLTO-10の; c 、 d c のCVプロファイル 手付かずのLCOと d LCO-LLTO-10、掃引速度0.05 mV / s、2.75〜4.5 V
ここで R は理想気体定数(J /(mol * K))、 T はケルビン温度(K)、 A は有効な電気化学的界面面積(cm 2 )、 n はキャリアイオンの電荷数、 F はファラデー定数(C / mol))、 C Li + です 単位格子体積中の濃度(mol / cm 3 )、およびδ はウォーバーグ係数(Ω*(rad / s) 0.5 )。ウォーバーグ係数δ 式によって決定することができます。 2 [42]:
$$ {Z} _ {re} ={R} _ {\ mathrm {total}} + \ delta {\ omega} ^ {-1/2} $$(2)ここで Z re ウォーバーグインピーダンス、 R 合計 は斜線の開始抵抗であり、ω は、インピーダンス掃引周波数 f に対応する角周波数です。 (ω=2π f )。 Z によると re vs. ω −1/2 図3bに示すプロットでは、LCO-LLTO-10の\({D} _ {Li ^ {+}} \)は7.52×10 -12 であると決定されます。 cm 2 / s、これは元のLCOよりもはるかに高い(2.32×10 -12 cm 2 / s)。これは、LCO電極のバルクイオン伝導が堆積したα-LLTOによって強化されることを示唆しています。
堆積したα-LLTOがLi + に及ぼす影響 LCO-電解質界面を横切る輸送はもっと顕著でなければなりません。測定されたインピーダンススペクトルは、図3aの挿入図に示されている等価回路モデルにさらに適合します。ここで、 R s 、 R f 、および R ct 電解質のバルク抵抗、カソード表面の固体電解質中間相の抵抗、および電荷移動抵抗をそれぞれ表します。その結果、LCO-LLTO-10ははるかに低い R を示します ct (40.9Ω)元のLCO(101.8Ω)よりも、堆積したα-LLTOが大幅に強化されたLi + であることを示しています。 LCO-電解質界面を通過する輸送。
追加されたインターフェースは、電荷の輸送および移動の困難さを高めると一般に考えられている。ただし、上記のEIS分析は、Li + バルクでの輸送と界面を横切る電荷移動の両方が、LCO電極の表面へのα-LLTOの堆積によって改善されます。これは、LCO-LLTO-10の観測された優れたレート容量(図2cおよびd)とよく一致しており、次の事実に起因する可能性があります。まず、堆積したα-LLTOのイオン伝導率はLCOのイオン伝導率よりもはるかに高くなります(〜10 -8 S / cm)[43]。第二に、物理蒸着であるスパッタリングプロセスは、堆積されたα-LLTOがLCO粒子と十分に接触した界面を形成することを可能にします[19、20]。第三に、堆積されたα-LLTOは追加のLi + を提供する可能性があります 電極内の輸送経路[19、42]。
R の減少は一般的に考えられています ct CVプロファイルのレドックスピーク間の差である分極電圧(ΔV)が小さくなります。図3cおよびdは、5回のスイープサイクルでの未処理のLCOおよびLCO-LLTO-10のCVプロファイルを示しています。 ΔVの値は表2にまとめられています。予期せぬことに、LCO-LLTO-10は、5回の掃引サイクルで元のLCOよりも大きなΔVを示します。小さい R 間の矛盾 ct LCO-LLTO-10のより大きなΔVは次のように説明できます。実験的に決定された R ct LCO-LLTO-10の場合、LCO-LLTOインターフェイスから派生する可能性がありますが、 R ct 手付かずのLCOの場合、LCOと液体電解質の間の界面に由来します。上記のように、物理蒸着により、LCO-LLTOインターフェースが十分に接触し、 R が減少します。 ct LCO-LLTO-10の場合。一方、ΔVは液体電解質からLCOまでの総インピーダンスから導き出されます。 α-LLTOの導入により、LCO-LLTO-電解質構成にLCO-LLTOおよびLLTO-電解質界面の2つの界面が追加される場合があります。さらに、α-LLTOは、最も導電性の高い固体電解質の1つですが、液体電解質のイオン伝導度よりもはるかに低くなっています。したがって、LCO-LLTO-10を使用したサンプルでは、より大きなΔVが観察されます。カソードと電解質の間の電荷移動は一般に律速段階であるため、Li + α-LLTO固体電解質とLiPF 6 間の輸送 ベースの液体電解質は比較的高速である必要があり[42]、LCO-LLTO-10で観察されるより良いレート容量とより大きなΔVが妥当です。さらに重要なことに、LCO-LLTO-10は5回の掃引サイクルで一定のΔVを維持しますが、元のLCOのΔVは変化し、増加傾向を示します(表2)。これは、元のLCOと液体電解質の間の界面が継続的に劣化している一方で、LCO-LLTO-電解質構成が優れた界面安定性につながることを意味します。
<図>上記のように、個々の粒子上の非導電性材料のコーティング層は、界面電荷移動を妨げる可能性がある。一方、 R の分析 ct ΔVは、LCO電極と液体電解質の間の電荷移動が、堆積したα-LLTOの非常に薄い層によって促進されることを示しています。したがって、LiCoO 2 のサイクリング安定性とレート性能を期待することは合理的です。 個々の粒子が導電性α-LLTOの極薄層で十分にコーティングされている場合は、さらに改善する必要があります。
高いカットオフ電圧で循環するLCOの劣化を引き起こす可能性のあるメカニズムには、脱リチウム化LCOによる電解質酸化[44]、LCOの酸素損失[45、46]、Co溶解[47]、およびHF腐食が含まれますが、これらに限定されません。カソード-電解質界面[48]。堆積したα-LLTOが界面の安定化にどのように役立つかを明らかにするために、100回の充放電サイクル後にXPSによって元のLCOとLCO-LLTO-10に基づく電極の表面化学を分析します。 La、Ti、およびOの信号は、サイクルされたLCO-LLTO-10から得られたスペクトルではるかに強く(図4a)、サイクリング中にLaおよびTiが電解質に溶解しないことを示しています。さらに、LLTOのチタン酸塩酸素に起因する530 eVのピークが、循環LCO-LLTO-10から得られたO 1sスペクトルで観察されます(図S3)。さらに、F 1sスペクトルは、PVDFと吸収された液体電解質に由来する2つのピークのみを示し、他のフッ化物(LaF 3 )に関連するピークはありません。 、TiF 3 、またはTiF 4 )が観察されます(図4b)。これらの観察結果は、LCO電極表面に堆積したα-LLTOが長期間の充放電サイクル中に安定していることを示唆しています。
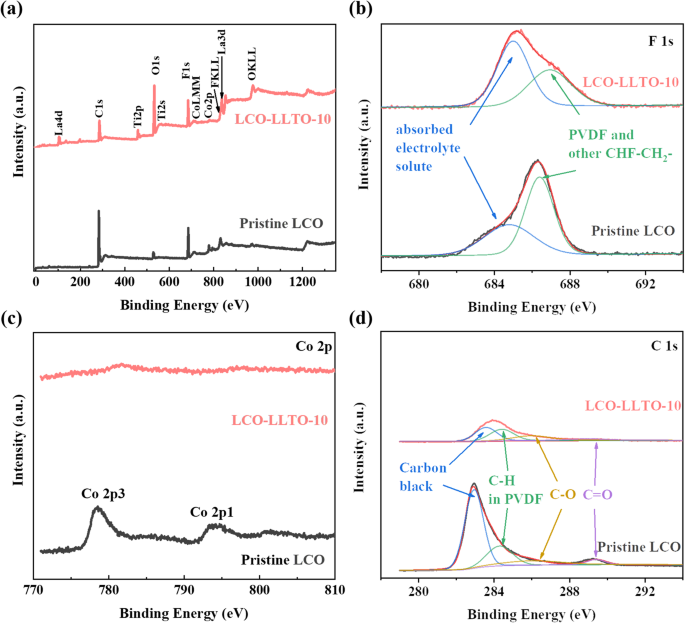
100サイクル後の元のLCOおよびLCO-LLTO-10のXPSスペクトル。 a フルスペクトル、 b F 1のスペクトル、 c Co 2pスペクトル、および d C1のスペクトル
LCO-LLTO-10の場合、望ましくない副反応のためにHFが形成された場合、LCO粒子は堆積したα-LLTOによってHF腐食から保護されます。 LCO-LLTO-10に由来するより強いO信号(図4a)は、LCOの酸素損失が堆積したα-LLTOによって潜在的に防止されることを意味します。さらに、LCO-LLTO-10は、元のLCOと比較して、吸収された液体電解質溶質に起因するはるかに強いピークを示します(図4b)。これは、堆積したα-LLTOが電極表面の液体電解質の湿潤性を向上させるか、液体電解質の分解を抑制することを示しています。 Co 2pに対応するピークは、LCO-LLTO-10ではほとんど観察されませんが、元のLCOでは明らかです(図4c)。堆積したα-LLTOはCo 3 + / 4 + の拡散を防ぐ可能性があります 電極の表面と液体電解質への溶解。 C1sスペクトル(図4d)で観察された283 eV、285 eV、286 eV、および289 eV付近のピークは、カーボンブラック、PVDF、ポリエーテルカーボン(O–C–O)、およびカルボニル基(C =O)に関連しています。 、それぞれ[33、49]。一般に、ポリエーテルの炭素とカルボニル基は電解質の分解に起因すると考えられています[33、49]。 LCO-LLTO-10から得られた曲線にC =Oピークがないことは、cacoethic副反応の少なくとも一部が堆積したα-LLTOによってブロックされていることを示しています。上記の分析に基づいて、4.5 VでのLCOカソードの安定性の問題のほとんどは、堆積したα-LLTOによって対処する必要があります。
結論
要約すると、高いカットオフ電圧でのLCOのサイクル安定性とレート容量は、構成された電極の表面にα-LLTOを堆積することによって改善されました。堆積したα-LLTOがLCO-電解質界面に及ぼす影響を詳細に調べた。結果は、HF腐食、Co溶解、およびその他の望ましくない副反応など、高いカットオフ電圧でのLCOの安定性の問題のほとんどは、堆積したα-LLTOによって対処できることを示唆しています。さらに、両方のLi + 導電性α-LLTOを導入することにより、バルク輸送とLCO-電解質界面を通過する電荷移動が強化されました。適切な堆積時間で、α-LLTOによる表面改質により、LCOは2.75〜4.5 V vs 。内で安定したサイクルを実現しました。 Li + / Liであり、0.2Cで150mAh / gの可逆容量を実行しました。高いサイクリングレートでは、α-LLTO修飾のプラスの効果がより顕著になります。ここで紹介するLCOの表面改質戦略は、LIBのエネルギー密度とサイクル寿命を改善するための有望な手段を提供します。
データと資料の可用性
この記事の結論を裏付けるデータは、記事とその追加ファイルに含まれています。
略語
- LIB:
-
リチウムイオン電池
- LCO:
-
LiCoO 2
- LLTO:
-
Li 3x La 2 / 3-x TiO 3
- α:
-
アモルファス
- HF:
-
フッ化水素酸
- SEM:
-
走査型電子顕微鏡
- CV:
-
サイクリックボルタンメトリー
- EIS:
-
電気化学インピーダンス分光法
- XRD:
-
X線回折
- EDS:
-
エネルギー分散型分光計
- XPS:
-
X線光電子分光法
- PVDF:
-
ポリ(フッ化ビニリデン)
- EC:
-
エチレンカーボネート
- DMC:
-
炭酸ジメチル
- EMC:
-
エチルメチルカーボネート
- CEI:
-
カソード電解質中間相。
ナノマテリアル
- 材料:表面特性が改善され、充填挙動が最適化されたEPPフォーム
- 誘電体メタ表面を介した帯域幅の拡大による完全なテラヘルツ分極制御
- アニーリングによって酸化ケイ素膜上に成長したアモルファスシリコンナノワイヤ
- AFMチップベースの動的耕起リソグラフィーを使用したポリマー薄膜上での高スループットのナノスケールピットの製造
- PEG化リポソームを介したブファリンの改善された抗腫瘍効果および薬物動態
- ITO / PtRh:PtRh薄膜熱電対の調製と熱電特性
- AgNWs電極を備えたテクスチャ表面に基づくPEDOT:PSS / n-Si太陽電池の高性能
- 超長くて細い銅ナノワイヤの容易な合成とその高性能で柔軟な透明導電性電極への応用
- Ptナノ粒子表面プラズモンとのカップリングによるMgZnO金属-半導体-金属光検出器の大幅な強化
- PECVDによる低欠陥密度nc-Si:H薄膜の堆積のための便利で効果的な方法
- 銅タングステン電極で耐摩耗性を向上



