金属酸化物/グラフェン/ CNTベースのナノバイオセンサーの最近の進歩に関する概要
要約
ナノバイオセンサーは、化学的および生物学的因子を検出し、その結果を、物理化学的検出器によってシグナルトランスデューサーの表面に固定化された生物学的に活性な分子と認識要素の間の意味のあるデータに変換する、便利で実用的で感度の高いアナライザーです。ナノバイオセンサーは、高速で正確かつ信頼性の高い動作特性により、臨床および非臨床アプリケーション、ベッドサイドテスト、医療繊維産業、環境モニタリング、食品安全などで広く使用されています。これらの重要なアプリケーションで重要な役割を果たします。したがって、バイオセンシングインターフェースの設計は、ナノバイオセンサーの性能を決定する上で不可欠です。ナノ材料のユニークな化学的および物理的特性は、バイオセンサーの新しく改良されたセンシングデバイスへの道を開いた。改善されたセンシングおよび選択性機能、短い応答時間、検出下限、および低コストを備えたデバイスに対する需要の高まりにより、バイオセンサーの足場として使用されるナノバイオマテリアルに関する新たな調査が行われています。他のすべてのナノ材料の中で、金属酸化物ナノ構造、グラフェンとその誘導体、カーボンナノチューブに基づくナノバイオセンサーの開発、およびハイブリッド構造としてのこれらのナノ材料の広範な使用に関する研究が最近注目を集めています。これらのナノ構造を組み合わせて作成されたナノハイブリッド構造は、高い電極触媒活性により、将来のバイオセンサーのニーズを直接満たします。このレビューは、これらのナノ材料とその誘導体に関する最近の開発、およびバイオセンサーの足場としてのそれらの使用に取り組んだ。これらの人気のあるナノマテリアルを、比較研究、表、およびチャートで評価することによってレビューしました。
はじめに
バイオセンサーは、生物学的分析物からの信号を、他の物理化学的物質に巻き込まれている可能性のある分析物の定性的および/または定量的検出のための測定可能で識別可能な電気信号に変換する診断デバイスです[1]。最初の既知のバイオセンサーはクラークらによって開発されました。 [2]酸素の検出用であり、Clark and Lyons [3]によって開発された最初のアンペロメトリー酵素電極は、酵素ベースのグルコースバイオセンサーでした。長年にわたり、酵素ベース、組織ベース、デオキシリボ核酸(DNA)ベース、および熱的、光学的、電気化学的バイオセンサータイプが開発されてきました。バイオセンサーは、臨床診断、生物医学部門、食品生産、分析などの一部のアプリケーションで、従来の方法よりも安定した正確な結果を提供します[2、4]。さらに、特異性、選択性、簡単な操作によるコスト削減、リアルタイム分析、継続使用などの特性により、さまざまな種類のバイオセンサーが世紀の後半に急速に開発され、関連する医療で広く使用されるようになりました。環境および法医学分野[5]。これらの重要なアプリケーション分野での集中的な使用により、高感度、安定性、高選択性、長寿命、再現性、シンプルさと安価さ、広い測定範囲、高速応答時間など、バイオセンサーから期待されるいくつかの機能が生まれました。
国際純正応用化学連合(IUPAC)によると、バイオセンサーには、生物学的認識要素、トランスデューサーコンポーネント、およびトランスデューサーと組み合わされることが多い電子システムの3つの主要コンポーネントが含まれています。統合された受容体-トランスデューサーデバイスとして、バイオセンサーは生物学的認識要素を使用して選択的な定量的または半定量的分析情報を提供することができます[7](図1)。このフレーム内で、核酸、酵素、抗体、受容体、微生物、細胞、組織、さらには生体模倣構造でさえ、生物学的検出のための生体受容体として利用される可能性があります。
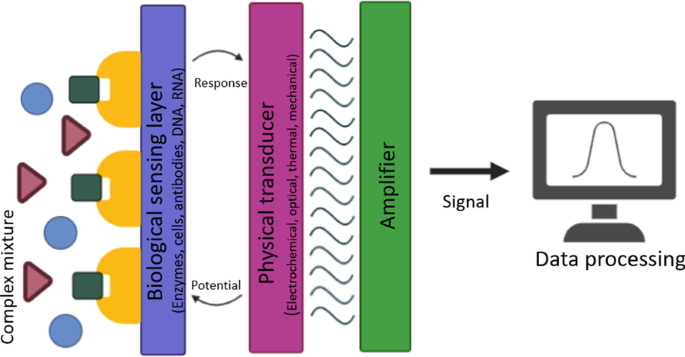
バイオセンサーの概略図
バイオセンサーの設計は、分析物が出現する可能性のあるあらゆる状況またはあらゆる位置での迅速かつ便利なテストにとって非常に重要です。その設計の範囲内で、トランスデューサのコンポーネント材料も検出品質に大きな影響を及ぼします。物理的なトランスデューサーは、定量化可能な信号源によって大幅に異なり、主に光学および電気化学システムを利用します[5]。物理的トランスデューサーとして使用される材料の物理化学的、電子的/光学的/電気化学的特徴は、バイオセンサーの性能に直接影響します。さらに、バイオセンサーの効率と有効性は、酵素の固定化に使用されるマトリックス、メディエーター、および安定剤によって決定されます。したがって、物理的なトランスデューサコンポーネントが生成される材料の特性は、バイオセンサーの高い信号安定性と再現性、およびそれらの選択性などの機能を取得する上で重要な役割を果たします。バイオセンサーの前述の3つのコンポーネントの中で、このレビューは主にナノ材料を使用したトランスデューサーコンポーネントの表面機能化に関する最近の開発に焦点を当てています。
トランスデューサーは、主に電気化学、生物発光、圧電、熱量測定、光学の4つのクラスに分類できます。トランスデューサーの表面は、センサーの性能を向上させるために、多くの異なる機能材料を使用して変更することができます。これらの材料の構造、形態、および特性を制御することも同じように役立ちます。これらの材料の中で、ナノ材料と呼ばれるナノサイズの材料は、大きな表面積、改善された電気などの独自のサイズ依存特性を備えた、より広いアプリケーション領域向けの新規で適応性のある高感度バイオセンサーの開発に不可欠な大きな可能性を秘めています導電性、および高い化学反応性。これらの並外れた特性を考慮すると、ナノ材料は、高感度バイオセンサーの構築に必要な要件を満たすための好ましい候補の1つです[6]。
ナノマテリアルと見なされるには、少なくとも1次元で、ナノマテリアルのサイズは1〜100nmである必要があります[8]。それらの非常に微細なサイズのために、ナノ材料では、ほとんどの原子は表面の近くに存在するか、表面に存在します。これらのナノ粒子(NP)は、物理化学的特性の向上、表面積の増加、電子の距離の短縮などの顕著な特徴を適切に獲得しており、バルクサイズのナノ粒子と比較して大きな違いをもたらします。したがって、ブーストされた性能は、これらのナノスケール材料の光学的、熱的、電気的、および磁気的特性において維持され、バイオセンサーコンポーネントとしての使用に非常に効果的である。さらに、より高い表面積を有するナノサイズの材料は、電極の表面上に十分な数の生体受容体を固定化するための適切な空間を提供する。したがって、研究者は最近、バイオセンサー用途のためのナノ材料の製造、特性評価、および使用に大きな関心を示しています[9、10]。
すべてのナノ材料の中で、MON、グラフェンとその誘導体、およびCNTは、その独自の機能で際立っています[11、12]。 MONは、その印象的な形態学的多様性、非毒性、および生体適合性により、重要な触媒特性を示します。 MONは生体分子の固定化に適した構造を提供することにも注意する必要があります。
それらの結晶格子は、量子閉じ込め効果によるセルパラメータと電気化学的特性の変更を可能にし、導電率と化学反応性に影響を与えるそれらの表面特性を変更することによるバンドギャップの制御可能性により、バイオセンシング要素として使用され、MONをバルクから区別する可能性が高くなりました対応する[12、13]。さらに、複合構造を形成することによってこれらの特性をさらに改善するために、MONは最近、グラフェンやCNTなどのカーボンナノ材料と広範囲に組み合わされて、ナノハイブリッド構造を形成しています。そうすることで、検出と診断の電気化学的反応性が向上し、バイオセンサーの感度や選択性などの将来の要件を満たすことができます[14]。
これらのカーボンナノ材料とMONの混成は、優れた光学的、磁気的、および電気的特性を備えた1つまたは複数の機能を備えた高度なバイオセンサーの製造を提供します[14、15、16]。グラフェンとその誘導体は、他のナノ材料と簡単に統合して、ナノハイブリッド材料を作成し、目的の電気化学的活性を得ることができます[13、17、18]。たとえば、多くのアプリケーションでは、グラフェンはタンパク質の酸化還元応答への電子伝達を促進するための有用なツールと見なされています[19]。しかし、生物学的環境におけるグラフェンの物理的安定性と細胞に対する毒性評価については、まだ議論の余地があります[20、21、22]。一方、CNTは、グラフェンとは異なり、キラリティーが変化するため、光学的特徴が異なり、光学バイオセンシングアプリケーションでグラフェンと比較して有利になります[23]。優れた電気化学的能力を備えたCNTは、化学的に容易に変更可能であり、グラフェンのように表面積対体積比が高くなっています[24]。表面特性に関しては、周囲にさらされると、グラフェンはその単層の2次元の性質のためにすべての体積でさらされますが、この露出は1次元(1D)CNTの場合に制限されます[25]。さらに、グラフェンは、CNTに比べて優れた生体分子センシングと信号対雑音比の特性により、干渉に対する選択性が高いことが以前の研究で何度も報告されています。これは主に、表面積の大きいグラフェンの金属を含まないグラファイトエッジによるものです。それにもかかわらず、残留金属触媒の存在により、信号摂動としての問題がCNTベースのバイオセンサーに存在します[25]。前述のすべての側面で、グラフェンおよび/またはCNT構造の組み合わせによって形成されたナノハイブリッドは、高度なバイオセンサーの設計において重要な役割を果たす可能性があり、それらから複合構造を形成することによる両方の材料の欠点の補償は、これらの問題と検出を克服します最大化することができます。 MON、グラフェン、およびCNTの複合構造によって作成された協力を利用して、改善された信号増幅を提供し、高度なバイオアフィニティ戦略を準備することが不可欠であると思われ、将来の要件を満たすために改善されたバイオセンシングデバイスの開発につながります。したがって、このレビューの範囲内で、最近実現されたMON、グラフェン、およびCNTベースのバイオセンサーに焦点を当てています。さらに、これらのナノ材料を単独でではなく、一緒に使用することの重要な役割が、それらの組み合わせによって得られる優れた特性を備えたバイオセンサーの製造において議論されてきた。将来の期待と課題を評価することにより、さらなる研究のための代替的な視点を提案したいと思います。
金属酸化物ナノ構造ベースのバイオセンサー
金属酸化物(MO)は、1954年の最初のバイオセンサー研究以来、センサーアプリケーションの重要な候補となっています[26、27]。 MOは、NP [28、29]、ナノファイバー[30]、ナノスフェア(NS)[31]、ナノロッド[32]、ナノチューブおよびナノワイヤー(NW)[33]、ナノシート[34、35]などのさまざまなナノ形態で合成できます。 。形態学的多様性に加えて、MONはいくつかの利点を提供します:高い表面積/体積比、非毒性、優れた生体適合性、化学的安定性、優れた選択性、電子とフォノンの制限、高い触媒効率、および強力な吸着能力、物理化学的界面の特徴[36,37,38、 39,40]。さらに、MONは、高周波(RF)マグネトロンスパッタリング[41,42,43]、熱蒸発[44、45]、プラズマ化学気相成長法(PECVD)[46]などの比較的簡単で費用効果の高い方法で製造できます。 、47]、分子線エピタキシー[48]、およびソルゲル技術[49]、化学蒸着プロセス[50]、および水熱法[51]。これらの重要な機能により、MONは生物医学アプリケーションおよびバイオセンサー市場で最も望ましい材料の1つになっています。 2010年から2020年までのMONに関する出版物が分析され、図2に、MONの生物医学的応用の分布として示されている円グラフとともに示されています。
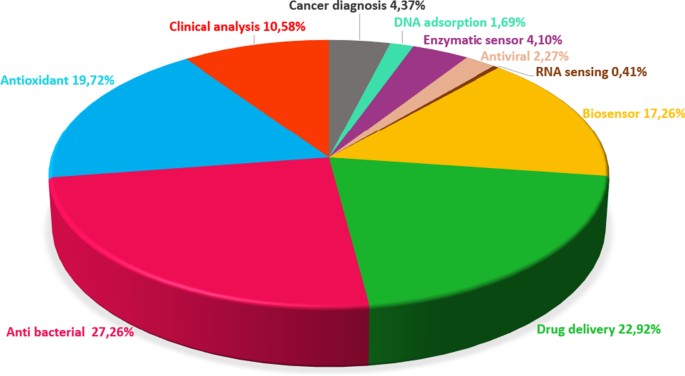
生物医学アプリケーションにおけるMONの分布を示す円グラフ
一方、主に近年では、ZnO、Fe 3 などのさまざまなMON O 4 、CuO、NiO、TiO 2 、MgOは、多用途で機能的なバイオセンサーとして長い間継続的に製造されてきました[44、52]。 MONの中で、ZnOとFe 3 O 4 、それらの広範な用途のために、バイオセンサー構築における著名なメンバーであると考えられている[53、54]。
ZnOナノ構造
ZnOナノ構造は、高い等電点(IEP〜9,5)[55]、ワイドバンドギャップ、有用な電子通信機能、高い化学的安定性、優れた生体適合性などの独自の特性により、新しいナノ構造バイオセンサーの製造に大きな役割を果たします。と圧電性。特に、その高い等電点は、なぜZnOがバイオセンシング技術に使用される最も一般的な金属酸化物であるかを明確に説明しています。さらに、ZnOは環境に優しく安全な材料であるため、すべての臨床または非臨床用途で利用できます[53、54、56]。たとえば、Akhtar etal。 [57]は、より大きな表面積を持つ花のようなZnOナノ構造を利用することにより、アルツハイマー病やインスリン依存性II型糖尿病などの神経変性疾患の診断におけるアミロイド検出のための蛍光増強のメカニズムに基づく試薬レス光学バイオセンサーを開発しました。 。さらに、ZnOナノフラワーは、より高速で費用効果の高いアミロイドバイオセンサーを提供する優れた性能向上材料であると報告されています[57]。さらに、糖尿病患者のためのウェアラブル連続グルコースモニタリングアプリケーションに関連するZnOナノロッドベースの電界効果トランジスタ(FET)を使用するグルコースバイオセンサーは、水熱法を介してZong and Zhu [54]によって製造されました。彼らは、1.6 mA / µM cm 2 の高感度を備えた高性能バイオセンサーを実現しました。 180 µm 2 の小さな検出領域を備えています ZnOナノロッドの表面積対体積比が大きいため、検出限界は1 µMです[54]。 Sahyar etal。 [58]は、肉の腐敗を早期に検出するための新しいAgドープZnONPベースのバイオセンサーを開発しました。酵素キサンチンオキシダーゼ(XO)修飾電極(nanoAg-ZnO /ポリピロール(PPy)/鉛筆グラファイト電極)を用いた分析の結果、得られた酵素バイオセンサーは0.03μA/ mMの感度で高い選択性を示し、 0.07μMの低検出限界[58]。
別の研究では、Yue等。 [59]、Au NPs-ZnOナノコーンアレイ/グラフェンフォーム電極に基づく理想的なドーパミン(DA)バイオセンサーの開発に成功しました。彼らの特性評価では、彼らが変更した電極が高感度(4.36μAμM -1 )を持っていることを証明しました。 )およびDAの検出における低い検出限界(0.04μM、S / N =3)。さらに、彼らは、ZnOナノコーンベースの電極が、優れた選択性、優れた再現性、および尿酸(UA)干渉下での安定性を示したことを報告しました。彼らはまた、電極が医学と健康管理において途方もない可能性を持っていることを強調しました[59]。同じ年に、銭等。 ZnONPを使用した電気化学的グルコース検出器を開発しました。センサーはCeO 2 で構成されています ナノウィスカーはZnONPで装飾されており、彼らはZnO / CeO 2 ナノコンポジット構造は、表面積が大きく、毒性がなく、電極触媒活性が高い。ナノコンポジットは、0.5〜300 µMの線形範囲と0.224 µM(40 ppb)の検出限界(LOD)で、グルコースを検出するための並外れた性能を示しました。彼らはまた、ナノコンポジットセンサーが電流信号強度とグルコース濃度( R )の間に優れた線形関係を示したことを強調しました。 2 =0.99944)[60]。別のグルコースバイオセンサーは、Rafieeらによって開発されました。 [61]高い導電率と化学的安定性で知られるグラフェンナノプレートレット(GNP)と、グルコースに敏感であることが知られているZnONWを組み合わせることによって。彼らの研究では、GNP1、GNP2、およびGNP3として定義される3つの異なる濃度(0.5、1、および2 mg)のGNPの薄膜上でZnO NWを合成することにより、グルコースバイオセンサーのようなデバイスの構造を変更しました。このシステムは、ZnO NWとGNPの二重効果が、効率的なグルコースバイオセンサーの完全な改善につながることを示しました。たとえば、彼らは、低グルコース濃度の場合、溶液中のグラフェンの量が増えるとデバイスの応答が増加し、GNPの数が増えるとセンサーの応答時間が減少することを指摘しました。さらに、彼らは、30 mg / dLのグルコースに30日間曝露した後、GNPで修飾されたサンプルで、長期安定性、つまり、理想的なバイオセンサーの重要な基準である濃度関係に対する一貫した耐性が観察されたことを報告しました。その結果、彼らは、5秒の応答時間、0.003〜30,000 mg / dLの検出範囲、および長期の電気的安定性という有用な機能を備えた理想的なグルコースバイオセンサーを提示しました[61]。これらの研究に加えて、さまざまな酵素の検出にさまざまなZnOナノ構造を使用した他のいくつかの最近の研究を表1に示します。
<図>表1に示した現在の研究を考慮すると、さまざまな形態のさまざまな方法で生成されたZnO構造が表現でき、複合構造への統合が容易なため、引き続き広く使用されています。代替生産と形態学的多様性、および他のナノ材料、特にカーボンナノ構造とのナノコンポジットおよびナノハイブリッド構造の形成は、理想的なバイオセンサーで期待される特性を完全な効率で満たすという点で、ZnO構造に並外れた可能性を提供します。
Fe 3 O 4 ナノ構造
近年、Fe 3 O 4 ナノ構造は、優れた生体適合性、低毒性、超常磁性、触媒活性、および調製と修飾プロセスの容易さなどの優れた特性のおかげで、バイオセンサー、ドラッグデリバリー、細胞分離、薬局など、多くの有望なアプリケーションに大きな関心を呼んでいます。磁性Fe 3 O 4 NPは、その磁気的性質による媒体からの単純な分離能力[77]により、酵素などの目的の生体分子の固定化に適しています[73,74,75,76]。 Fe 3 O 4 磁性NPとその誘導体は、バイオセンサー技術で広く使用されており、さまざまな魅力的な研究が文献で議論されています[75、78]。これに関連して、Sanaeifar etal。 [75]は、グルコース検出用の新しい電気化学バイオセンサーを設計しました。彼らは、Fe 3 を分散させて調製したナノコンポジットの電気化学的性能を評価しました。 O 4 ポリビニルアルコール(PVA)での共沈法によって生成された磁性NP。彼らは、Fe 3 O 4 固定化されたグルコースオキシダーゼに対して優れた触媒特性を有するPVAマトリックス中のNPは、酵素と電極表面の間の電子移動速度を増加させました。準備した生体電極は、5 \(\ times \ hspace {0.17em} \)10 -3 の範囲でグルコースを測定できます。 〜30 mM、感度9.36 µA mM -1 検出限界は8µM未満でした[75]。ドンら[79] Ag / Fe 3 を開発 O 4 環境保護のためのヒドラジンの検出に使用される、単純なソルボサーマルアプローチによって生成されたコアシェルNSベースのセンサー。彼らは、高性能ヒドラジンセンサーの応答時間が2で、線形範囲が0.25〜3400 µm、感度が270 µA mM -1 であると報告しました。 cm − 2 、および0.06μMの検出限界。図を比較すると、文献の他のセンサーよりもはるかに優れたヒドラジンセンサーが開発されました[79]。
別の研究では、Sriram等。 [80]開発されたFe 3 O 4 尿および血清サンプル中のUAを検出するためのNS /還元型酸化グラフェン(rGO)ナノコンポジット。それらの電気化学的分析の結果、Fe 3 O 4 NSs /還元グラフェンオキシド(rGO)ナノコンポジットは、高い安定性と再現性を備えており、優れた電気化学的還元ピークを示しました。さらに、彼らは、開発したUAセンサーの線形範囲が0.02〜783.6 µMであり、LODが0.12nMであることを強調しました[80]。同様に、酸化グラフェン(GO)とFe 3 を組み合わせたDA検出用の新しいバイオセンサー O 4 カイらによって開発されました。 [81]。彼らの研究では、Fe 3 の合成に成功しました。 O 4 / GO /元のグラフェン(PG)分散および共沈法による三元複合材料。その後、彼らは、ドロップ技術によって、作用電極であるグラッシーカーボン電極(GCE)にナノコンポジットを堆積させました。最高ピーク電流はFe 3 で記録されます O 4 サイクリックボルタモグラム(CV)の/ GO / PG構造。同様に、彼らは、DAの存在下での最高ピーク電流はFe 3 に属すると報告しました。 O 4 / GO / PG / GCEサンプル。彼らはまた、Fe 3 のピーク電流の増加を強調しました O 4 DA濃度の増加による/ GO / PG / GCEサンプル。最後にカイら。電気化学センサーはDA検出に効果的に使用できると述べた[81]。 Fe 3 に関するいくつかの代表的な研究 O 4 バイオセンサーコンポーネントとしてのナノ構造を表2に示します。
<図>それらの優れた特性にもかかわらず、磁性Fe 3 O 4 ナノ構造は、バイオセンサーおよび生物学的用途において制限的な問題を抱えています。それらの高い表面エネルギー、化学反応性、および強い磁気相互作用のために、それらは非常に凝集しやすく、Fe 3 の安定化を困難にします。 O 4 磁気ナノ構造。この問題を克服するために、Fe 3 の表面 O 4 ナノ構造はポリマー層でコーティングされています[95]。ただし、ポリマーで表面をコーティングすると、電気化学的バイオセンサーの用途の観点から効率が低下する可能性があります。したがって、磁性Fe 3 の安定化において O 4 ナノ構造、遺伝子、細胞、酵素、タンパク質などの生体分子、およびその他の必須のナノ構造(グラフェン、CNT、量子ドット、NPなど)を使用できます。したがって、磁性Fe 3 に基づく複雑なナノハイブリッドおよびナノコンポジットシステムが予測できます。 O 4 ナノ構造は、将来、新世代のバイオセンサーを製造する際の現象になるでしょう。
結局のところ、さまざまなナノ構造を組み込んだMOベースのバイオセンサーは、実用的および産業的アプリケーションにおいて独自の斬新な機能を発揮します。 MOのナノ構造は、比類のない特性により、高感度、高速、安定のバイオセンサーの考案に大きな影響を与えます。その上、金属の各種類のナノ構造と酸化物にはその利点が含まれています。したがって、センシングデバイスの新しい進歩はバイオテクノロジーで起こる可能性があります。さらに、最近の研究ではナノカーボン構造に多くのスペースが与えられており、MOがそれらと一緒に使用されていることがわかります。したがって、この作業の第2部では、バイオセンサーで最も一般的に使用される2つのナノカーボン(グラフェンとCNT)に焦点を当てます。
グラフェンとその誘導体ベースのバイオセンサー
グラフェンは、グラファイト、CNT、フラーレン、ダイヤモンドと同様に、炭素の最も人気のある同素体の1つです。これは、sp 2 の2次元レイヤーです。 -混成炭素原子。ガイムとノボセロフによるグラフェンの発見後、透明電極、エネルギー貯蔵、薬物送達、バイオセンサー、スーパーキャパシター、バッテリー、触媒作用などのさまざまな分野で世界中で大きな注目を集めています[96、97]。グラフェンは、他の多くのナノ材料と同様に、トップダウン(機械的剥離、化学的剥離、および化学合成)およびボトムアップ法(熱分解、エピタキシャル成長、化学蒸着(CVD))によって合成できます[97]。さまざまな製造方法により、グラフェン、GQD、GO、rGO、グラフェンナノリボン(GNR)、ナノメッシュ、ナノシートなどの多数のグラフェン様材料が存在します[98]。よく使用される派生物を図3に示します。
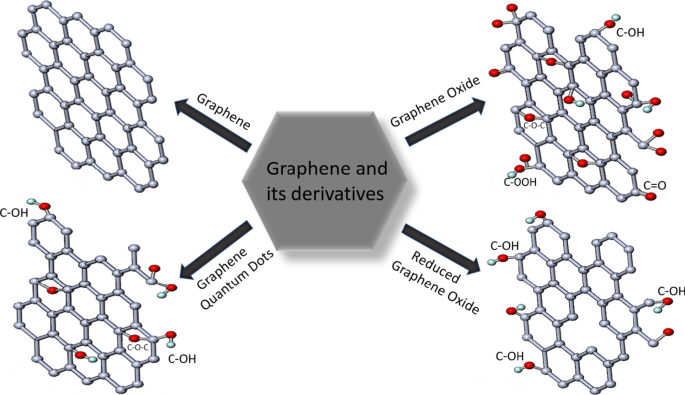
最も人気のあるグラフェンベースの材料の構造
グラフェンは、優れた熱伝導率(5000 W / mK)、室温での高い電子移動度(250,000 cm 2 )を備えています。 / V s)、大きな表面積(2630 m 2 / g)、高い弾性率(21 T Pa)、および良好な電気伝導率[99]。さらに、グラフェンシートの原子の厚さとそれらの高い表面積は、条件の変化に対する材料の感度を提供します。したがって、すべての原子が直接接触できるグラフェンの表面の特徴により、グラフェンは環境に敏感になります。したがって、他の材料と比較して、センサーアプリケーションの優れた候補です[、、 4、100、101]。グラフェンとその誘導体に関連する過去10年間の研究が分析され、グラフェンの生物医学的応用の分布を示す円グラフとともに図102に示されています。上記のグラフェンの特徴により、研究者は主にバイオセンサーの分野に焦点を合わせていると言えます。
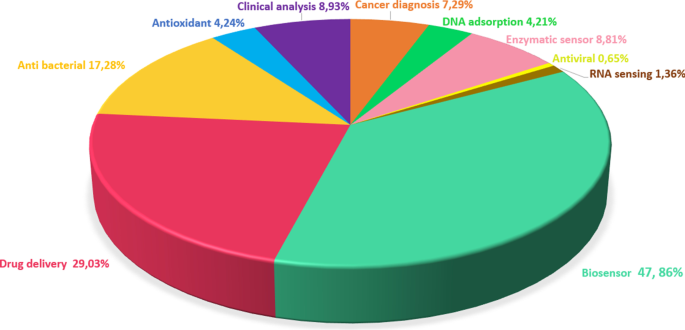
生物医学的応用におけるグラフェンの分布を示す円グラフ
最初のセクションで述べたように、いくつかのバイオセンサーは、グラフェンおよびグラフェン誘導体をMONと組み合わせることによって調製されます。レビューのこの部分では、グラフェンとその誘導体に基づくバイオセンサーに焦点を当てます。グラフェンベースのバイオセンサーの一般的な表現とメカニズムを図5に示します。ここでは、グラフェン表面の官能基と相互作用する分析物、およびこの相互作用に基づいて電気化学的、光学的、またはその他の出力を取得できます[96 、97、103]。たとえば、Mani etal。 [104]は、H 2 を高感度かつ選択的に検出するために、rGOナノリボン/ MWCNT /キトサンに基づく三元ナノバイオコンポジットを開発しました。 O 2 およびNO 2 − 。彼らは、コンタクトレンズ洗浄液と肉サンプルにおけるバイオセンサーの有益な特性を調査しました。彼らは、H 2 について O 2 、ナノバイオコンポジットベースのセンサーの感度は0.616 µAµM -1 でした cm −2 、検出限界は1 nm、線形範囲は0.001〜1625 µMですが、これらの値はNO 2 − 、0.643 µAµM -1 cm −2 、10 nm、および0.01〜1350 µM。したがって、彼らは、グラフェンベースのセンサーが医療用途や食品安全に効果的に使用できることを証明しました[104]。別のグラフェンベースのH 2 O 2 センサーはYinらによって準備されました。 [105]。彼らの研究では、Yinらは、Ni 3 で装飾された導電性の3次元(3D)グラフェンエアロゲル(GA)を合成しました。 水熱法を使用したNNP。それらの特性評価の結果、彼らはNi 3 彼らが得たN / GA複合材料は、H 2 だけでなく適用できます。 O 2 だけでなく、グルコース測定用。彼らは、Ni 3 N / GAベースの電極、H 2 の測定 O 2 、5 µM〜75.13 mMの検出範囲、101.9 µAmM -1 の感度として、高い電気化学的性能を示しました。 cm −2 、および1.80 µMの低い検出限界。さらに、グルコース測定では、設計された電極の検出範囲が0.1〜7645.3 µM、検出限界が0.04 µM、感度が905.6 µA mM -1 であることを強調しました。 cm −2 [105]。
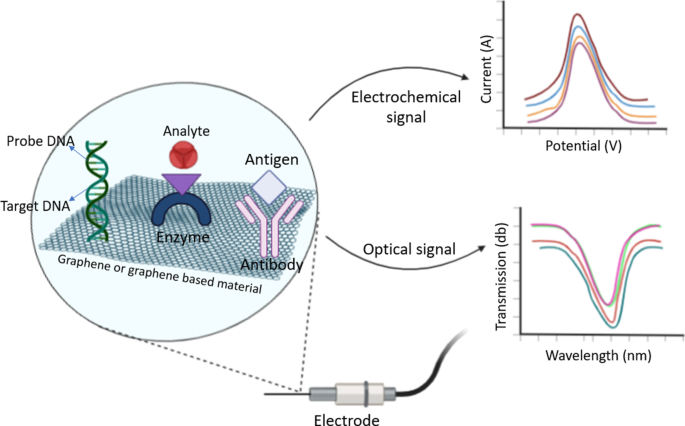
グラフェンベースのバイオセンサーとそのメカニズムの表現
最近、グルコースを実用的に検出するためのグラフェンベースのバイオセンサーに強い関心が寄せられていると言えます。表3.たとえば、Đurđićetal。 [106] Bi 2 に基づく使い捨てバイオセンサーの合成に成功 O 3 -共沈による装飾されたGNR。特性評価の結果、得られたセンサーの検出限界は0.07 mM、線形範囲は0.28〜1.70 mM、感度は64.81μA/ mMcm 2 であることが証明されました。 。したがって、彼らは、グラフェンベースのセンサーが、再現性があり安定した血清および尿サンプル中のグルコースを検出できることを提案しました[106]。同じ年に、NiCo 2 を使用した3D窒素ドープ多孔質グラフェンヒドロゲル(NHGH)のシングルポット水熱合成により、有用なグルコースバイオセンサーの設計に成功しました。 O 4 ナノフラワー(NHGH / NiCo 2 O 4 )Luとチームによる。彼らは、入手したナノコンポジットでGCEを変更し、グルコースを測定する際の変更された電極の電気化学的性能を評価しました。まず、スキャンレートが50 mV s -1 の0.1MNaOH溶液でCVを受け取りました。 、電気化学的触媒性能を調べるため。彼らは、NHGH / GCEの酸化ピーク電流が、裸のGCEの弱い陽極ピーク電流よりも0.5V増加していると報告しました。さらに、彼らの研究では、レドックスピークペアが見えることを観察しました。これは、NHGH / NiCo 2 の電気化学的活性を示しています。 O 4 / GCEは他の電極と比較して最も高いです。彼らは、この改善をグラフェンの拡張された表面積に起因すると考えました、 良好な導電率、およびCoとNiの酸化還元反応。さらに、5.0mMのグルコース添加における電極の電気化学的触媒性能を示しました。彼らはNHGH / NiCo 2 を解釈しました O 4 / GCEは、0.5 Vで最大のピーク電流を示します。これは、NiCo 2 の二重効果により、グルコース酸化が他の電極よりも優れた触媒作用を発揮する可能性があることを明確に示しています。 O 4 とNHGH。彼らはまた、ピーク電流がグルコース濃度およびNHGH / NiCo 2 の増加とともに直線的に増加したことを報告しました。 O 4 ベースのグルコースセンサーは、ピーク電流とグルコース濃度の間に、それぞれ5μM〜2.6mMと2.6mM〜10.9mMの範囲で幅広い線形関係を示しました。また、彼らはNHGH / NiCo 2 O 4 / GCEは高感度です(2072μAmM -1 cm − 2 )および低い検出限界(0.39μM)。その結果、彼らは実際の血液サンプル中のグルコースの正確な測定に使用することを提案しました[107]。
<図>表3に示すように、グラフェンとその誘導体は、その優れた特性により、バイオセンサーアプリケーションに不可欠な構成要素になっています。表3で最近行われた研究を考慮すると、グラフェンとその誘導体が、バイオセンサーの感度と再現性を改善するためにMONとのハイブリッドナノ構造で使用されていることは注目に値します。さらに、MON /グラフェンの相乗効果を評価して、多機能バイオセンサーを取得し、高い電極触媒活性を実現する必要があります。さらに、グラフェンはCNTなどの他のナノカーボンと簡単に組み合わせることができます。したがって、酵素バイオセンサーを作成するための豊富なエッジ密度と非常に有益なエッジ欠陥を得ることができます。
カーボンナノチューブベースのバイオセンサー
1991年に飯島によって発見されたCNTは、グラフェン層が円柱状に形成されたものと考えることができます。 CNTは、一般に、単層カーボンナノチューブ(SWCNT)図6aとMWCNT図6bの2つのタイプに分類できます[125]。直径とラッピング角度は、キラリティーと(n、m)インデックスによってCNTの物理的特徴を決定します[126,127,128]。 (n、m)インデックスによると、CNTは金属または半導体の挙動を示す可能性があり[129,130,131,132]、キラリティーに応じて、SWCNTは次の3つの方法で分類できます。(1) m = n はアームチェアナノチューブです図6c、(2) n > m m の場合 =0はキラルナノチューブ図6d、 m =0はジグザグナノチューブ図6eです。 CNTは、その性質上、半導体の振る舞いを示しますが、特定の( n 、 m )SWNT、(2 n + m )/ 3は整数で、CNTは金属製になります。したがって、すべてのアームチェアナノチューブは金属であると主張することができます[130]。したがって、製造中にキラリティーを制御する能力は、CNTの電子的特徴を制御することを意味し、バイオセンサーの用途に大きな利点をもたらします。近年、CNTを合成するためにいくつかの異なる方法が提案されてきた。ただし、3つの主要な合成技術(アーク放電、レーザーアブレーション、およびCNT製造用のCVD [133]があります。アーク放電およびレーザーアブレーション法と比較して、CVDは、 CNT [133、134]。
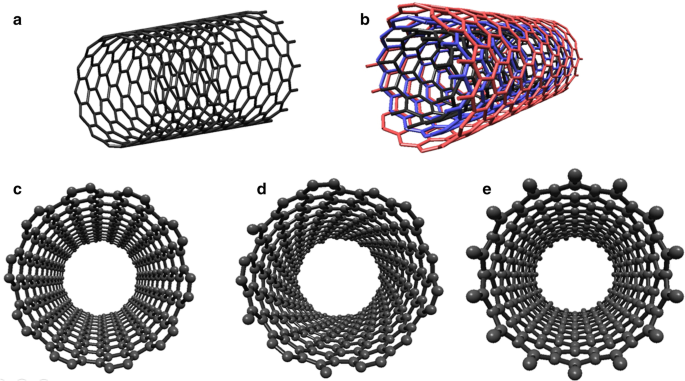
a のCNTの分類 SWCNT、 b MWCNT; SWCNTの3つの典型的なタイプの概略図 c アームチェア(10、10)、 d キラル(13、6)、および e ジグザグ(14、0)
CNTの端部および側壁は、事実上任意の所望の化学種を添加することによって容易に変更することができる。 CNTは、感度が高いため、ナノスケールセンサーの優れたトランスデューサーになります。さらに、CNTは、ターゲットの認識時に生成される電気信号を送信するための非常に有利な特性を備えているため、酵素ベースのバイオセンサーの最終的な開発に不可欠な役割を果たします[135]。さらに、サイズが小さく、応答時間が速く、電気化学的特性が優れているCNTは、イオン、代謝物、およびタンパク質バイオマーカーを備えた他のほとんどの電極と同等またはそれ以上です[136]。 CNTは、長さと直径の比率が広い独自の管状ナノ構造の結果として、優れた電気化学的安定性、優れた機械的柔軟性、迅速な電子輸送、および独自の熱伝導率により、電気化学的バイオセンサーを適用する上で望ましい材料です[137、133]。 CNTは、生体適合性を確保し、有機化合物または金属NPと結合した後、電気的および機械的機能を改善するために、組織工学および薬物送達システムでも広く使用されています。 [138]。 2010年から2020年までのCNTに関する研究が分析され、CNTの生物医学的応用の分布を示す円グラフとして図7に示されています。
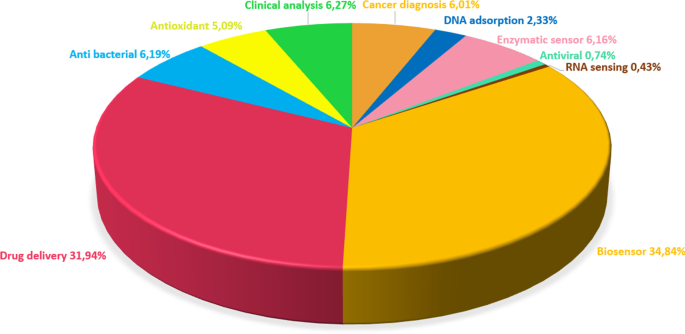
生物医学アプリケーションにおけるCNTの分布を示す円グラフ
CNTは、グラフェンやその誘導体と同様に、MONとハイブリダイズすることにより、より高い感度と選択性を備えたバイオセンサーの開発に重要な貢献をしています。研究者たちは最近、CNTのユニークな特性と金属NPの優れた特性を組み合わせることができる新しいナノバイオセンサーの製造と特性評価に焦点を合わせています。たとえば、Rahman etal。 [139] Fe 3 を設計しました O 4 -環境保護用途向けの装飾されたCNTベースの3-メトキシフェニル(3-MP)バイオセンサー。 Fe 3 O 4 / CNTsナノコンポジットは、湿式化学法で合成され、GCE表面に薄層としてコーティングされています。次に、彼らはI-V特性評価によって修飾電極の電気化学的性能を評価し、Fe 3 O 4 / CNTベースの電極は、広い検出範囲(90.0 pM〜90.0 mM)、低い検出限界(1.0 pM)、および高い感度(9×10 -4 )を示しました。 μAμM -1 cm −2 )危険なフェノールの検出[139]。同様に、環境保護のために、MWCNT / TiO 2 /キトサンベースのバイオセンサーは、Fotouhiらによって開発されました。 [140]化学および製薬業界から環境に放出されたジヒドロキシベンゼン異性体を検出する。 Fotouhi etal。彼らは、ハイドロキノン(HQ)、カテコール(CC)、およびレゾルシノール(RS)の同時測定を実行し、MWCNTベースのセンサーによって実際の水サンプルに汚染を引き起こしたと報告しました。さらに、彼らは検出限界を示しました( S / N =3)HQ、CC、RSの場合、0.06μmoldm -3 、0.07μmoldm -3 、および0.52μmoldm -3 、線形応答範囲は0.4〜276.0μmol d m -3 、0.4〜159.0μmol d m -3 、および3.0–657μmol d m -3 、それぞれ[140]。
環境保護に加えて、臨床応用のためのCNTのバイオセンサー設計は、最近非常に興味深いものになりました。 [141]は、ヘリウムアーク放電法により、精製されたSWCNTとNiOで装飾されたSWCNTの2つの層を含むバッキーペーパーを入手しました。その後、電気化学的性能を評価するための分析の結果、グルコースバイオセンサーの線形範囲が広く(0.1〜9 mM)、感度が高い(2701μAmM -1 )ことが示されました。 cm −2 )、および高速応答時間(<2.5秒)[141]。 BarthwalとSingh [142]は、彼らの研究で尿素を検出するためにZnO / MWCNTsナノコンポジットバイオセンサーを設計しました。彼らは、ZnO / MWCNTsベースのセンサーがZnOおよびMWCNTsベースのセンサーと比較して最も高い検出特性を持っていることを示しました。また、2%のMWCNTを含むナノコンポジットの感度は10秒未満であり、検出限界は10ppmであることを強調しました[142]。同じ年に、Guan等。 DAとUAを同時に高感度で検出するための電気化学的バイオセンサーとして、CNTベースのハイブリッドナノコンポジットの開発に成功しました。彼らの研究では、彼らは最も広範囲(Δ E p =144 mV)、CNTベースのナノハイブリッドで修飾された電極で最高の酸化電流が観察されました。さらに、彼らは、差動パルスボルタンメトリー(DPV)を介してナノハイブリッド修飾GCEでDAとUAの同時検出を調査しました。彼らは、ナノハイブリッド/ GCEの陽極ピーク電流応答が、DA濃度の増加により直線的に増加することを示しました。また、UA濃度についても同様の観察結果が得られました。彼らは、両方の対象化合物の濃度範囲が2〜150μMであることを強調しました。その結果、DAとUAの検出値の限界はそれぞれ0.37μMと0.61μMであると報告されました[143]。
<図>MONおよびグラフェンおよびグラフェン誘導体とハイブリダイズし、それらの特性を改善することにより、さまざまなアプリケーション分野でCNTベースのバイオセンサーの効率を高める研究は非常に興味深い表4。CNTベースの電気化学で設計されたナノハイブリッド構造のより高い電気化学活性とより高い導電率センサーは、CNTの固有の特性の結果と見なすことができます。一方、バイオセンサーアプリケーションでのCNTの使用を制限する特徴の1つは、ほとんどの溶媒に溶解しないことです。また、生体適合性が低く、場合によっては毒性があります。これらの問題を克服するために、CNTの表面とエンドキャップの異なる官能基をMONと組み合わせ、表面修飾を適用することが解決策と見なすことができます。
さらに、CNTとグラフェンおよびその誘導体との統合により、強力な結合相互作用により、生体分子に対してより活性な部位を作成することが可能です。 CNT /グラフェンハイブリッド構造のもう1つの利点は、電子移動速度が速いため、バイオセンサーがより短い時間で応答できることです。したがって、将来開発される次世代のバイオセンサーでは、CNTとMONまたはグラフェンやその誘導体などの他のナノカーボンとの二重効果の恩恵を受けて、高感度と選択性、同時ターゲット生体分子検出を達成することは避けられないようです。
結論と展望
バイオセンサーと生体電極は、環境モニタリング、食品安全、医療繊維産業、創薬と分析、臨床および非臨床アプリケーションで重要な役割を果たします。最近のCOVID-19のパンデミックにより、感染症との闘いを制御するために、応答性が速く、再利用可能で、安価で、選択性の高いバイオセンサーが不可欠になりました。バイオセンサーの設計では、トランスデューサーのコンポーネントに使用され、トランスデューサーの表面を機能化するために使用される材料は、バイオセンサーから得られる前述の特性を備えた結果に明確な影響を及ぼします。このフレーム内で、これらのデバイスの特性を改善するために、ナノ材料が広く使用されており、それらの拡張された表面積、あらゆるタイプの分析物の使用のための表面修飾に適応する能力、およびそのような並外れたナノサイズ依存の特性がそれらをもたらした理想的なバイオセンサーの製造において、前例のない一歩を踏み出しました。
この動機で、この論文は、MON、グラフェン、およびCNTの併用によって作成されたハイブリッドナノシステムの最近の開発の概要を示します。これらのナノ構造の助けを借りて生体分子を検出するための改善された感度と選択性を備えたバイオセンサーを作成するために多くの努力がなされてきた。明らかに、これらの材料のそれぞれの独特の特徴とは別に、それらのハイブリッド設計の複数の効果は、より高性能のバイオセンサーを得るための重要なポイントです。これらのナノ構造を組み合わせてハイブリッド設計を作成すると、バイオセンサーの電極触媒活性とその電子移動速度が向上し、より多くの活性部位で2つ以上の生体分子を同時に検出できるようになります。また、安定性、長い貯蔵寿命、再現性、広い測定範囲、次世代バイオセンサーアプリケーションの高速応答時間など、理想的なバイオセンサーに期待される他の望ましい機能も満たしています。ただし、これら3つのトレンドのナノ材料を組み合わせるには、凝集傾向の制御、細胞毒性、適切な濃度の選択、純度を向上させるための条件の広範な最適化などの説得力のある要因があり、これらの材料は互いによりよく統合されます。したがって、ナノマテリアルとその複合構造の準備のために行われるべき改善の余地はまだあります。さらに、医療用途のバイオセンサーに大きな影響を与える分析物のオンサイト診断では、費用効果の高い方法で迅速かつ信頼性の高い結果を得ることが重要です。この目的のために、バイオセンサーで使用されるナノ材料は、特に初期段階で非常に微量の濃度を持ついくつかの疾患のバイオマーカーについて、より繊細な感知で診断を容易にするように変更される可能性があります。このような機能を獲得して改善するには、グラフェン、CNT、およびMONを、最小限の触媒不純物、高い結晶化度、および費用効果の高い方法で大量に製造する必要があります。それらはまた、より良い電子輸送特性を調整するために、それらの状態密度および結合の構造のために設計されるべきである。このレビューでは、正確な「将来のバイオセンサー」メカニズムの開発に役立つナノ構造の組み合わせが提案され、感度、優れた選択性、検出下限、多機能特性を備えたリアルタイムセンシングとしての期待がまとめられました。
データと資料の可用性
該当なし。
略語
- 1D:
-
一次元
- 3D:
-
三次元
- CD:
-
シクロデキストリン
- CVD:
-
化学蒸着
- CV:
-
サイクリックボルタモグラム
- DA:
-
ドーパミン
- DNA:
-
デオキシリボ核酸
- DPV:
-
微分パルスボルタンメトリー
- FET:
-
電界効果トランジスタ
- GCE:
-
ガラス状炭素電極
- GelMA:
-
ゼラチンメタクリロイル
- GNP:
-
グラフェンナノプレートレット
- GNR:
-
グラフェンナノリボン
- GO:
-
酸化グラフェン
- GQD:
-
グラフェン量子ドット
- LOD:
-
検出限界
- MIP:
-
分子インプリントポリマー
- MOF:
-
金属有機フレームワーク
- MO:
-
金属酸化物
- MWCNT:
-
多層カーボンナノチューブ
- NHGH:
-
窒素ドープ多孔質グラフェンヒドロゲル
- NP:
-
ナノ粒子
- NR:
-
ナノロッド
- NSs:
-
ナノスフェア
- NW:
-
ナノワイヤー
- PANI:
-
ポリアニリン
- PDADMAC:
-
ポリ(ジアリルジメチルアンモニウムクロリド)
- PDPA:
-
ポリジフェニルアミン
- PECVD:
-
プラズマ化学気相成長法
- PEDOT:
-
ポリ(3,4-エチレンジオキシチオフェン)
- PG:
-
純粋なグラフェン
- PPy:
-
ポリピロール
- PTA:
-
リンタングステン酸
- PVA:
-
ポリビニルアルコール
- RF:
-
無線周波数
- rGO:
-
還元型酸化グラフェン
- SERS:
-
表面増強ラマン散乱
- SWCNT:
-
単層カーボンナノチューブ
- UA:
-
尿酸
- XO:
-
キサンチンオキシダーゼ
ナノマテリアル
- 高融点金属レニウムの概要
- チタン酸塩ナノチューブで装飾された酸化グラフェンナノコンポジット:調製、難燃性、および光分解
- invitroおよびinvivoでのグラフェンおよび酸化グラフェンのバイオセーフティおよび抗菌能力
- 酸化グラフェンハイブリダイズしたnHAC / PLGA足場はMC3T3-E1細胞の増殖を促進します
- スーパーキャパシター用途の電極としてのグラフェン/ WO3およびグラフェン/ CeOx構造の評価
- グラフェン上の金属ナノ粒子における電磁界の再分布
- ミルストーン剥離:大型の数層酸化グラフェンの真のせん断剥離
- 初心者のための概要:金属加工とは何ですか?
- 板金プレス金型の概要
- スポット溶接板金の概要
- 薄板金の概要



