フェロマンガンの生産
フェロマンガンの製造
フェロマンガン(Fe-Mn)は、鉄鋼製造の脱酸剤として使用される重要な添加剤です。鉄(Fe)とマンガン(Mn)のマスター合金で、最小Mn含有量は65%、最大Mn含有量は95%です。これは、Mn(MnO2)と鉄(Fe2O3)の酸化物の混合物を、通常はコークスまたは石炭として炭素(C)と加熱することによって生成されます。
以前に可能であったよりもかなり高いMn含有量の高炉(BF)内のFe-Mnは、1872年にLambertVonPantzによって最初に製造されました。生成されたFe-Mnは、以前に得られた12%ではなく、37%のMnでした。 Mn含有量が40%を超える冶金グレードのMn鉱石は、通常、鉄のパイロ冶金プロセスと非常によく似たパイロ冶金プロセスによって、適切な金属フェロアロイの形に加工されます。その製造工程では、Mn鉱石、還元剤(Cの一種)およびフラックス(CaO)の混合物が1200℃より高い温度で製錬され、還元反応と合金形成が可能になります。標準グレードのFe-Mnは、BFまたは電気水中アーク炉(SAF)のいずれかで製造できます。
ただし、電気SAFプロセスは、スラグをさらにSi-Mnおよび精製Fe-Mnに処理できるという点で、BFプロセスよりもはるかに柔軟性があります。プロセスの選択は、電力とコークスの相対価格にも依存します。三相SAFでは、電極は電荷材料に埋め込まれます。原料は加熱され、高温の一酸化炭素(CO)ガスによって事前に還元されたMn酸化物が、炉のより深い反応ゾーンを形成します。発熱反応は、必要な熱に有利に寄与します。 HC Fe-Mnの効率的な生産は、炉の上部領域で発生する予備還元の程度に依存します。
多くのグループに分けられるFe-Mnのいくつかの等級があります。 3つの主要なグループは、高C Fe-Mn、中C Fe-Mn、および低CFe-Mnです。高CFe-MnはBFおよびSAFで製造できます。 SAFでは、2つの異なる慣行、すなわち(i)高Mnスラグ慣行と(ii)廃棄スラグ慣行によって作成されます。中程度のCFe-Mnは、脱炭酸プロセスによって、またはシリコマンガン(Si-Mn)合金中のシリコン(Si)とMn鉱石との間のレドックス(還元-酸化)反応によって生成できます。低CFe-Mnは、Mn鉱石と低CSi-Mnの反応によって生成されます。
Fe-Mnの生産に必要な原材料
Fe-Mnの生産に必要な原材料は、Mn鉱石、コークス、および石灰石、ドロマイト、珪岩などのフラックスです。原材料は屋外に保管されることが多いため、Mn鉱石に化学的に結合した水を含む含水量は、最大10%と高くなる可能性があります。
Mn鉱石は、Fe-Mnの製造に使用される重要な原料です。 Mn鉱石は、Mnの含有量に応じて分類されます。一般に、35%以上のMnを含む鉱石はMn鉱石として分類されます。通常、Mn含有量に基づいて3つのグレードのMn鉱石があります。これらは、(i)Mn含有量が44%から48%の高品位Mn鉱石、(ii)Mn含有量が35%から44%の中級Mn鉱石、およびMn含有量が25%から35の低品位Mn鉱石です。 %。
Mn含有量が10%から35%の鉱石は鉄質Mn鉱石と呼ばれ、Mn含有量が5%から10%の鉱石はマンガン鉄鉱石と呼ばれます。 Mnが5%未満で、残りが主にFeである鉱石は、鉄鉱石に分類されます。
SAFでのFe-Mnの生成に必要なコークスは、鉄BFで通常使用されるコークスよりも反応性が高くなります。 SAFで使用した場合の反応性の高いコークスは、安定した炉の運転をもたらし、優れた生産性をもたらします。
BFでの高CFe-Mnの生成
高炉は、第二次世界大戦の終わりまで、Fe-Mnの生産のために先進国で広く使用されていました。通常、統合された製鉄所は、高CFe-Mnの生産のためにそれらのより小さなBFを運命づけられました。 Mn含有量が28%以上の低品位Mn鉱石は、BFでの製錬に使用できます。
高CFe-Mnは、BFで溶銑(HM)を製造するプロセスと同様のプロセスでBFで製造されます。ただし、2つのプロセスの間にはいくつかの重要な違いがあります。酸化鉄は、次の反応に従って、炉のシャフト領域でCOによって還元されます。
3Fe2O3 + CO =2Fe3O4 + CO2
Fe3O4 + CO =3FeO + CO2
FeO + CO =Fe + CO2
一方、BFのボッシュおよびハース領域では、次の反応が原因で温度が高くなるため、Mn酸化物は固体Cによって還元されます。
Mn3O4 + 4C =3Mn + 4CO
MnO + C =Mn + CO
したがって、BFでのFe-Mnの生産には、BFでのHM生産に必要な量よりも大量のコークスが必要です。ブラストの予熱と酸素(O2)濃縮は、通常、コークスの必要量を減らすために使用されます。チャージにドロマイトまたは石灰石を加えると、還元のためにMnOの活性が高まります。 Mnの回収率を高めるには、少量のスラグ、基本的なスラグ、および高い爆風温度が必要です。注意深い制御とBFのシャフトでのより均一なチャージミックスにより、90%を超えるMnの回収率と1530 kg/tのコークス率が達成されました。
BFのトップガスは、Fe-Mnを伴う過剰な微粉を生成します。 SAFは、コークス率が低く、耐火物の寿命が長く、熱風を必要とせず、Si-Mnフェロアロイの製造にMnOに富むスラグを再利用するため、BFに取って代わりました。
SAFでの高CFe-Mnの生成
BFで高CFe-Mnを製造する場合、製錬プロセスに必要な熱エネルギーは追加のコークスの燃焼によって供給されますが、SAFで高C Fe-Mnを製造する場合は、製錬の過程で必要なエネルギーは電力によって供給されます。 SAFの場合、新しい施設に必要な資本的支出も少なくなります。
高CFe-Mn生産のためのSAFの重要な設計パラメータは、(i)電極の直径と間隔、(ii)炉床の直径、(iii)るつぼの深さ、(iv)電圧範囲、および(v)MVAです。変圧器の容量。 Fe-Mnの生成における負荷の抵抗率が低いため、充電中の電極の十分な浸透を維持するために、電極間の低電圧が必要です。したがって、炉の適切な電力負荷を得るためには、より高い電流が必要です。したがって、C電極の電流容量内で動作するために、Fe-Mnを生成するSAFの電極の直径は、他のフェロアロイを生成するSAFよりも大きくなります。電気エネルギーは、通常はセルフベーキングタイプの3つのカーボン電極を介して製錬反応に供給されます。るつぼは、耐火レンガで裏打ちされた鋼製シェルとCブロックの内張りで構成されています。炉床はBFに似ていますが、Cの裏地が厚くなっています。
SAFのシャフトの高さは、鉄BFのシャフトの高さよりもはるかに低く、シャフト内の負荷の滞留時間はそれに比例して短くなります。通常、酸化物の金属への還元は、鉄BFでの6〜8時間と比較して、数時間で実行されます。 Fe-MnのSAF製造に反応性コークスを使用すると、酸化鉄を金属に還元し、Mnの高次酸化物をMnOに還元し、少量のMnOを鉄に溶解したMnに還元することができます。負荷は電極の下の混合スラグコークス層に到達します。 BFの高さに比べてシャフトの高さが低いということは、Fe-MnのSAF製錬では、鉄BF製錬よりもコークスの強度がそれほど重要ではないことも意味します。
SAFを生成するFe-Mnは、オープントップまたはクローズドトップのいずれかを持つことができます。オープントップ炉には、炉シェルの上部から少なくとも1メートル上にヒューム収集フードがあります。可動式のパネルまたはスクリーンは、炉とフードの間の空き領域を減らし、排出物の捕捉効率を向上させるために使用されることがあります。炉装入物を通って上昇するCOガスは、装入物表面と捕捉フードの間の領域で燃焼します。これにより、封じ込めシステムが処理する必要のあるガスの量が大幅に増加します。さらに、活発な開放燃焼プロセスは、より細かい材料を装入物に同伴します。ファブリックバッグフィルターは通常、オープントップ炉からの排出を制御するために使用されます。
クローズドトップSAF(図1)には通常、水冷式の鋼製カバーがあり、炉のシェルにぴったりとはまります。クローズドトップ炉の目的は、炉ガスへの空気の浸透を減らし、ガスの燃焼を減らすことです。これにより、収集と処理が必要なガスの量が削減されます。カバーには、帯電材料と電極が通過するための穴があります。これらのフード開口部を部分的に閉じるクローズドトップファーネスは、「ミックスシール」または「セミクローズドファーネス」と呼ばれます。このタイプの密閉型炉は空気の浸透を大幅に低減しますが、炉のカバーの下で燃焼が発生します。電極の周りにメカニカルシールがあり、外縁の周りにシールコンパウンドがあるクローズドトップSAFは、「シール」または「完全クローズ」と呼ばれます。この炉は、空気の浸透と覆面燃焼があったとしてもほとんどありません。カバーから炉への水漏れは最小限に抑える必要があります。これは、過剰なガス生成と不安定な炉の動作につながるためです。プロセスガスの放出が非常に変動しやすい製品は、安全上の理由から、通常、クローズトップ炉では製造されません。囲いの程度が増すにつれて、フードシステムによって捕捉されるために生成されるガスが少なくなり、炉ガス中のCO濃度が増加します。ウェットスクラバーは、クローズドトップSAFからの排出を制御するために使用されます。スクラブされた高CO含有ガスは、プラント内で燃料またはフレアとして使用できます。
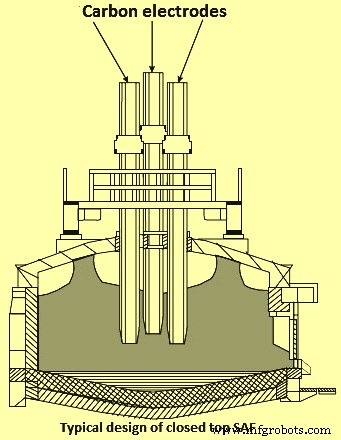
図1クローズドトップ水中アーク炉の典型的な設計
クローズドトップSAFにより、より低い資本コストでより優れたヒューム制御が可能になり、必要なエネルギーが削減されます。一方、クローズドトップ炉で使用される鉱石の要件は、より制限されています。遊離O2は10%未満で、砕けにくい鉱石でなければなりません。そうしないと、クラストが形成されて爆発が発生する可能性があります。クローズドトップSAFに適した適切な原料を選択し、原料に最適な物質収支を適用し、製錬条件を強化することにより、Fe-Mnの生産の経済的パフォーマンスが向上します。これらの結果、原材料の消費量が削減され、比エネルギー消費量が削減され、炉の操作が良好になり、合金の品質が向上し、製造コストが削減されます。
1977年に南アフリカのMeyertonFe-Mnプラントで発掘された冷凍炉を広範囲に研究することにより、SAFでの高C Fe-Mnの生成中の負荷物質の反応と変化がよりよく理解されました。これらの研究は、かなりの量を提供しました。負担材料の変化と反応ゾーンの性質の理解。発掘調査により、炉の内部は9つのゾーンに分割できることが明らかになり、そのうち3つが還元および冶金処理にとって最も重要であると思われます。これらは、(i)各電極の周りの急速に下降する負荷の円錐、(ii)電極の真下のコークス床、および(iii)コークス床の下の混合コークススラグ層です。掘削の主な発見は、1300℃から1600℃の範囲の温度の間で、3つの主要な段階で還元が起こったことでした。状態)COガスと主にCaOとSiO2からなる一次スラグの形成、(ii)MnOのスラグへの溶解と鉱石塊の表面での還元による金属ビーズの形成、(iii)接触した塊Cによる還元溶融スラグを使用します。
MnOとFeOの炭素熱還元は吸熱反応ですが、次の反応で示されるように、MnO還元はFeO還元よりも多くの熱を必要とします。
MnO(s)+ C(s)=Mn(l)+ CO(g)デルタH =276 KJ(1200℃)
FeO(l)+ C(s)=Fe(s)+ CO(g)デルタH =149 KJ(1200℃)
MnOの削減には、より高い最低温度も必要です。 MnOの還元温度は1400℃、FeOの還元温度は720℃です。実際には、合金の形成によりMnとFeの熱力学的活性は1未満であるため、実際の最低温度はわずかに低くなります。したがって、Fe-Mnの製造では、鉄鉱石をFeに還元し、より高いMn酸化物をMnOに還元し、MnOの一部を金属Feに溶解したMnに還元することが熱力学的に可能です(感知可能な熱を使用し、スラグコークスゾーンで生成されたガスの容量を低減するシャフト内の条件下での固体状態での低熱力学的活性で)。これにより、残りのMnOの減少のみが、高温混合スラグ-コークスゾーンで発生します。 Fe酸化物の金属への還元速度とMnの高級酸化物のMnOへの還元は、約1300度までの温度でSAFのシャフトに存在する条件下で、Boudouard反応(C + CO2 =2CO)によって強力に制御されます。 C. MnOの大部分が還元される温度(1300℃を超える)では、初期値に関係なく、コークスの反応性がほぼ同様の値に収束します。
最高のMn酸化物(MnO2)の還元は、4つのステップで行われます。 MnO2からMn2O3(4MnO2 =2Mn2O3 + O2)への最初の還元ステップは450°Cから500°Cを超える温度で到達し、2番目のステップMn2O3からMn3O4(6Mn2O3 =4Mn3O4 + O2)は900°Cを超える温度で到達します。 950℃までであり、還元剤なしで、熱分解によってのみ両方を実現することができます。熱分解の両方のステップは、Mn酸化物の安定性の範囲を示しています。 Mn3O4からMnO(Mn3O4 + CO =3 MnO + CO2、およびMn3O4 + C =3 MnO + CO)への還元は、COガスまたは固体Cによってのみ可能です。大気圧での炭素によるMnOの還元は、温度でのみ実現可能です。 1410℃以上。完全な還元を達成するには、温度をさらに高くする必要があります。ここでの問題は、Mnの蒸気圧が高く、その結果として強い蒸発が発生することです。さまざまな還元ステップを伴うMn製造プロセスの場合、MnOは最初にスラグ相に溶解し、そこからMnが固体Cによって還元され、金属相に移動します。ここでは、スラグと合金の非理想的な解決策が非常に重要です。最新の熱力学的手法を使用して、物質収支に基づいて相とエネルギー収支を決定します。
SAFでのFe-Mnの生成に使用されるより反応性の高いコークスにより、Boudouard制御の反応をシャフトのより高い位置で完了できるため、顕熱をより効果的に利用し、炉の下部からのガスの容量を減らすことができます。 MnOからMnへの最終的な高熱需要の削減を、高温混合スラグ-コークスゾーンでの主要な反応にすることができます。逆に、反応性の低いコークスは、炉内の還元条件が悪く、コークス床が大きくなる可能性があり、その結果、炉の制御が不十分になり、合金とスラグの組成が不安定になり、消費電力が高くなります。
製錬作業を成功させるための重要な考慮事項は、スラグの組成です。これは、炉の抵抗率、製錬温度、Mnの回収率、およびFe-Mn中のSiの量に明確な影響を与えるためです。所望のスラグ組成物を製造するために、鉱石の混合または流動試薬の添加がしばしば必要である。通常、SAFでのFe-Mnの生産には、2種類のスラグ慣行が使用されます。これらは、(i)高Mnスラグの慣行、および(ii)「廃棄スラグ」慣行としても知られる低Mnスラグの慣行です。
高Mnスラグの慣行は、高品位のMn鉱石が製錬され、Si-Mnも生産されるプラントで一般的に好まれます。このスラグのMn含有量は28%から40%の範囲です。スラグ中の他の化合物の典型的な%範囲は、(i)MgO -3%から8%、(ii)Al2O3 – 10%から30%、(iii)CaO –約15%、および(iv)SiO2 – 25%です。 28%まで。これらのスラグは一般的にSi-Mnの製造に使用されるため、Mnの全体的な回収率が向上します。スラグ中の望ましいMn濃度に応じて、ドロマイトや石灰石などの少量のフラックスも使用されます。
Mn鉱石の品質が非常に低い場合は、廃棄スラグの慣行に従います。 Mn鉱石の品質が低いため、Fe-Mn合金で目的のMn含有量を達成するには、高度なMn抽出が必要です。また、Mn鉱石にCaOやMgOなどの塩基性酸化物が含まれている場合、そのような鉱石を単独で製錬すると、当然、Mnスラグが少なくなります。この慣行からのスラグのMn含有量は一般に10%から20%の範囲であり、Fe-Mn合金中のMnの回収率は80%から90%の範囲です。スラグ中の他の化合物の典型的な%範囲は、(i)MgO -3%〜8%、(ii)Al2O3 – 4%〜10%、(iii)CaO –約35%、および(iv)SiO2 – 28%です。 32%まで。 Mn鉱石に含まれるCaOまたはMgOの量が少ない場合、炉の装入物はMn鉱石、コークス、および石灰石やドロマイトなどの塩基性フラックスで構成されます。必要な塩基性酸化物(CaOまたはMgO)がMn鉱石に含まれていると、より良い結果が得られます。チャージ中のドロマイトまたは石灰石の煆焼に必要な追加のエネルギーと、スラグから抽出されるMnの量が多いため、高Mnスラグの練習に必要な電力よりも、廃棄スラグの練習に必要な電力が高くなり、高Mnプラクティスよりもオフガス。
中程度のCFe-Mnの生産
中程度のCFe-Mnは1%から1.5%のCを含み、75%から85%の範囲のMn含有量を持っています。中程度のCFe-Mnは、高CのFe-MnをO2で精製するか、Si-Mn中のSiを使用して鉱石またはスラグとして追加される追加のMnOを削減する珪熱ルートによって生成できます。
高CFe-MnのO2による精製 –このプロセスは、マンガン酸素精製(MOR)プロセスとも呼ばれ、UnionCarbideが特許を取得しています。このプロセスでは、高C Fe-Mnは、転炉(BOF)での製鋼プロセスで行われるのと同様の方法で脱炭されます。ただし、Fe-Mnの精製の場合にはいくつかの明確な違いがあります。これらの違いは、(i)製鋼に必要な1650℃と比較して1750℃の最終温度が必要、(ii)耐火物へのより厳しい攻撃、(iii)最終合金の鋳造が困難、(iv)より高い蒸気圧です。 Mnの量、および(v)オフガスのより高い体積と温度。
MORプロセスでは、O2が溶融した高C Fe-Mnに吹き込まれ、温度がタッピング値の1300℃から1750℃に上昇します。必要な熱は、MnからMn酸化物への酸化、およびCからCO。ブロープロセスの初期段階では、O2の大部分はMnの酸化によって消費され、溶融物の温度は1300℃から1550℃に上昇します。その後、Cは急速に酸化され、温度は1650℃。この温度を超えると、Cの除去速度が低下し、Mnが再び酸化されます。プロセスは1750℃で停止します。これは1.3%のC含有量に相当します。 C含有量をさらに減らすと、Mnの損失が許容できないほど高くなります。 MORプロセスでは、Mnの回収率は約80%であり、Mnの分布は(i)MC Fe-Mn合金80%、(ii)気化によって形成されたヒューム13%、(iii)によって形成されたスラグとして分解できます。 Mnの酸化5%、および(iv)その他の損失、飛沫など2%。
このプロセスが正常に機能するかどうかは、ブロー容器とO2ランスの設計、および操作手順に細心の注意を払う必要があります。 MORプロセスには、エネルギー消費量の削減、設備投資の削減、生産コストの削減、柔軟性の向上など、珪熱プロセスに比べて多くの利点があります。このプロセスの主な欠点は、C含有量を1.3%未満に減らすことができないため、その使用が中程度のCFe-Mnの生産に限定されることです。
シリコンサーミックルート –中程度のC Fe-Mnを製造するための珪熱ルートでは、高品位のスラグまたはMn鉱石と石灰(CaO)を含むメルトを16%から30%の範囲でSiを含むSi-Mnと接触させます。合金中のSiは、プロセスで還元剤として機能し、反応Si + 2MnO =SiO2+2Mnに従って溶融物中のMn酸化物を還元します。石灰の目的は、溶融物中のSiO2の活性を低下させ、上記の反応を可能な限り右側に強制することです。スラグの塩基度比(CaO / SiO2)は、SiO2の活性を十分に低下させるために、1.4より大きくする必要があります。
Si-Mnでプロセスに入るCは完全に金属相のままであるため、製品に含まれています。したがって、1%のCを含む中程度のC Fe-Mnを生成するには、20%のSiを含むSi-Mnが必要です。珪熱還元によって生成される熱は、プロセスを維持するのに十分ではありません。したがって、それは通常、電気アーク炉(EAF)で実行されます。このEAFは、マグネサイトレンガで裏打ちされており、非常に塩基性の高いスラグに対してかなり耐性があります。 EAFを傾けて、スラグを金属から分離することができます。
珪熱還元プロセスは、高C Fe-Mnの脱炭よりもエネルギー集約的ですが、最終的なC含有量が最初のSi-MnのC含有量によってのみ制限されるという利点があります。したがって、珪熱プロセスを使用して、低CのFe-Mnおよび工業用Mn金属を製造できます。
低CFe-Mnの生産
低CFe-Mnには、76%から92%の範囲のMnと0.5%から0.75の範囲のCが含まれています。低CFe-Mnの生成は、Mnの非常に高い損失なしに、高CFe-Mnの脱炭によっては不可能です。したがって、それは珪熱還元プロセスでできていなければなりません。このプロセスは、中程度のCFe-Mnの珪熱生成で使用されるプロセスと似ています。高純度の鉱石が使用されており、特にFeとPを含む鉱石は避けてください。高品位鉱石として製造された人工Mn鉱石は、不純物レベルが低く、すべてのMnがMnOとして存在するため、特に適しています。したがって、Mnの高級酸化物の還元は不要です。 Mn – 85%〜92%、C –約0.1%、Si約1%、マンガン回収率75%の低C Fe-Mnフェロマンガンの1トンあたりの典型的な消費量は、Mn鉱石–1250kgから1350 kg、Si-Mn(32%〜33%Siを含む)– 800 kg〜850 kg、クイックライム– 1000 kg〜1100 kg、電極– 10 kg〜12 kg、電力– 1800 kWh〜2500kWh。
>
製造プロセス



