多機能GaN / Feナノ粒子による内皮細胞の標的化
要約
この論文では、多機能ナノ粒子と生きている内皮細胞との相互作用について報告します。ナノ粒子は、酸化鉄と合金化された酸化亜鉛ナノ粒子上で窒化ガリウムを直接成長させた後、高温で水素流中でコアを分解することによって合成されました。透過型電子顕微鏡を使用して、ブタの大動脈内皮細胞が増殖培地に懸濁したGaNベースのナノ粒子を取り込むことを示します。ナノ粒子は小胞に沈着し、内皮細胞は細胞損傷の兆候を示しません。細胞内不活性ナノ粒子は、外部磁場における細胞の制御された輸送または設計された空間分布のためのガイド要素として使用されます。
背景
近年、ナノテクノロジーを用いて癌や関連疾患と闘うために多くの努力がなされてきました。最も一般的なアプローチの1つは、薬物担体として利用できるナノ粒子に基づいています[1、2]。ただし、このアプローチには、薬物吸着および共有結合のための認識リガンドでナノ粒子をコーティングする必要性に関連する制限、またはナノ粒子内に薬物をカプセル化する必要性によって引き起こされる制限があります。別の治療アプローチは、ナノ粒子を直接細胞治療に利用することです。つまり、病気を生物学的に治療する目的で部位を標的にすることです[3]。たとえば、磁性ナノ粒子がロードされた内皮細胞は、印加された磁場によって動脈損傷の部位に誘導される可能性があります。治療への応用に加えて、ナノ粒子を利用した細胞誘導は、invitroでの細胞分離や3次元構造の細胞コーティングにも役立ちます[4]。この論文では、内皮細胞がGaN / Feベースのナノ粒子を取り込むこと、およびこの現象を使用してinvitroで細胞の空間分布を制御できることを示します。
メソッド
ナノ粒子合成
GaNの薄層は、Fe 2 と合金化されたZnOナノ粒子上に成長しました。 O 3 2つのステップでHVPEによって。最初に、核形成層は600°Cで5分間堆積されました。その後、温度を800℃に上げ、この温度で10分間維持した。 2番目の温度レジームは、ZnOコアの分解とGaN結晶品質の改善に必要です。 GaNの成長は、以前に私たちのグループによって詳細に説明されています[5、6]。簡単に言うと、金属ガリウム、アンモニア(NH 3 )ガス、塩化水素(HCl)ガス、および水素(H 2 )キャリアガスとして。 GaNの成長過程では、HCl、NH 3 、およびH 2 流量はそれぞれ20、600、3500sccmでした。
細胞培養
ブタの大動脈内皮細胞は、メスで内皮細胞層を穏やかにこすることによって大動脈から単離された。細胞は、標準的なインキュベーターで37°C、5%CO 2 で培養されました。 EGM™-2(内皮増殖因子培地2、ロンザ)。細胞の分裂は、TrypLE™Select(1X)(Gibco®)を使用して実行されました。すべての実験で、継代3〜8の細胞を使用しました。他の場所で説明されているように、レンチウイルス形質導入によって細胞を緑色蛍光タンパク質(GFP)で標識しました[7]。
XTTアッセイ
XTTアッセイは、ナノ粒子を添加した新しい培地を追加したときに、培地交換の24時間後に開始されました。次に、培養培地を、2:1の比率でXTT試薬を含む新鮮なEGM2培地と交換した。 XTT試薬は、5mlのXTTに0.1mlの電子カップリング試薬が含まれています。 5%CO 2 を含む37°Cで4時間のインキュベーション後 、吸光度はParadigmマルチモードプレートリーダーで測定されました。
セルカウント
ナノ粒子の濃度が異なる細胞を2日間インキュベートした後、細胞を4%パラホルムアルデヒドで10分間固定し、PBSで洗浄し、DAPI(PBSで1:7500に希釈)で10分間染色しました。蛍光顕微鏡(Zeiss)に設置された高解像度カメラを使用して、6つの独立したウェルからランダムな視野を撮影しました。コンピューター支援ソフトウェアDotCountv1.2 [8]を使用して、すべてのウェルの相対的な細胞数を定量化し、コントロールと比較しました。
透過型電子顕微鏡
透過型電子顕微鏡法は、細胞をナノ粒子と1日間インキュベートした後に実施しました。細胞が50%のコンフルエンスに達した後、培地を50μg/ mlのGaN / Feナノ粒子を添加した培地と交換し、細胞をさらに24時間インキュベートしました。次に細胞をPBSで洗浄し、2%グルタルアルデヒドと2%ホルムアルデヒドで室温で2時間固定し、4°Cで一晩インキュベートしました。サンプルを0.1Mカコジル酸ナトリウムで洗浄し、1%OsO 4 で後固定しました。 0.1Mカコジル酸ナトリウム中で1時間。固定後、サンプルを段階的アセトンシリーズで脱水し、EPONに埋め込みました。重合は60℃で2日間行った。厚さ約50nmの薄片を、formvarでコーティングされた銅スロットグリッドに収集し、4%酢酸ウラニルとクエン酸鉛で染色しました。細胞切片は、200kVの加速電圧で透過型電子顕微鏡FEITecnai20を使用して詳細に調査されました。
結果と考察
多機能磁性ナノ粒子は、Fe 2 と合金化されたZnOの犠牲ナノ粒子上にGaN層を成長させることによって製造されています。 O 3 。水素化物気相エピタキシー(HVPE)を使用してGaN層を成長させた後、ZnOコアが分解されます。得られた化学的に安定なナノ粒子は、主に、堆積したGaN内の鉄原子の拡散、およびFe 2 > O 3 GaNシェルの内面に。これらのナノ粒子は、電子顕微鏡を使用して調査されました。 GaNのHVPE成長プロセス後、横方向のサイズが20〜100 nmの単結晶ナノ粒子は、空間的に分離されたままです(図1)。 GaN成長前後のナノ粒子のX線回折とラマン分光法による特性評価の結果(図1c、d)は、ZnOコアの分解とGaNナノ粒子の形成を示しています。エネルギー分散型X線分析(EDX)を使用して実行されたナノ粒子の化学分析により、GaN層の成長とZnOコアの分解が確認されます(図1e、f)。得られた材料は、最初のナノ粒子と比較して、比較的高い(約50%)濃度のFeを示すことに注意してください。
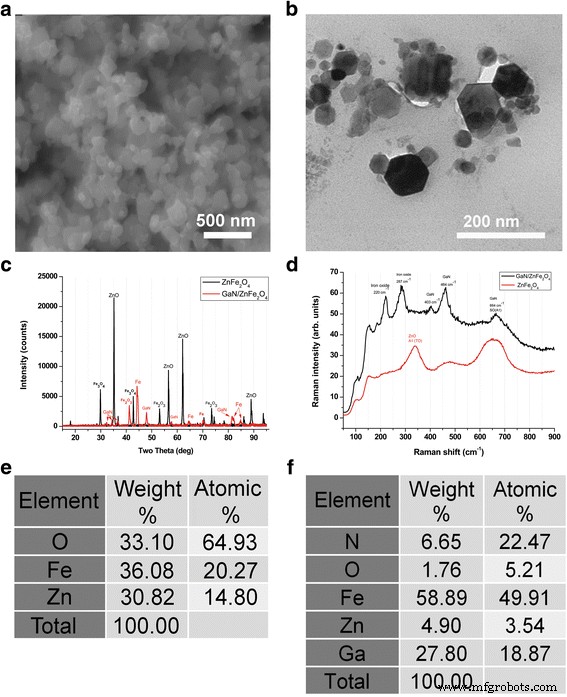
ナノ粒子の分析。 a Fe 2 と合金化されたZnOの犠牲ナノ粒子上に成長したGaNナノ粒子のSEM写真 O 3 。 b 得られたGaN / Feナノ粒子のTEM画像。 c 初期ZnFe 2 のXRDパターン O 4 ナノ粒子とその結果生じるGaN / ZnFe 2 O 4 ナノ粒子。 d GaN成長後の初期および結果として生じるナノ粒子のラマンスペクトル。 e Fe 2 と合金化したZnOのEDX分析 O 3 ナノ粒子。 f GaN層の成長後に得られたナノ粒子のEDX分析
GaN / Feベースのナノ粒子を初代ブタ大動脈内皮細胞とインキュベートしました。以前に示したように、GaNナノ粒子は100μg/ ml未満の濃度で内皮細胞に許容されます[5]。インキュベーションプロセス中、内皮細胞は、細胞の移動と増殖を維持しながら、周囲の培地中のナノ粒子の大部分を占めます。それにもかかわらず、培地中のナノ粒子の濃度の増加に伴い、生細胞の数がいくらか減少することに気づきました。この傾向は、図2に示したXTTアッセイの結果によって確認されています。
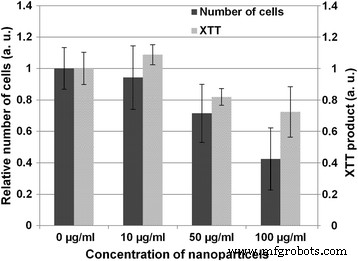
細胞生存率に対するナノ粒子の影響。細胞をさまざまな濃度のナノ粒子とインキュベートした1日後に測定された、濃度依存のXTT減少。 XTTアッセイの最後にカウントされた細胞の数は、未処理の細胞と比較して表されます。値は、6回の反復による2回の独立した実験の平均±標準偏差として表されます
GaN / Feナノ粒子が細胞とどのように相互作用するかを理解し、細胞内でのそれらの局在を特定するために、透過型電子顕微鏡(TEM)を使用して徹底的な形態素解析を実行しました。ブタ大動脈内皮細胞を50μg/ mlのナノ粒子と1日間インキュベートした後、ナノ粒子は細胞内の小胞に局在することが証明されました(図3a)。細胞質または細胞核にナノ粒子は見つかりませんでした。ナノ粒子の取り込みプロセスを図3b–dに示します。ナノ粒子のほとんどは、古典的な取り込み経路の1つ、つまりマイクロピノサイトーシス、クラスリン介在性エンドサイトーシス、またはカベオリン介在性エンドサイトーシスを介して細胞に取り込まれます[9]。内在化プロセスは、細胞の種類と局所的な細胞環境、および粒子自体の物理化学的特性(サイズ、形状、表面電荷など)に依存します。内皮細胞の場合、カベオリンを介したエンドサイトーシスは、この細胞型にカベオリンが豊富に存在するため、他のメカニズムよりもナノ粒子の取り込みに大きな影響を与えることが報告されています[10、11]。
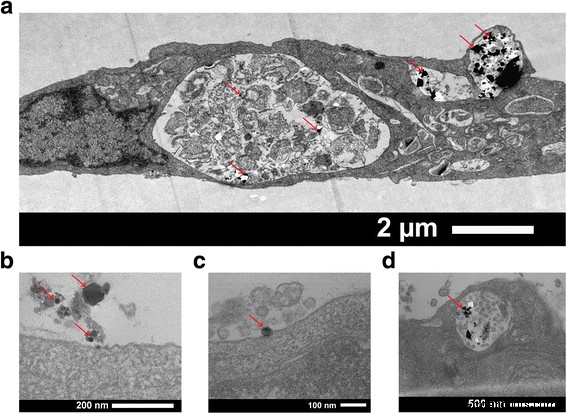
GaN / Feナノ粒子とインキュベートした単一の内皮細胞から撮影したTEM写真。 a 細胞小胞内のナノ粒子分布。 b – d 小胞へのナノ粒子の取り込みプロセス。 赤い矢印 生物学的媒体と比較して原子密度が高いため、TEMで暗く見えるナノ粒子を示します
前述の大量のFeの取り込みにより、得られたナノ粒子は、GaN半導体材料に固有の圧電性とともに強磁性を示します[12、13]。これらの2つの基本的なプロパティは、ナノ粒子の一部のプロセスのリモートアクティベーション、および/または関連するメディアでの制御されたガイドと空間分布に使用できます。圧電特性を使用して、たとえば、印加された超音波場によってGaNナノ粒子に電気分極を誘発することができます。このようにして、電気信号を細胞に送信して、特定の細胞プロセスを活性化または阻害することができます。鉄含有量によって与えられる磁気特性に関しては、それらは細胞の空間的位置の動的な視覚化と制御に到達することを可能にします。後者の可能性を実験的に実証するために、内皮細胞を50μg/ mlのGaN / Feナノ粒子を添加したEGM™-2培地で3日間(70〜80%の細胞コンフルエンスまで)インキュベートしました。その後、細胞を表面から剥がし、EGM™-2に再懸濁しました。 TrypLE™Selectによる細胞の剥離と遠心分離は、細胞の生存率に影響を与えず、細胞からのナノ粒子の放出も引き起こさないことに注意してください(データは示していません)。播種直後に、細胞を標準的なインキュベーター内で37°C、5%CO 2 下でインキュベートしました。 、培養プレートが永久磁石上に置かれた場所。図4は、磁場の存在下と非存在下でのナノ粒子を含む内皮細胞の分布を示しています。図4aは、磁場の非存在下でインキュベートされたナノ粒子を含んだ細胞を示していますが、図4bでは、ナノ粒子のない内皮細胞が磁場中でインキュベートされています。これらの写真は、両方の場合の細胞のランダムな分布を示しています。磁場勾配でのナノ粒子を含む細胞のインキュベーションは、磁場マップに従って、特定の領域での細胞の事前に設計された分布につながります。図4cは、直径5 mm、厚さ1mmの7つの希土類ネオジム円形磁石によって生成された磁場で1日間培養した後の培養プレート内の細胞を示しています。図4dは、直径7 mm、厚さ1mmの単一のリング状の磁石によって生成された磁場でのインキュベーション後の細胞分布を示しています。どちらの場合も、磁石は培養プレートの下に配置されました。
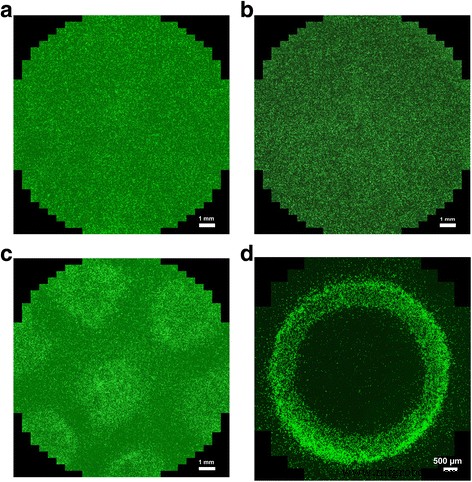
磁場を使用したナノ粒子を含む内皮細胞の誘導。対照群は、 a の空間分布を示しています ナノ粒子を標的とし、磁場および b の非存在下でインキュベートされた内皮細胞 磁場中でインキュベートされたナノ粒子を含まない内皮細胞。 c 、 d 磁場中での1日間のインキュベーション後のナノ粒子を標的とした内皮細胞の分布
結論
磁気特性を示すGaN / Feベースのナノ粒子が内皮細胞に取り込まれ、小胞内に保存されることを初めて実証しました。 GaN / Feナノ粒子を含む内皮細胞は、印加された磁場を使用して制御された方法で誘導することができます。これらの結果は、invitroで3次元組織を操作したり、invivoで細胞を組織損傷部位に標的化するための新しい可能性を開きます。これに加えて、固有の圧電特性を備えたGaNナノ粒子が細胞内に存在することで、細胞の生物学的プロセスの遠隔電気刺激への道が開かれます。この有望なアプローチは、私たちの研究室で調査中です。
略語
- EDX:
-
エネルギー分散型X線分析
- EGM™-2:
-
内皮増殖因子培地
- Fe:
-
鉄
- Fe 2 O 3 :
-
酸化鉄(III)
- GaN:
-
窒化ガリウム
- GFP:
-
緑色蛍光タンパク質
- H 2 :
-
水素
- HCl:
-
塩化水素
- NH 3 :
-
アンモニア
- OsO 4 :
-
四酸化オスミウム
- PBS:
-
リン酸緩衝生理食塩水
- SEM:
-
走査型電子顕微鏡
- TEM:
-
透過型電子顕微鏡
- XRD:
-
X線回折
- ZnO:
-
酸化亜鉛
ナノマテリアル
- 化学センシング用の貴金属ナノ粒子で装飾されたエレクトロスピニングポリマーナノファイバー
- CuSナノ粒子でコーティングされた着色および導電性CuSCN複合材料の容易な合成
- 光触媒活性が強化されたAgナノ粒子/ BiV1-xMoxO4の相乗効果
- 6-メルカプトプリンとニューロン透過性ペプチドで修飾された金ナノ粒子によるSH-SY5Y細胞増殖の促進
- クルクミンの処理効果を持つPEGコーティングされたCoFe2O4ナノ粒子の毒性
- 抗菌剤として銀ナノ粒子で装飾された酸化グラフェンベースのナノコンポジット
- ペロブスカイト太陽電池の変換効率に及ぼすTiO2コンパクト層に埋め込まれた異なるサイズと濃度のAgナノ粒子の影響
- トランスフェリン受容体による細胞内在化が増強されたパクリタキセルベースの標的脂質ナノ粒子の抗増殖およびアポトーシス誘発能—白血病細胞での研究
- リトコール酸で修飾された金ナノ粒子の肝臓癌細胞に対するアポトーシス効果
- 膀胱癌細胞を阻害するための疎水性修飾プルランナノ粒子を用いたミトキサントロンの新規送達および阻害効率に対するナノ薬物サイズの影響
- MnFe2O4ナノ粒子で装飾された還元型酸化グラフェンによるテトラサイクリンの吸着



