Pr2CuO4ナノシートの制御された合成と選択的吸着特性:メカニズムの議論
要約
正方晶相Pr 2 CuO 4 厚さ約60nmのナノシートは、配位化合物法(CCM)を使用して合成され、水溶液中のマラカイトグリーン(MG)に対する高効率の選択的吸着剤として使用されました。 Pr 2 CuO 4 サンプルは、X線回折(XRD)、走査型電子顕微鏡(SEM)、高分解能透過型電子顕微鏡(HRTEM)、X線光電子分光法(XPS)、UV-Vis拡散反射スペクトル(DRS)、および標準を使用して特性評価されました。 Brunauer–Emmett–Teller(BET)メソッド。最大吸着容量( Q m )準備されたままのサンプルは、異なる吸着剤投与量( m )の吸着等温線によって決定されました。 )ラングミュアモデルに基づく298、318、および338 Kで0.03〜0.07g。 m のとき <0.03gまたは> 0.07 g、全身質量損失と粒子凝集の影響が、298 Kでのラングミュアモデルからのデータ偏差について議論されました。水素結合と配位結合に基づいて、Pr <によるMGの選択的吸着の可能なメカニズムsub> 2 CuO 4 提案されており、CuOとPr 2 の吸着実験によってさらに検証されました。 O 3 MGおよび競合イオン実験に向けて。最後に、理論的研究をDFTレベルで実行して、吸着プロセスの可能性を明らかにしました。
背景
過去数十年にわたって、メチルオレンジ(MO)、メチレンブルー(MB)、ローダミンB(RhB)、マラカイトグリーン(MG)などの染料が原因で、産業から排出される染料含有廃水は特に危険な汚染物質です。人体では生分解性ではありません[1,2,3,4,5,6]。これらのうち、一般的に使用される染料としてのMGは、最近、魚卵の殺菌剤として使用されています[7、8]。したがって、それは他の廃水と一緒に地表水に現れることが多く、人間の健康に深刻な脅威をもたらします[9、10]。その結果、ナノ酸化物(すなわち、ZnOおよびZrO)[11,12,13]、メソポーラス材料(すなわち、秩序化されたメソポーラスカーボンおよびメソポーラスポリ(アクリル酸)/ SiO 2 などの多くの吸着剤 )[14、15]、およびいくつかの有機金属フレームワーク(MOF)[1]は、MGの吸着として機能することが報告されています。これらの吸着剤の中で、花のようなZnOが最大の Q で報告されました。 m (最大吸着容量)2587 mg / g。しかし、MGの吸着能力は、これらの吸着剤がさまざまな有機化合物で容易に覆われるため、実際の水中では大幅に低下します。したがって、有機染料の吸着には、大容量で選択的な吸着剤に焦点を当てた研究が重要です[7、8、16、17]。希土類銅酸塩が最大の特殊吸着容量(すなわち、 Q )を備えたMGの高い選択的吸着を示すことは心強いことです。 m Dy 2 の Cu 2 O 5 5.54 g / gより高い)[17];ただし、メカニズムはまだあまり明確ではありません。
この希土類銅酸塩の選択的吸着は、他の染料とは異なるMGの特定の分子構造に基づいて研究する必要があります。 Y.Liらによって報告されたように。 [4]、MGは水溶液中に異性体(ロイコマラカイトグリーン、LMG)を持ち、配位可能な酸素原子を含んでいます。そのため、MOF [1、2、17]のように、吸着過程での配位結合に基づくメカニズムを提案しました。
この作業では、Pr 2 でのMGの吸着プロセスのラングミュアモデルからの吸着データの偏差についてより深い洞察を提供します。 CuO 4 吸着剤。もう1つの目標は、MGへのLn–Cu–O化合物の大規模な選択的吸着と、多層吸着メカニズムの可能性を説明することです。吸着過程で水素結合と配位結合が形成される可能性について、DFTレベルで理論的研究を行いました。
Ln 2 の化学的性質に関する報告はほとんどありません。 CuO 4 遷移金属酸化物および希土類酸化物の多数の触媒および吸着剤と比較した、タイプの希土類銅酸化物[18、19、20]。私たちの知る限り、これはPr 2 の吸着メカニズムに関連する最初のレポートです。 CuO 4 MGに向かって、大きな Q を伴う m 室温での値。
メソッド/実験
資料
Cu(OAc) 2 ・4H 2 O、Pr(NO 3 ) 3 ・5H 2 O、3,4-pdc、およびトリエチルアミンは、Sinopharm Chemical Reagent Co. Ltd.(Shanghai、China)から購入しました。マラカイトグリーン(MG)は、上海のアラジンインダストリアルコーポレーションから購入しました。この研究で使用されたすべての試薬は分析グレードのものであり、さらに処理することなく使用されました。
合成
CCMの前駆体[PrCu(3,4-pdc) 2 (OAc)(H 2 O) 2 ]•10.5H 2 Oは以前の研究[21、22]に従って調製されました。 Cu(OAc) 2 ・4H 2 O、Pr(NO 3 ) 3 ・5H 2 対応する化学量論的比率のO、3,4-pdc、およびトリエチルアミンを、1:1の体積比で水-メタノールの混合物に溶解しました。溶液を3時間撹拌し、次にろ過して、青色の多結晶が形成されるまで静置しました。次に、得られた結晶を、N 2 の下で異なる温度で1時間煆焼しました。 Pr 2 を生成する雰囲気 CuO 4 。
特性評価
調製されたままのサンプルのXRDパターンは、Cu Kαを使用してD / Max-RB X線回折計(リガク、日本)で取得されました。 スキャンレートでの照射(2θ )10〜90°で0.05°/ s。粉末の形態は、SEM(Zeiss Supra 55、ドイツ語)およびHRTEM(FEI Tecnai F30、アメリカ)を使用して特徴付けられました。選択された領域の電子回折(SAED)パターンと高角度環状暗視野(HAADF)イメージングは、個々のナノ粒子を測定するために取得されました。調製したままのPr 2 のサイズ分布 CuO 4 レーザー粒度計(Mastersizer 2000、英国)を使用して検出されます。調製されたままのサンプルの比表面積は、N 2 によって測定されました。 BuilderSSA-4300を使用した吸着/脱着実験。 DRSは、BaSO 4 を使用したUV-Visible(PERSEE T9、中国)分光光度法で測定しました。 参照サンプルとして。触媒の元素の酸化状態は、Mg K を使用したPHI5000 C ESCAシステム(日本)での高分解能X線光電子分光法(XPS)によって得られました。 14.0kVおよび25mAで動作するソース。
吸着実験
水溶液からのMGの吸着は、Pr 2 を使用したバッチ実験で行われました。 CuO 4 100rpmのオーバーヘッドスターラーを備えた吸着剤としての粒子。さまざまな吸着剤の投与量(0.03〜0.07 g)を1000mLの0.1g / LMG水溶液に添加しました。平衡が確立されたら、溶液をろ過し、UV-Visible(RF 5301)を使用してろ液を分析し、MGの残留濃度を測定しました。吸着量は式(1)を用いて算出した。 (1)。
$$ {q} _e =\ frac {\ left({C} _0- {C} _e \ right)\ times V} {m} $$(1)ここで、 q e (mg / g)は、平衡濃度および C での吸着容量です。 0 (mg / L)および C e (mg / L)は、それぞれ水溶液中のMGの初期濃度と平衡濃度です。 V (L)は初期溶液量であり、 m (g)は使用済みの乾燥吸着剤の質量を表します。
線形形式のラングミュア方程式とフロイントリッヒ方程式は次のように表されます
$$ \ frac {1} {q_e} =\ frac {1} {K ^ {\ theta} {Q} _m} \ times \ frac {1} {C_e} + \ frac {1} {Q_m} $$( 2)$$ \ ln {q} _e =\ ln {K} _F + \ frac {1} {n} \ ln {C} _e $$(3)ここで K θ はラングミュア定数であり、 K F および n Freundlich定数です。平衡前の吸着プロセスの速度論的特性は、上記のように等温吸着実験の時間応答を使用して分析された。比較のために、メチルオレンジ(MO)とローダミンB(RhB)を含む競合イオン(O–PrおよびO–Cu配位結合に関連)実験を同じ条件下で実行しました。競合するイオンの初期濃度は0.02g / Lに設定されました。
理論的研究
DFTの計算は、DMol 3 を使用して実行されました。 Materials Studio(バージョン7.1)のパッケージ。すべての核電子は、計算コストを削減するために有効なコアポテンシャルを使用して計算されました。分極関数(DNP)で設定された二重数値の品質基底関数は、システム内のすべての原子に使用されました。吸着剤の表面の形状最適化は、一般化勾配近似(GGA)でPerdewWang(PW91)交換相関汎関数を使用して実装されました。平面波動関数のカットオフエネルギーと自己無撞着場(SCF)の許容誤差は、340eVと1×10 − 6 に設定されました。 それぞれeV /原子。すべての計算は逆格子空間で実行されました。
結果と考察
特性
Pr 2 のXRDパターン CuO 4 さまざまな温度で合成されたサンプルを図1に示します。600〜700°Cで、Pr 2 の結晶子 O 3 そしてCuOはPr 2 なしで現れます CuO 4 、温度が低すぎてアクティブなPr 2 がないことを示しています O 3 およびCuOはPr 2 を形成します CuO 4 [21]。 800°Cでは、正方晶相のPr 2 に関連するいくつかの特徴的なピークがあります。 CuO 4 (PDF#22-0245)は、23.5°と31.5°のブラッグ角で観察できます。ただし、Pr 2 はまだ大量にあります O 3 サンプル中のCuO。 900°Cでは、より多くのPr 2 O 3 とCuOが反応してPr 2 を形成します CuO 4 わずかな量のCuOが残留しています。回折ピークは鋭くて強く、サンプルの結晶化度が高いことを示しています。他の不純物ピークは観察されず、Pr 2 の高純度が確認されました。 CuO 4 。温度が1000°Cまで上昇しても、サンプルは完全な純度を維持します。温度が1100°Cを超えると、サンプルの分解により、明らかにCuOの不純物相がより多く現れます。したがって、吸着実験で研究されたすべてのサンプルは、900°Cで合成されました。
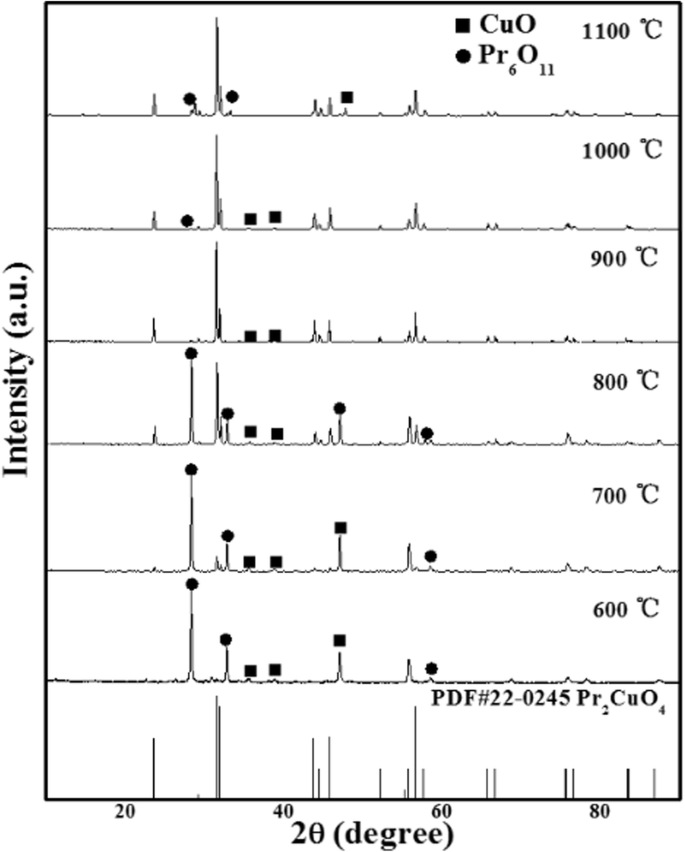
Pr 2 のXRDパターン CuO 4 600〜1100°CおよびPDF#22-0245
で合成図2a、bは、Pr 2 のSEM画像を示しています。 CuO 4 900°Cで調製された粒子。 Pr 2 CuO 4 粒子はよく分散したナノシートで、平均厚さは約60nmです。ほとんどのナノシートは溶岩のように積み重ねられていますが、層の構造はまだはっきりと観察されています。よく結晶化したナノシートの中には、規則的な八角形のシート構造を示すものはほとんどありません(図2bの黄色い円内)。ナノシートは相互接続されて、有機分子が通過するのに十分な大きさの3次元の穴を構築します。これは、吸着剤としての完璧な性質を示唆しています。参考文献に記載されているように。 [20]、配位前駆体は300°Cを超える温度で連続的に溶融して小さな移動相を形成し、次に固化して酸化物になり、最終的には重なり合うシートに分割されます(図2b)。金属イオンは配位前駆体に均一に分布しているため、生成物は低温(固体焼結法と比較して<900°C)での煆焼による多結晶粒子で構成されています。
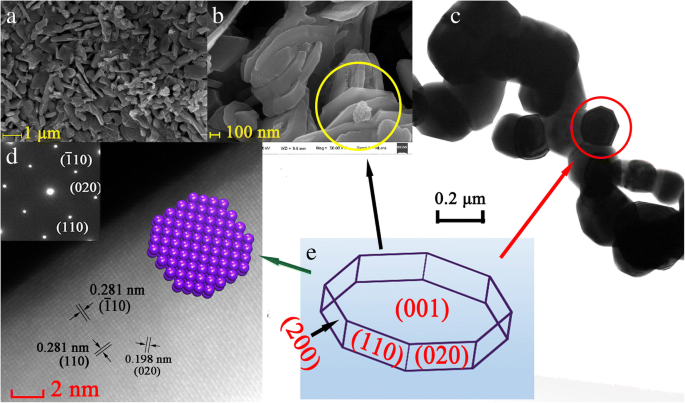
Pr 2 のSEM画像 CuO 4 900°Cで調製されたサンプル( a 、 b )、TEM( c )、SAEDおよびHAFFD画像( d )、および八角形の構造図( e )
Pr 2 の詳細な構造 CuO 4 さらに、高分解能TEM画像、SAED、およびHAADFによって明らかになります。図2cは、SEM画像と一致する八角形の構造(赤い円)を示しています。図2dのHAADF画像は、Pr 2 CuO 4 サンプルは明確な格子間隔を示し、その単結晶性を示しています。 0.281、0.281、および0.198 nmの格子面間隔は、正方晶系Pr 2 の(-110)、(020)、および(110)面とよく一致します。 CuO 4 、 それぞれ。図2b、cの八角形の薄片状構造の概略図が図2eにスケッチされており、多面体の側面のファセットインデックスは、対応する二面角とXRDの結果によって推測されます。まず、八角形の薄片状の側面の2つの結晶ファセットインデックスが(110)と(020)であることがわかります(図2d)。次に、八角形の隣接する辺の二面角が約45度に等しく、図1でインデックス付けされた観測された結晶面(200)の結晶面が片側であると推定されます。最後に、上面が側面に垂直であることを考慮して、上面の結晶ファセット指数は(001)であると決定されます。八角形のシートの厚さが薄いため、図1に示すように、{006}のX線回折強度は弱くなければなりません。これは上記の仮定を間接的にサポートします。したがって、準備されたままのサンプルは、{110}、{020}、{200}、および{001}に囲まれている可能性が高いと考えられます。 (001)平面の露出面積が最大であることを考慮して、DFTモデリングでは(001)結晶面が吸着面として選択されます。
図3は、Pr 2 の窒素吸着-脱着等温線と対応する細孔径分布を示しています。 CuO 4 吸着剤。等温線は、IUPAC分類によるタイプIII等温線を示しており、 p / p に凸であることがわかります。 0 多層吸着の開始を決定するための明確なポイントのない全範囲にわたる軸[23、24]。明らかなヒステリシスループは観察されず、弱いN 2 を示唆しています。 –pr 2 CuO 4 交流。さらに、その比表面積は11.6 m 2 と計算されます。 Brunauer–Emmet–Teller(BET)法によると、細孔径が10〜100Åの/ gであり、粒子間の間隔が非常に狭いことを示しています。これは、SEMの結果と一致しています。
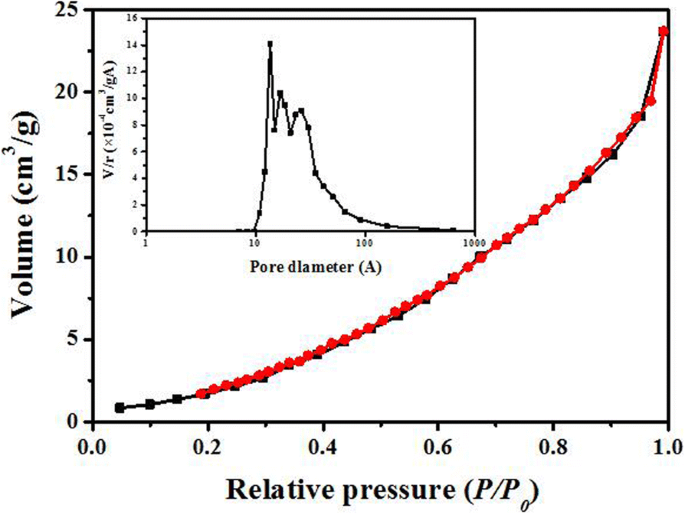
窒素の吸脱着等温線とそれに対応するPr 2 の細孔径分布 CuO 4 (吸着分岐の黒い線と脱着分岐の赤い線)
Pr 2 の表面化学組成と元素状態 CuO 4 吸着剤はXPSによって調査されます。図4aは、XPS調査スペクトルを示しており、サンプルにPr、Cu、O、およびC元素が含まれていることを示しています。 Pr、Cu、O、およびCの高分解能XPSスペクトルは、スピン軌道相互作用を考慮して非常にデコンボリューションされました。 Pr3dの高解像度XPSスペクトルを図4bに示します。 3d 5/2 のピーク および3d 3/2 それぞれ1073.1および1091.5eVで観測され、+ 3の形式電荷を持つ化学当量のPrイオンの存在を確認します[25,26,27]。図4cに示すように、Cu 2p XPSスペクトルは、1つのスピン軌道相互作用を持つCu2pスペクトル領域のコアレベルを示しています。主なピークはCu2p 1/2 を表します 953.8eVおよびCu2p 3/2 で 933.6 eVで、約20 eVのエネルギー差があります。これは、CuO 4 のCuイオンに起因する可能性があります。 +2の形式電荷を持つグループ[28]。一方、929.5 eVで観察された小さなピークは、Cu 2pの衛星ピークに起因する可能性があります。これは、吸着剤表面の対称性の低い配位環境を持つCuイオンが原因である可能性があります。図4dは、それぞれ531.3eVと535.6eV(より正)の2つの異なる原子価のOを示しており、2種類の非等価O原子があることを示しています。 531.3 eVを中心とするピークは、CuO 2 内の2つのCu原子と4つのPr原子に囲まれたO原子を表しています。 Pr 2 のレイヤー CuO 4 格子、535.6 eVのピークは、Pr 2 の4つのPr原子と配位したO原子に割り当てられます。 O 2 Pr 2 のレイヤー CuO 4 格子[29]。図4eでは、不定炭素の結合エネルギー(284.7 eV)が電荷補正に適用されています。ただし、289.5 eVのピークは、C–O種に起因する可能性があり、CCMの特性の1つと見なすことができるC残基の存在を示唆しています。
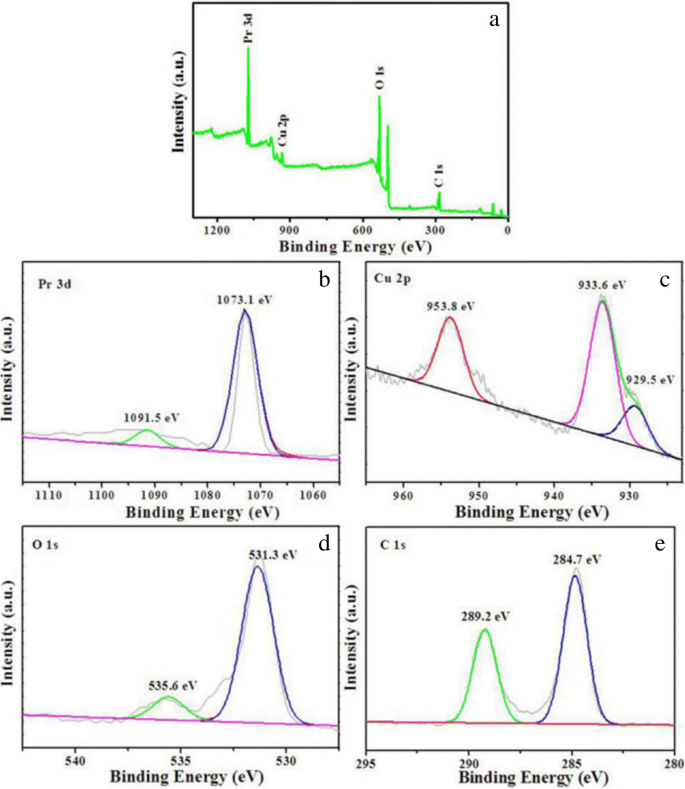
総XPSスペクトル( a )およびPr 3d( b )の高分解能XPSスペクトル )、Cu 2p( c )、O 1 s( d )、およびC 1 s( e )のPr 2 CuO 4
図5は、Pr2CuO4のUV-Vis吸収スペクトルを示しています。 Cu–OとPr–Oの強いd–d電子遷移と電荷移動遷移により、750〜300 nmの強くて広いスペクトル吸収帯をはっきりと観察できました[30、31]。したがって、サンプルは濃い青色で表示されます。光の強い吸収により、Pr2CuO4は潜在的な光触媒になりますが、光触媒現象は観察されていません。これは間接的に、Pr2CuO4の光生成された電子正孔対の再結合が集中的であることを意味します。直接バンド間エネルギーギャップは0.51eVと計算され(図5の挿入図)、光生成電子が格子振動によって容易に緩和される可能性があることを示しています。したがって、Pr2CuO4の光触媒特性は観察されません。
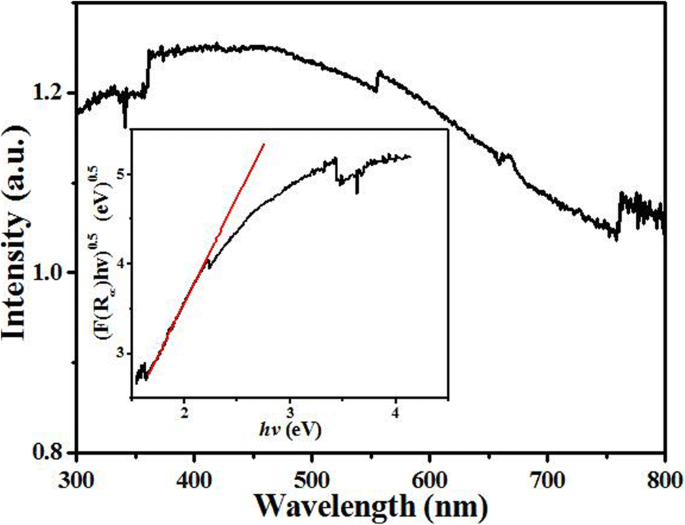
Pr 2 のUV-Vis拡散反射スペクトル CuO 4 サンプルと決定された直接バンド間遷移エネルギー
最大吸着容量とメカニズム
Pr 2 の吸着容量 CuO 4 図6a〜cに示すように、298、318、および338Kでの平衡吸着実験によって評価されます。吸着反応が298Kで平衡に達すると、MGの平衡濃度は、吸着剤の投与量を増やすと大幅に減少します(図6a)。温度が上昇すると、同じ用量の吸着剤の場合、MGの平衡濃度は徐々に増加します。これは、温度の上昇がMGの脱着にプラスの影響を与えることを示しています(図6b、c)。 Langmuirモデル(式2)とFreundlichモデル(式3)[32]によると、図6a〜cのデータは図6dに示されています。関連するパラメータの値と対応する R 2 表1にリストされています。結果は、等温線が R の値が高いほど、ラングミュアモデルによく従うことを示しています。 2 Freundlichモデルより。したがって、 Q m Pr 2 の CuO 4 ラングミュアモデルに従って計算された吸着剤は、298Kで3.52g / gに達します。比較のために、いくつかの選択された吸着剤の最大MG吸着容量を表2にまとめています。私たちの知る限り、 Q m Pr 2 の CuO 4 MGへの変換はアナログSm 2 のそれよりわずかに低いだけです CuO 4 しかし、竹ベースの活性炭などの物理吸着剤よりもはるかに大きいため、吸着メカニズムは通常の物理吸着とは異なる可能性があります。 Q m Pr 2 の CuO 4 温度が338Kに上昇すると、2.17 g / gに減少します。同時に、平衡定数( K θ )906から667 L・mol − 1 に低下 温度が298Kから338Kに上昇すると、吸着プロセスが発熱することを意味します[33]。
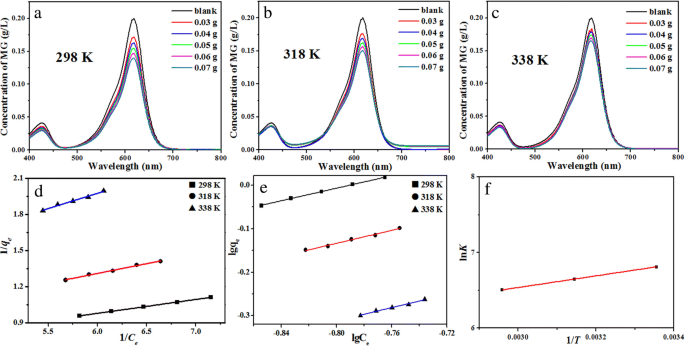
298でのCCMの最大吸着実験における品種MG平衡濃度( a )、318( b )、および338 K( c )および式による対応するフィッティングライン。 (2)、(3)、および(4)は( d )に示されています。 、 e 、および f )、それぞれ
熱力学的パラメータは、表1のデータから式(1)に従って適合されます。 (4)結果を図6f [34]に示します:
$$ \ ln {K} ^ {\ uptheta} =\ frac {-{\ Delta} _r {G_m} ^ {\ theta}} {RT} =-\ frac {\ Delta_r {H_m} ^ {\ theta}} {R} \ times \ frac {1} {T} + \ frac {\ Delta_r {S_m} ^ {\ theta}} {R} $$(4)ここで、Δ r G m θ 、Δ r H m θ 、およびΔ r S m θ は、それぞれ1 mol MGの吸着に対する標準ギブズの自由エネルギー変化、標準エンタルピー変化、および標準エントロピー変化です。
Δ r G m θ 、Δ r H m θ 、およびΔ r S m θ それぞれ、− 16.9 kJ / mol、− 6.41 kJ / mol、および35.1 J / mol・Kと計算されます。 Δの負の値 r G m θ 吸着反応が自発的であることを示します。 Δの負の値 r H m θ さらに、温度の上昇に伴う平衡定数の減少を解釈します。 Δの正の値 r S m θ 吸着剤の表面が最初は水分子で覆われており、吸着されたMG分子が表面の広い領域を占めていることを意味している可能性があります[33]。
偏差の分析
1 / q のプロット e 対1 / c e 式によると。 2と q e 式によって変更されます。 5 with m ’ 298 Kで0〜0.009 gの範囲が、図7aに示されています。 m ’の場合、プロットがはっきりと観察されます。 =0、ラングミュアモデルからの有意な偏差を示します(0.01 g < m <0.03gおよび0.07g < m <0.10 g)。したがって、1 / q のプロット e 対1 / c e 係数 m ’を導入して調整する必要があります 式によると。 5.図7bに示すように、0.001 g < m ’の場合 <0.003 g、 R 2 m ’で着実に増加 、 R 2 m ’の場合、急速に減少します 0.004gを超えています。したがって、 m ’の最適値 は0.003gであり、吸着剤粒子の凝集など、何らかの理由で系統的なエラーが発生している可能性があることを示しています。吸着剤粒子の凝集は、MG分子の吸着後の吸着剤粒子の粘度の増加に起因する可能性があります。対応するメカニズムとプロセスについては、次のセクションで説明します。
$$ {q} _e =\ frac {\ left({C} _0- {C} _e \ right)\ times V} {m- {m} ^ {\ hbox {'}}} $$(5)<図> <画像>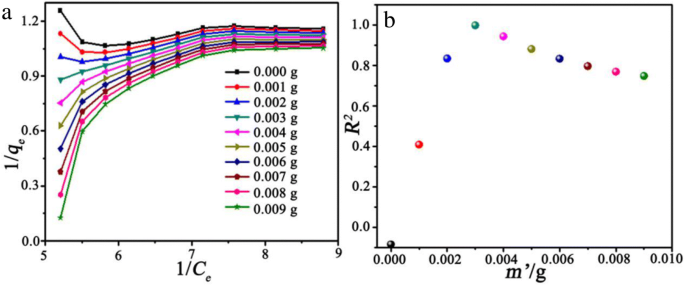
1 / q のプロット e 対1 / c e 式によると。 2(ここで、 m ’ = 0 )with q e 式によって変更されます。 m ’の値が異なる5 298 Kで0.000〜0.009 gの範囲( a )。対応する R 2 m ’の関数として ( b )
前述の補正方法は、 m の場合の偏差をうまく説明できます。 <0.04 g、ただし m の場合> 0.07 g、偏差を説明するのは非常に困難になります。 m の高次項の追加 m ’ m の偏差を説明するオプションです> 0.07 g;ただし、その物理的な意味はあいまいになります。別の方法は、多層吸着理論を採用することです。明らかな実験的現象である、容器の壁に濃い青色の斑点が現れることは、この理論を裏付けています。これは、吸着剤粒子の凝集の可能性を示唆しています。図8に示すように、MGの吸着中にH原子が再配列したことが原因である可能性があります[4]。水素原子の移動によりO - が生成されます。 イオンとNH 3 + イオン、双極MGを生成します。 MG分子の分極により分子間相互作用が大幅に増加するため、MG分子が吸着された吸着剤粒子は凝集して容器の壁に付着する傾向があります。溶液として1:1の体積比の水性/エタノール混合溶液を使用し、上記の等温実験を298 Kで繰り返しました。凝集の程度は、水性/エタノール混合溶液で明らかに減少しました。これは、脱分極によって説明できます。弱極性溶媒中のMG分子の分析。
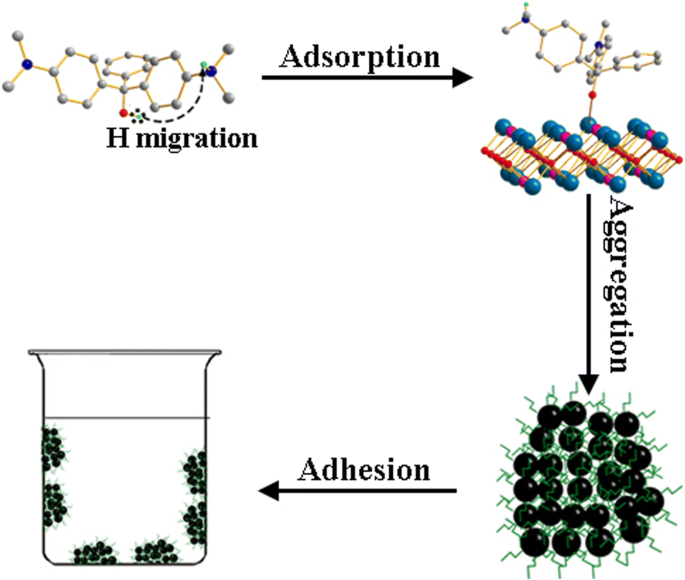
Pr 2 の集計プロセスの概略図 CuO 4 巨大な Q を持つ粒子 m 水と水/エタノール混合物中
DFTレベルでの理論的分析
上記の仮定は、DFT法によってさらに分析されます。 Liらによって報告されたように。 [4]、MGの異性体(図9)には、吸着剤のCuおよびPr原子と結合する能力を持つ配位可能な酸素原子が含まれています。このモードは、図9でルート1として説明されています。ルート1の吸着エネルギーは、DFTレベルでのO-Pr配位結合に基づいて62.5 kJ / molと計算され、Oより6.46 eV / mol大きくなります。 –cu。これに基づいて、ルート2は2つの段階で表されます。(i)MG分子のH原子は、28.8 kJ / molのエネルギー上昇と309.8kJ / molの活性化エネルギーで、ヒドロキシル基からアミノ基に移動します。 O–Hの結合エネルギーに近い。ただし、Oのイオン化は、83.3 kJ / molの大きな吸着エネルギーを持つより強力なO-Pr配位結合によって、吸着強度を高めます。ルート2の積は、ルート1と比較して20.8 kJ / mol安定しています。O MG の長さ –Pr配位結合は2.99Åと計算され、Cu–Pr配位複合体よりもわずかに大きく(CCDC:1524771では2.36Å)、PrとO MG の間の強い相互作用を示唆しています。 。 (ii)イオン化されたMG分子は、隣接するMG分子の分極を誘発し、MG分子間の静電相互作用を増加させ、さらにH···N結合を形成する可能性があります。その結果、26.4 kJ / molのエネルギー降下を伴う多層吸着が得られます。ルート2の値は、上記の熱力学的結果とより一致しており、ルート2の信頼性が高いことを意味します。水素結合の形成後(図10)、O–Hの結合長は1.07Åに伸び、遊離MG分子よりも0.10Å長くなります。 H…NのH結合長は約1.60Åであり、MG分子間の共有相互作用が水素結合の形成に重要な役割を果たしていることを意味します。ルート2では、Pr 2 の表面に多数のイオン化MG分子が吸着しました。 CuO 4 は静電的に粘性があり、吸着プロセス中の吸着剤粒子の凝集を説明している可能性があります(図8)。したがって、多層吸着経路が主要なモードである可能性があり、これは大きな Q を説明する可能性があります m Pr 2 の CuO 4 良い。上記のメカニズムは、Tang [35]によって報告されたイオン化可能な化合物のpH依存性吸着のメカニズムと類似しています。
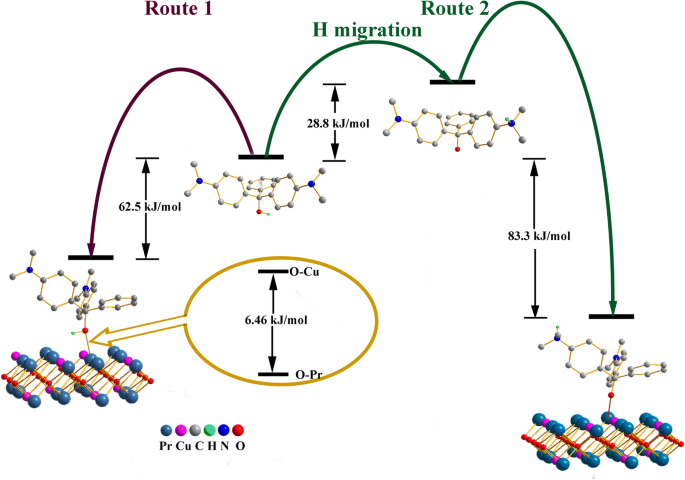
DFT研究に基づくルート1と2のエネルギー変化の概略図
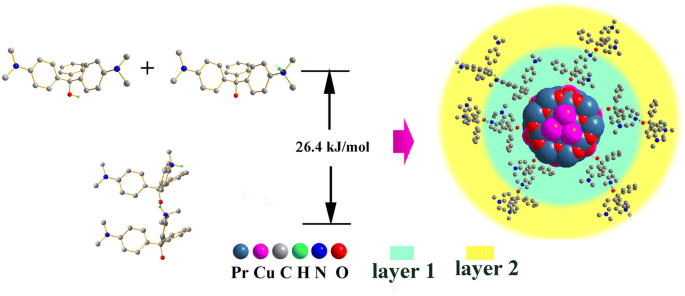
双極子MG分子間の水素結合による多層吸着のエネルギー変化の概略図
吸着メカニズムをよりよく理解するために、さまざまな競合イオン、染料、酸化物を使用した等温吸着実験も実施し、データを図11に示します。MOやRhBなどの染料は、吸着プロセスにほとんど影響を与えません。 Pr 2 を提案する CuO 4 選択的吸着剤です。イオン(Cl - 陰イオンとNa + カチオン)も吸着プロセスにわずかな影響を示し、選択的吸着が静電吸着とは異なることを示唆しています。 OAcの効果 − Cl − よりも強い 、O–CuおよびO–Pr配位結合の形成に一部起因します。同様に、Cu 2+ およびPr 3+ 配位結合を介したMGの吸着を効果的にブロックできます。一方、CuOとPr 2 O 3 吸着容量を大幅に増加させ、Pr 2 と同じ吸着メカニズムを持っている可能性があることを示しています CuO 4 。これらの実験結果は、配位吸着の見方をさらに支持するDFT分析と一致しています。
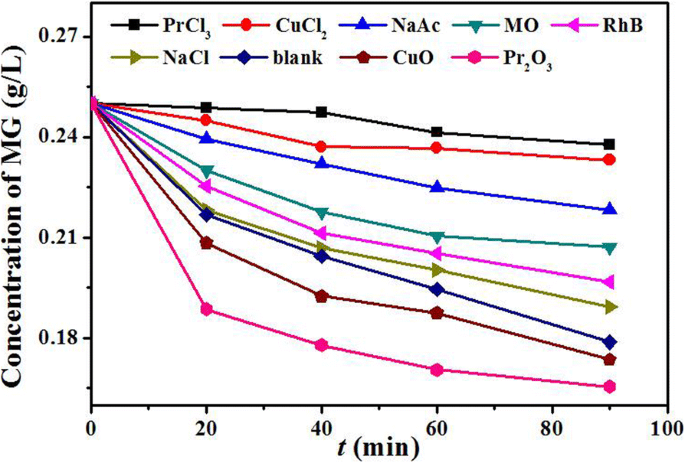
競合イオン、色素、CuO、およびPr 2 の影響 O 3 Pr 2 の吸着について CuO 4 MG用
結論
Pr 2 CuO 4 吸着剤は、 Q が大きいCCMを介して正常に調製されました。 m of 3.52 g/g at 298 K. The deviation of the adsorption data from the Langmuir model is due to the systematic mass loss of 0.003 g, when m < 0.04. When m > 0.07 g, the effect of agglomeration of particles on the adsorption capacity could not be ignored. The large adsorption capacity of Pr2 CuO4 adsorbent was discussed according to multilayer adsorption model:(i) the H atom of the MG molecule migrates from the hydroxyl group to the amino group to enhance the adsorption strength, with the adsorption energy of 83.3 kJ/mol. (ii) The polarized MG molecules are bound to each other by hydrogen bond during multilayer adsorption process with an energy drop of 26.4 kJ/mol. In addition, this multilayer adsorption mechanism was confirmed by the DFT studies and competing-ion experiments.
略語
- 3,4-pdc:
-
3,4-pyridinedicarboxylic acid
- CCMs:
-
Coordination compound methods
- HAADF:
-
高角度環状暗視野
- MG:
-
Malachite green
- MOF:
-
Metal-organic frameworks
- Qm :
-
The maximum adsorption capacity
- RhB:
-
ローダミンB
- SAED:
-
選択領域電子回折
ナノマテリアル
- 小さなセレンナノ結晶とナノロッドの容易な合成と光学的性質
- ゾル-ゲル法によるナノ構造シリカ/金-セルロース結合アミノ-POSSハイブリッド複合材料とその特性
- MnХFe3−XО4スピネルの構造的および磁気的特性に及ぼす接触非平衡プラズマの影響
- 水溶性α-NaGdF4/β-NaYF4:Yb、Erコアシェルナノ粒子の合成と発光特性
- 水溶性硫化アンチモン量子ドットの合成とそれらの光電特性
- 蒸発誘起自己組織化と強化されたガス検知特性によるワームホールのようなメソポーラス酸化スズの容易な合成
- グラフェン/ Ag3PO4量子ドット複合材料の簡単なワンステップソノケミカル合成と光触媒特性
- 修飾BiOClの合成と特性評価および水溶液からの低濃度染料の吸着におけるそれらの応用
- カチオン染料の効果的な選択的吸着のための表面官能化磁性ナノ複合材料の容易な合成
- ナノ粒子と超音波によって制御される水の過冷却
- 水溶性青色発光Mn合金CdTe量子ドットの合成と性質



