バイオイメージングおよび強化された細胞内薬物送達のための緑色蛍光カーボンドットの費用効果の高い調製
要約
ドキソルビシンに捕捉されたカーボンドット(DOX-CD)は、バイオイメージングと細胞内薬物送達の強化のために準備されました。 CDは、200°Cで1時間、クエン酸塩と尿素を使用した水熱合成法で合成されました。次に、DOXは物理化学的相互作用を介してCDに正常に結合されました。 DOX-CDは、良好な結晶構造、優れた水性安定性、優れたフォトルミネッセンス特性、および93%の高い量子収率を示しました。蛍光画像は、DOX-CDが細胞標識のために癌細胞に容易に取り込まれる可能性があることを明らかにしました。さらに、エンドリソソームのpH支援DOX放出挙動がDOX-CDから観察され、DOX-CDの細胞毒性はH0-8910卵巣癌細胞に対するMTSアッセイによって確認されました。さらに、CDは動物イメージング試験で明るい蛍光シグナルを示し、7日間および21日間の投与後に低い毒性を示しました。したがって、準備されたCDは、生物医学イメージングおよび細胞内ドラッグデリバリーのための有望なイメージングプローブになる可能性があります。
はじめに
ドキソルビシン(DOX)は、乳がん、肺がん、胃がん、卵巣がん、甲状腺がん、多発性骨髄腫、肉腫、小児がんなどのいくつかのがんの治療に広く使用されているアントラサイクリン化学療法薬です。 DOXの抗がん作用のメカニズムは、DNA合成と修復プロセスを妨げると考えられています。したがって、DOXは細胞膜を越えて細胞核に輸送され、癌治療中のDNA合成を妨害する必要があります。しかし、遊離DOXは細胞核に容易に近づくことができず、重度のin vivo心毒性を誘発するため、癌治療としての適用が妨げられました[1、2]。
最近、リポソーム、ミセル、ナノエマルジョン、高分子ナノ粒子、およびその他のナノ粒子などの多機能ナノキャリアが、抗がん剤送達におけるそれらの重要性について大きな注目を集めています[3]。その中でも、新しいタイプの量子ドットファミリーとして、カーボン量子ドット(CD)は2004年に発見されて以来、世界中で大きな関心を集めています[4]。特に、蛍光CDは細胞イメージングで好まれています 2 、光触媒、薬物送達、汚染物質および重金属イオンの検出、および準ゼロの重量とサイズ(<10 nm)での優れた特性、高い光安定性、広く連続的な励起スペクトル、調整可能な波長、生体適合性を満たすための光電装置、低毒性、および蛍光に対する優れた性能[5,6,7,8,9,10,11,12,13,14]。たとえば、Yang etal。抗がん治療を強化するためにDOXをCDに結合することに成功しました。これは、CDが核を標的としたドラッグデリバリーに大きな意味を持っていることを意味します[1]。
以前は、多数のバイオマス材料、炭化、不動態化、および表面機能化を含むCDを調製するためのさまざまな技術が提案されてきました[14、15]。詳細には、2つの主要な方法に分類できます。 1つは、「トップダウン」アプローチ、アーク放電、レーザーアブレーション法、電気化学エッチング、および酸化法です。これは、大規模な炭素構造を炭素ナノ粒子に分解することを意味します[16、17、18、19、20]。もう1つの方法は、分子前駆体からカーボンドットを合成する「ボトムアップ」法であり、主に熱水アプローチ、超音波法、および波動支援合成が含まれます[21、22、23、24]。 Xu etal。アーク放電、酸化、抽出、およびゲル電気泳動によって得られたカーボンドット。 Ming etal。電気分解によって獲得されたカーボンドット。ヤンら。異なる蛍光を発するカーボンドットを合成するために、元の水熱合成法を最適化しました[21]。しかし、これらの方法は、複雑な合成プロセス、時間のかかる手順、厳格な製造要件、および高価な原材料のために制限されています[25]。さらに、反応の不動態化剤として有機溶媒を使用すると、CDの毒性が高まる可能性があります[26]。さらに、報告されたCDのほとんどは、UV光励起下で青色の蛍光を発し、強い組織の自家蛍光干渉に起因する生物医学画像の分野での可能性を深刻に妨げました。
ここでは、クエン酸ナトリウム二水和物と尿素の緑色で効率的なワンステップ制御熱分解を介して緑色蛍光CDを合成しました。 DOXは、疎水性相互作用と静電相互作用、およびπによって、ドラッグデリバリー用に準備されたCDの表面に非共有結合で結合しました。 -π スタッキング相互作用[27、28、29]。 CDの形態と構造は、透過型電子顕微鏡(TEM)とX線回折分析によって調査されました。光学特性は、UV-vis分光計とフォトルミネッセンス(PL)発光スペクトルによって評価されました。持続的な薬物放出は、透析法によって実施された。 DOX-CDの細胞取り込みと細胞内分布を蛍光顕微鏡で調べた。 DOX-CDの抗癌効果は、標準的なMTSアッセイによって評価されました。 CDのinvivoイメージングはBalb / cヌードマウスで実施されました。最後に、CDの長期毒性を組織学的分析によって調査した。したがって、準備されたCDは、invivoイメージングおよび標的化ドラッグデリバリーの潜在的なエージェントになります。
材料と方法
資料
クエン酸ナトリウム二水和物、尿素、l-アルギニン、エチレンジアミンアセトン、硫酸キニーネ、リン酸緩衝生理食塩水(PBS)、酢酸、リン酸水素二ナトリウム、およびパラホルムアルデヒドは、Sinopharm Chemical Reagent Co. Ltd(上海、中国)から入手しました。 MTS細胞増殖比色分析キット(MTS)、ダルベッコ改変イーグル培地(DMEM /高グルコース)、ペニシリン-ストレプトマイシン溶液、およびトリプシン-EDTA溶液は、Beyotime Biotechnology Co. Ltd(上海、中国)から購入しました。ウシ胎児血清(FBS)は、Tianhang Biotechnology Co. Ltd(杭州、中国)から入手しました。 HO-8910卵巣癌細胞およびEA.hy926ヒト臍帯静脈内皮細胞は、中国科学院の上海栄養健康研究所(上海、中国)から入手しました。ドキソルビシン塩酸塩(DOX)は、Sigma-Aldrich(上海、中国)から購入しました。透析バッグ(MWCO =1000 Da)はSpectrumLabs(ロサンゼルス、カリフォルニア州、米国)から購入しました。
CDおよびDOX-CDの合成
簡単に説明すると、クエン酸ナトリウム二水和物(0.2 mmoL)と尿素(5 mmoL)を最初に1mLのDI水に溶解しました。次に、混合物をガラス容器に移し、200℃で1時間炭化した。その後、1 mLのDI水とアセトン(v / v、1/3)を添加し、10000rpmで10分間3回遠心分離しました。
DOXは非共有相互作用によってCDに結合されました。簡単に説明すると、DOX・HCl(0.5 mg)を5 mLのCD(5 mg / mL)に加え、暗所で48時間撹拌しました。得られた溶液を、透析バッグ(MWCO =1000 Da)内でDI水に対して24時間透析して、DOX-CDを得た。最後に、DOX-CDを凍結乾燥し、4°Cで保存しました。
CDおよびDOX-CDの特性評価
CDのサイズ形態は、透過型電子顕微鏡(TEM、FEI Tecnai G2 Spirit)によって特徴づけられました。 PL発光測定は、LS55蛍光分光光度計(PerkinElmer、米国マサチューセッツ州ウォルサム)で行われました。量子収率( QY )CDは、H 2 の硫酸キニーネ溶液を使用して測定しました。 SO 4 参考として。結晶構造は、Bruker Tensor27フーリエ変換赤外分光光度計(Pike Corporation、ウィスコンシン州マディソン)によって観察されました。 X線光電子分光法(XPS)は、ESCALAB250Xi分光計(Thermo、USA)を使用して実行されました。ゼータ電位は、ゼータポテンショメータ(Malvern Panalytical、Malvern、UK)で測定されました。
インビトロ薬物放出研究
DOX-CDからのDOXのinvitro薬物放出は、透析バッグを使用して調査されました。簡単に説明すると、DOX-CDを透析バッグに入れ、それぞれPBS(pH 7.4および5.0)に浸し、振とうインキュベーター(37°C、100 rpm)に入れました。所定の時間に、0.5mlのサンプルを取り出し、同量のPBSと交換した。放出されたDOXは、590nmでの蛍光強度によって記録されました。
インビトロ細胞毒性試験
DOX-CDの細胞毒性は、HO-8910卵巣癌細胞およびEA.hy926臍帯静脈内皮細胞に対するMTSアッセイによって決定されました[30、31]。簡単に説明すると、細胞を96ウェルプレートに0.5×10 5 の濃度で播種しました。 細胞/ mL、細胞接着を可能にするために24時間維持。次に、さまざまな濃度のDOX-CDを各ウェルに添加しました。 24時間のインキュベーション後、培地を吸引し、90μLの培地と10μLのMTSを各ウェルに添加しました。 4時間後、マイクロプレートリーダー(BioTek Epoch、Service Card)を使用して490nmでの吸光度を測定しました。細胞生存率は生存細胞のパーセンテージとして表され、3回の測定の手段として報告されました。
インビトロ細胞イメージング研究
HO-8910卵巣癌細胞を6ウェルプレートに接種し、細胞接着のために37°Cで24時間インキュベートしました。次に、細胞をDOX-CDとインキュベートして、細胞への取り込みを可能にしました。 4時間のインキュベーション後、培地を除去し、細胞を冷PBSで3回洗浄し、4%パラホルムアルデヒドで10分間固定しました。最後に、細胞の形態と蛍光分布を蛍光顕微鏡(Leica Microsystems、Wetzlar、Hessen、German)で視覚化しました。
In Vivo Imaging
動物実験は徐州医科大学の動物管理委員会によって承認された[32]。 Balb / cヌードマウスを使用して、蛍光イメージングにおけるCDの可能性を評価しました。簡単に説明すると、麻酔のために2%ペントバルビタールを腹腔内注射した後、注射部位にBalb / cヌードマウスにCD水溶液(50μL、6 mg / mL)を皮下注射しました。さらに、尾静脈からCD(5 mg / kg)を注射することにより、マウス体内のCDの生体内分布も調べました。さまざまな時点での蛍光評価のために、さまざまな臓器(心臓、腎臓、脾臓、肝臓、膀胱)を収集しました。動物の蛍光画像はTanon-5200MultiGel画像システムで撮影され、露光時間はすべての蛍光画像で1.0秒でした。
InVivo毒性研究
昆明マウス(雌、7週間)を使用して、CDのinvivoでの長期毒性を調査しました。昆明マウスはランダムに2つのグループに分けられました:CDとコントロールグループ。マウスに尾静脈(6 mg / kg)を介してPBSおよびCDを注射した。次に、注射の7日後と21日後に、心臓、肺、腎臓、肝臓、脾臓などの主要臓器を採取しました。その後、臓器を4%パラホルムアルデヒドで固定し、スライスし、ヘマトキシリンおよびエオシン(H&E)で染色しました。最後に、組織切片を光学顕微鏡(Leica Microsystems、Wetzlar、Hessen、German)で観察しました。
結果と考察
CDおよびDOX-CDの特性評価
CDは、クエン酸ナトリウム二水和物と尿素(クエン酸ナトリウム二水和物/尿素=1/25)を200°Cで1時間使用するワンステップ戦略によって作成されました。 DOXは、ドラッグデリバリー用に準備されたCDの表面に共有結合しました(スキーム1)。 TEM画像(図1a)に示すように、CDは、平均直径2.75 nm、サイズ分布が比較的狭い均一な球状の形態を示しました。さらに、CDの結晶構造は、高解像度のTEM画像(図1aの挿入図)で観察でき、顕著な格子縞を伴う十分な結晶性を示しています。
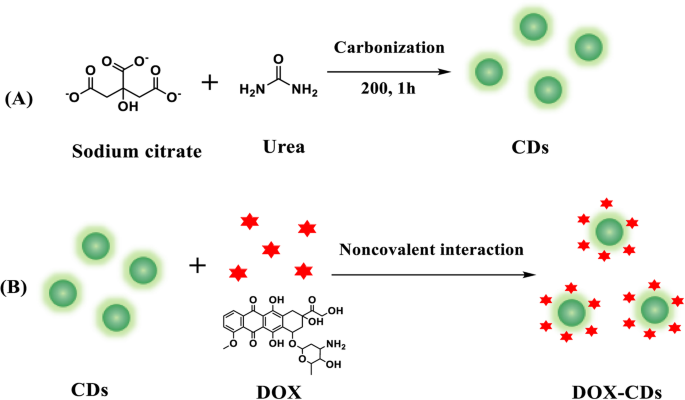
CDの概略準備( a )およびDOX-CD( b )
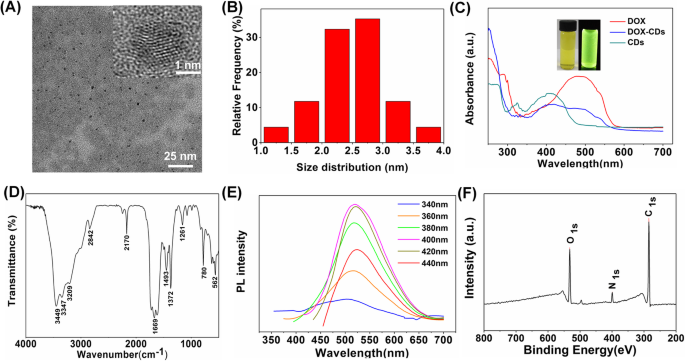
CDの特性。 a CDのTEM画像(挿入図、高解像度TEM画像)。 b CDのサイズ分布。 c DOX、CD、およびDOX-CDのUV-vis吸収と挿入図は、自然光とUV光の下でのCDを示しています。 d CDおよび e のFTIRスペクトル 20nm刻みで340nmから440nmまでの励起波長を持つCDのPL発光。 f CDのXPSスペクトル
CDの化学構造はFTIR分光法によって特徴づけられました。図1dに示すように、3499 cm -1 に鋭いピークがあります。 および1729cm -1 それぞれ–OHと–COOHに割り当てられ、780 cm -1 および1372cm -1 N–Hに起因する可能性があります。カルボキシル基とアミノ基の両方が官能基としてカーボンドットの表面に存在し、特定の機能を持つ生体高分子を修飾していると結論付けることができます。これにより、カーボンドットのさらなる応用研究の可能性が提供されます。
さらに、CDの光学特性はUV-vis吸光度とPL分光法を使用して調査されました。図1cに示すように、CDは410 nmに吸光度のピークを示し、DOXは500nmに吸光度のピークを示しました。一方、DOX-CDはCDとDOXの吸光度ピークをそれぞれ410nmと500nmに維持し、CDへのDOXの結合が成功したことを示しています。さらに、図1cの挿入図に示すように、DOX-CDs水溶液は、自然光の下では淡黄色で透明であり、UV励起下ではナットが明るい緑色に変わりました。さらに、蛍光量子収率は、参照としてキニーネ硫酸塩を使用して93%と計算されました( QY =54%)。 CDは340〜440 nmの波長で励起されたため、PLピークはほとんどシフトを示さず、CDの励起に依存しない発光特性を示しています。 CDの最大励起波長とPLピークは、それぞれ400nmと525nmです。励起に依存しないPLの振る舞いは、CDの均一な表面状態に起因する可能性があります[33]。
さらに、CDの元素組成はXPSによって決定されました。図1fに示されているように、XPSスペクトルは、CDが主に炭素( C )で構成されていることを示しています。 )、窒素( N )、および酸素( O )および対応する原子比は、それぞれ78.39%、7.52%、および14.1%でした。 C の3つの典型的なピーク 1S 、 N 1S 、および O 1S それぞれ284.8、399.5、532.6eVで観測できます。具体的には、 C 1S スペクトルは、284.8、286.7、および288.3 eVに3つのピークを示し、C–C、C–N、C–O、またはC =O結合の存在を個別に表しています(図S1A)。 N の高解像度スペクトル 1S C–Nに割り当てられた399.5eVにピークを示しました。さらに、 O 1s スペクトルはまた、それぞれ531.9および532.6eVでC =OおよびC–O結合の存在を確認しました(図S1B)。
CDの蛍光強度は、4°Cと室温の両方で素晴らしい安定性を維持しました(図S2A)。 4°Cで2週間で10%未満の蛍光強度の低下は無視できます。したがって、カーボンドットは生物医学的造影剤として使用するための長期安定性を備えていることが期待されます。
図S2Bは、CDのPL強度が高(> 10)または低(<3)pHの水溶液で減少したことを示しています。それにもかかわらず、PL強度はpH 3〜10の水溶液で安定していました。バイオマーキングおよびバイオイメージングに適用される調製済みのCDは、細胞と共培養する必要があります。この場合、pH条件はほぼ中性(pH =6〜8)であり、PLの安定性が保証されます。理論的には、調製されたCDは、バイオマーキングおよびバイオイメージングのために細胞内で高い安定性で蛍光を発することができることを示しました。
CDの蛍光安定性を明らかにするために、蛍光抗光退色試験を実施した。図S2Cに示すように、量子ドット(CdTe)や従来の蛍光色素(DAPI)と比較して、カーボンドットは高い蛍光強度だけでなく、優れた耐光退色性も示しました。さらに、CDは、DI水、PBS、FBS培地、DMEM培地、CM1-1培地などのさまざまな溶液にもよく分散しており、血液系での優れた安定性が期待されます(図S3)。
CDは、-31.1 mVのゼータ電位値を示しました(図S4)。これは、これらの粒子の表面に酸素およびカルボキシル官能基が存在するためと考えられます。潜在的な正に帯電したDOXは、カルボキシル基との静電相互作用および疎水性相互作用を介してCDの表面に物理的に付着する可能性があります。 DOX-CDは-9.7mVのゼータ電位値を示し、DOX-CD複合体の製造を確認します。さらに、CDにはsp 2 が含まれています -強力なπを介してDOXの芳香族構造をロードできるカーボンネットワーク -π 相互作用。最適なカプセル化効率と薬物負荷効率は、さまざまな濃度のDOXによって調査されました。図S5に示すように、最大カプセル化効率は50.82%と計算され、対応するローディング効率は0.1 mg / mLのDOXで6.82%でした。
DOX-CDのinvitro薬物放出
DOX-CDからのinvitroDOX放出挙動は、pH感受性DOX放出を調査するためにPBSで実施されました。これを実証するために、DOX-CDをさまざまなpH値(pH 7.4、6.0、および5.0)でインキュベートし、DOXの放出をモニターしました。図2に示すように、DOX-CDは、休止期間中、pH 7.4、6.0、および5.0で徐放性プロファイルを示しました。結果は、DOX放出がpH依存性であることを示した。 DOX-CDをpH7.4でインキュベートした場合、8時間以内に放出されたDOXはわずか13%でした。しかし、pH値を6.0または5.0に下げると、DOXの35%または65%以上がそれぞれDOX-CDから放出され、低pHに対するDOX-CDの感度が示唆されました。放出されたDOXの量がより低いpHで増加したことを示しました。これは、–NH 2 のプロトン化の増加に起因していました。 酸性環境でのDOX上のグループ。したがって、DOX-CDは、血液循環中のDOXの早期漏出を防ぎ、細胞内薬物放出を促進する可能性があります。それは癌の効果的な治療に大きな利益をもたらします。
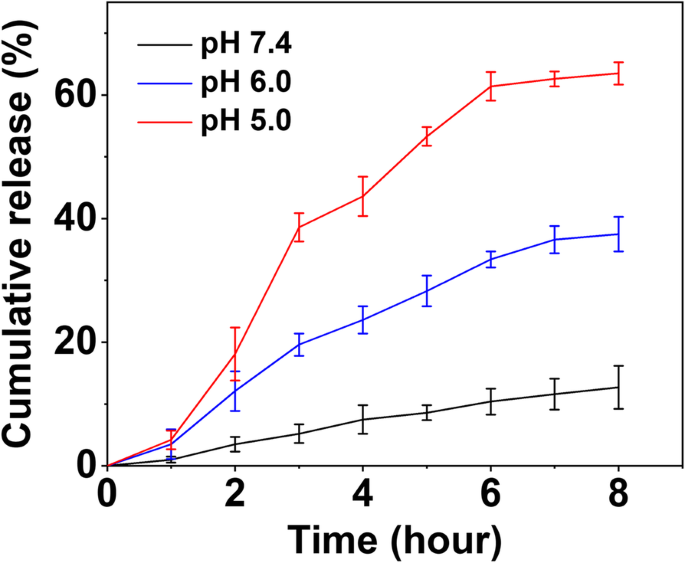
pH 5.0、6.0、および7.4でのDOX-CDのin vitroDOX放出プロファイル
インビトロ細胞毒性試験
生体適合性の問題は、生物医学イメージングおよびドラッグデリバリーに適用するためのCDにとって重要です。さまざまな濃度でのCDの細胞毒性は、HO-8910卵巣癌細胞およびEA.hy926臍帯静脈内皮細胞に対して実施されました。図3aに示すように、HO-8910細胞とEA.hy926細胞はどちらも、5 mg / mLの高濃度でも85%を超える高い生存率を維持しており、CDの優れた生体適合性と低い細胞毒性を示しています。
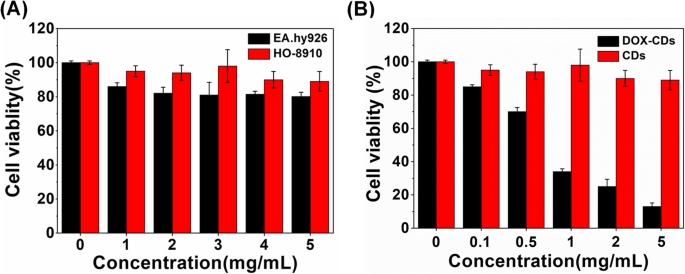
インビトロ細胞毒性。 a HO-8910およびEA.hy926細胞に対するCDの生体適合性。 b HO-8910腫瘍細胞に対するDOX-CDおよびCDの細胞毒性。値は平均±SD、( n =3)
DOXと組み合わせると、DOX-CDはHO-8910卵巣癌細胞に対してDOX濃度依存性の細胞生存率を示しました。図3bに示すように、特にDOXの濃度が0.05 mg / mLを超える場合、DOX-CDの細胞生存率はDOXフリーCDの細胞生存率よりも大幅に低く、DOX-CDの優れた抗がん効果を示しています。
インビトロ細胞取り込みおよび標識研究
DOX-CDの細胞内取り込み能力を評価するために、HO-8910細胞で細胞イメージングを調べました。図4に示すように、CDとDOXの存在に起因する癌細胞内で、それぞれ鮮やかな緑色と赤色の蛍光が観察されました。特に、強い緑色蛍光シグナルは主に細胞質に局在しており、CDの細胞内分布を示しています。逆に、赤い信号は細胞質と比較して細胞核で有意に強く、DOXがCDと結合を解除し、DNAとの高い親和性に起因する細胞核に直接移動する可能性があることを示唆しています。エンドソームとリソソームの低いpH値(5.0)は、DOX-CDからのDOXの放出を助ける可能性があると説明できます。したがって、DOX-CDは細胞標識および細胞内ドラッグデリバリーのための有望な薬剤である可能性があります。
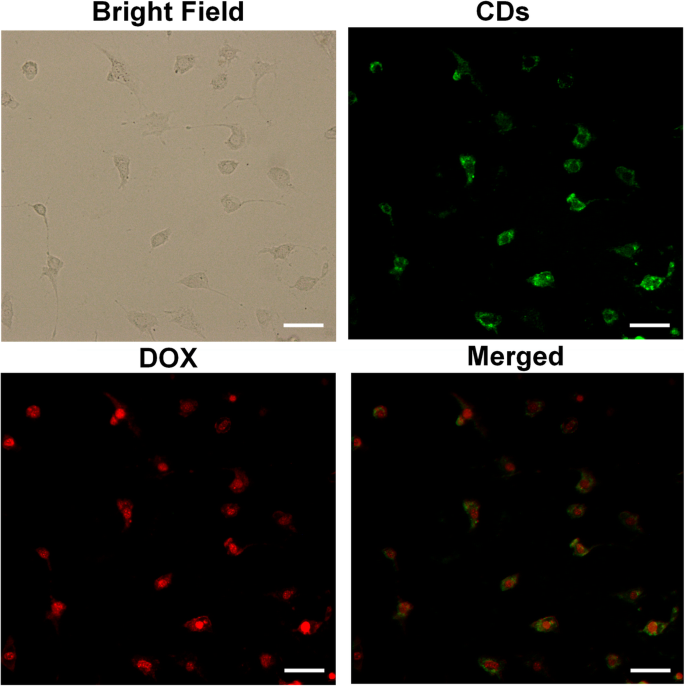
HO-8910細胞によるDOX-CDのinvitro細胞取り込み。スケールバー=50μm
InVivo動物イメージング研究
ヌードマウスにCD水溶液(50μL、6 mg / mL)を皮下投与した。次に、マウスを1%ペントバルビタールの腹腔内注射によって麻酔し、488nmの励起光と535nmの発光フィルターの下でTanon-5200MultiGelイメージングシステムによってイメージングしました。図5aに示すように、投与されたスポットで強い緑色の蛍光が観察され、これは、CDの蛍光がマウスの皮膚および組織に効果的に浸透できることを意味している。さらに、マウスは注射後も健康を維持しており、CDが優れた生体適合性と動物に対する低毒性であることを示しています。すべての結果を考慮すると、CDはinvitroおよびinvivoでのバイオイメージングのための優れた発光プローブとして機能しました。
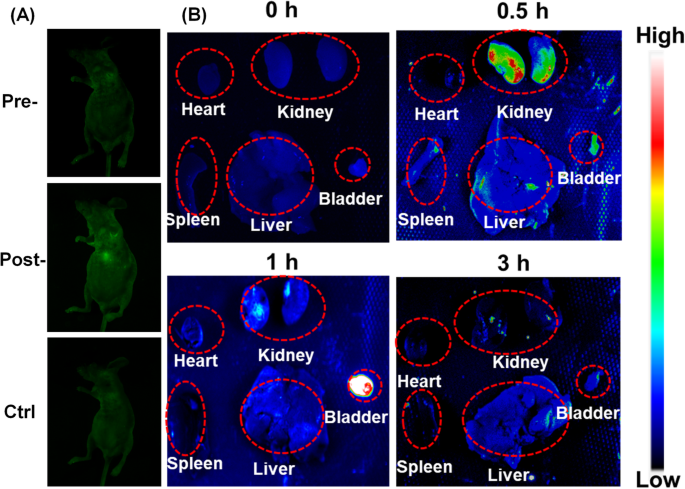
インビボ動物試験。 a CDによる動物の蛍光イメージング。 b 異なる期間でのCDの静脈内注射後のマウスのexvivoイメージング
さらに、CDの生体内分布および排泄経路は、尾静脈を介してナノプローブを注入することによって実行されました。さまざまな時点(0、0.5、1、3 h)で、さまざまな臓器を蛍光イメージングのために解剖しました。図5bに示すように、腎臓と膀胱は、注射後、心臓、脾臓、肝臓などの他の臓器と比較して、はるかに強い蛍光信号を示しました。さらに、腎臓の蛍光シグナルは、注射後0.5時間以内に有意に増加し、1時間後に徐々に減少しました。その後、膀胱内の蛍光シグナルは0.5hから1hに徐々に増加し、CDが腎臓から膀胱に送達されたことを示しています。その結果、CDは腎臓と膀胱のシステムによって排泄され、除去される可能性があることが示されました。
InVivo長期毒性試験
さらに、臨床研究でCDを使用する可能性を完全に調査するために、invivoでの長期毒性試験も実施されました。 KunmingマウスにPBSとCDを尾静脈から注射し、組織学的分析のために7日後と21日後に主要臓器(心臓、肺、腎臓、肝臓、脾臓)を採取しました。続いて、組織学的組織の図を顕微鏡で画像化して、実験群と対照群との間の病理学的差異を評価した。図6に示すように、CDを投与した動物の主要な臓器に顕著な臓器損傷や炎症性病変は観察されなかった。これは、調製したままのCDが臨床使用およびinvivo研究に安全であることを示唆している。したがって、合成されたままの緑色のCDは、バイオマーカーおよびバイオイメージングプローブとして生体適合性がありました。
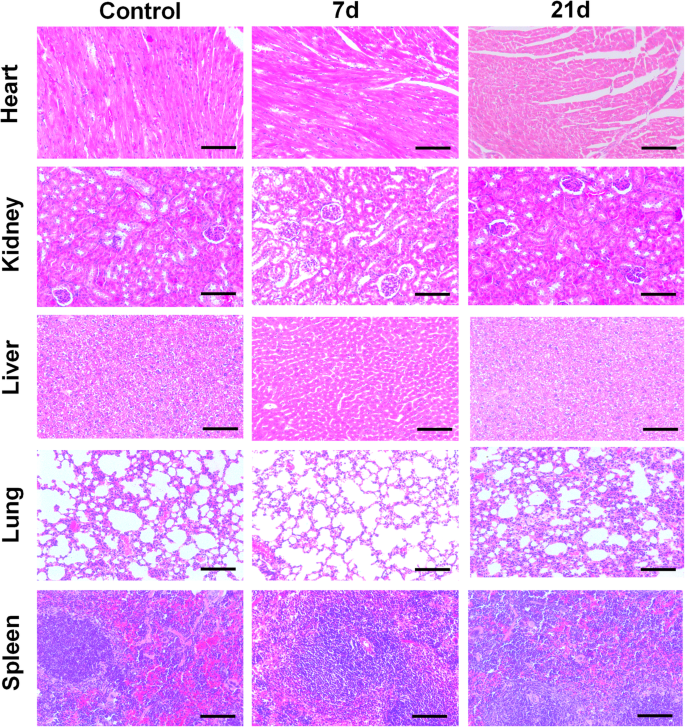
CDの7日および21日投与後の主要臓器の組織学的分析。スケールバー=100μm
結論
結論として、この作業は、 QY が高い緑色蛍光CDの費用効果の高い準備を示しています。 バイオイメージングと強化された細胞内ドラッグデリバリーのための93%の。 DOXはCDにうまく結合し、良好な結晶構造、優れた水性安定性、および優れたフォトルミネッセンス特性を備えたDOX-CDを形成しました。 DOX-CDは、細胞内pH環境に応答して、酸によって引き起こされる細胞内放出を促進する可能性があります。 pH感受性に起因して、DOX-CDはHO-8910細胞の増殖に対して効果的な阻害を示しました。 DOX-CDは優れた細胞標識能力を示し、エンド/リソソームpHに応答して、細胞内にDOXを放出しました。 CDはinvitroおよびinvivoの両方で蛍光プローブとして機能しました。最後に、組織学的分析により、CD処置マウスからの顕著な毒性効果は観察されなかった。それにもかかわらず、この研究は、費用効果の高い方法で調製されたCDが、生物医学的イメージングおよび細胞内薬物送達において大きな可能性を秘めている可能性があることを示しました。
データと資料の可用性
この調査中に生成または分析されたすべてのデータは、この公開された記事とその補足情報ファイルに含まれています。
略語
- CD:
-
カーボンドット
- DOX:
-
ドキソルビシン
- DOX-CD:
-
ドキソルビシンに閉じ込められたカーボンドット
- FBS:
-
ウシ胎児血清
- MTSアッセイ:
-
MTS細胞増殖比色分析キット
- PBS:
-
リン酸緩衝生理食塩水
- QY :
-
量子収率
- TEM:
-
透過型電子顕微鏡
- XPS:
-
X線光電子分光法
ナノマテリアル
- ドラッグデリバリーを強化するためのナノファイバーとフィラメント
- 黒色腫の標的化学療法治療のための薬物送達担体としての131I追跡PLGA-脂質ナノ粒子
- 細胞内タンパク質送達のためのシリカナノ粒子:緑色蛍光タンパク質を使用した新しい合成アプローチ
- Au @ TiO2卵黄シェルナノ構造の調製とメチレンブルーの分解および検出へのその応用
- 豆腐廃水から蛍光炭素量子ドットを合成するための簡単なアプローチ
- Fe3 +用の再開可能な蛍光プローブBHN-Fe3O4 @ SiO2ハイブリッドナノ構造とそのバイオイメージングへの応用
- 金および銀ナノ粒子のグリーン合成のためのPlatycodiRadix(Platycodon grandiflorum)からのPlatycodonサポニン
- 光熱治療のためのポリドーパミンカーボンドットの簡単なワンポット合成
- 硫酸を利用した赤色発光炭化ポリマードットの調製とバイオイメージングの応用
- アミノ末端HBP修飾rGOの光熱/ pH二重応答性ドラッグデリバリーシステムと腫瘍細胞に対する化学光熱療法
- 髄外多発性骨髄腫治療のためのスマートドラッグデリバリーシステムとしてのドキソルビシン負荷PEG-CdTe量子ドット



