抗癌剤送達システムとしての5-フルオロウラシルを用いたタウリン官能化酸化グラフェンの製造と特性化
要約
最近、癌治療薬用のナノキャリアシステム、特にGOベースのドラッグデリバリーシステムは、癌患者にとって恩恵になっています。この研究では、生体適合性を向上させるためにGO表面を機能化するためにTauを選択します。第一に、ナノスケールのGOは、修正されたHummerの方法と超音波ストリッピング法によって合成されました。タウリン修飾酸化グラフェン担体(Tau-GO)を化学法で合成し、ゼータ電位− 38.8 mV、粒度242nmの水中での分散性と安定性に優れたTau-GOを得ました。カプセル化効率の評価基準に基づいて、非共有結合によってTau-GOと5-FUを組み合わせるのに最適な製剤が決定されました。 5-FU-Tau-GOは、酸性環境よりも中性環境でより安定しており、特定のPH応答と徐放効果がありました。インビボでは、薬物動態試験および関連するパラメーターを使用して、それぞれ5-FUおよび5-FU-Tau-GOの経口および静脈内投与を比較し、5-FU-Tau-GOの経口または静脈内投与が5の作用時間を延長することを示した-体内のFUとその生物学的利用能を向上させます。さらに、MTTアッセイによって測定されたHepG2細胞の阻害は、IC 50 5-FUの値は196±8.73μg/ mLであり、IC 50 5-FU-Tau-GOの値は65.2±0.7μg/ mLでした。これは、5-FU-Tau-GOがHepG2細胞に対してより強力であり、癌細胞に対してより強力な阻害効果があることを示しています。 AO / EB染色を使用して測定された細胞形態への影響は、5-FU-Tau-GOが細胞を破壊するだけでなく、5-FUと比較してアポトーシスを有意に誘導することも示しました。また、コンピューター支援設計により、Tau-GOが未修飾のGOよりも5-FUによく結合できること、および形成された5-FU-Tau-GOシステムがより安定しており、5-の移動と放出に役立つことを確認しました。インビボでのFU。
はじめに
化学療法は今でもさまざまな癌の治療に使用される一般的な方法です[1]。ほとんどの化学療法剤の重大な障害は、有効濃度で腫瘍組織に浸透できないこと、または正常組織に対する望ましくない副作用です[2]。したがって、科学者たちは、効果的な薬物送達と治療を確実にするために、腫瘍組織での薬物放出の制御された速度を達成できる強力な薬物送達システムの開発に力を注いできました。
リポソーム[3]、ポリマー[4]、ナノ粒子[5]、デンドリマー[6]、ミセル[7]、酸化グラフェン[8、9]を含む多くのナノサイズの材料が、さまざまな薬物の送達のために開発されてきました。これらのナノ材料の中で、酸化グラフェン(GO)は、酸化グラファイトから化学的に剥離され、豊富な官能基、大きな比表面積、高い薬物負荷量、優れた分散性など、いくつかの魅力的な物理的および化学的特性を示す新しいカーボンナノ材料です。水中での能力[10,11,12]。さらに、インビトロ実験結果のほとんどは、低GO濃度が細胞増殖の基質として、および免疫細胞を活性化するために使用できることを示した。したがって、GOは、疾患診断[13]、癌細胞のイメージングと追跡[14]、癌の光熱療法[15]、組織工学[16]、標的化ドラッグデリバリー[17]、特に抗癌剤として広く使用されています。腫瘍ドラッグキャリア[18、19]。ただし、いくつかの研究グループは、高GO濃度が前臨床および臨床研究において明らかな細胞毒性効果を有することを報告しています。 GOがinvivoで毒性作用を引き起こすメカニズムは、酸化ストレスと細胞内活性酸素種の過剰産生によるもので、細胞アポトーシスを誘発し、重度の炎症、肺水腫、肉芽腫の形成を引き起こします[20]。したがって、GO毒性の問題を解決することは非常に重要です。
報告によれば、共有結合または非共有結合の機能化は、GOと細胞の間の強い疎水性相互作用を減らすことができます。これは、GOの機能化がその生体適合性を改善し、invivoおよびinvitroでの毒性をほぼ排除することを示したいくつかの研究によって実証されました。Yangetal。初めて、放射性標識法を使用して、マウスにおける共有結合PEG-GOの長期生体内分布を研究し、その結果は、PEG-GOがマウスから、おそらく尿や糞便中に徐々に排泄される可能性があることを示しました[21]。張ら。 DEXで機能化されたGOとGOを比較したところ、GO-DEXは細胞毒性を著しく低下させ、1週間以内にマウスからほとんど除去できることがわかりました[22]。さらに、GOのプルロニックF127への非共有結合は、生理学的条件での良性の溶解性と安定性、および低毒性をもたらします[23]。 GOを機能化するためにいくつかのポリマーまたは分子が使用されてきましたが、この分野では重要な結果が得られています。ただし、優れた生体適合性のGOベースの薬物担体を構築するための簡単な方法を開発するための努力は依然として必要です。
タウリン(タウ)は、安定性と水溶性に優れた半必須アミノ酸です。タウは、心血管および脳血管疾患を予防し、視覚機能を維持し、細胞を保護し、免疫を調節することができます。多くの研究が、タウが肺癌、胃癌、結腸直腸癌、および乳癌を含むさまざまな癌で重要な役割を果たす発現因子のアップレギュレーションまたはダウンレギュレーションを通じて抗腫瘍特性を有することを提案しています[24]。したがって、タウ機能化GOは、抗腫瘍薬の担体として優れた役割を果たす可能性があります。この記事では、初めて共有結合タウ官能化GOをナノキャリアとして使用し、invitroでその細胞毒性を評価しました。さらに、5-フルオロウラシル(5-FU)を抗がん剤として使用し、Tau-GOの表面に非共有結合でロードしてドラッグデリバリーシステムを構築しました。 5-FU-Tau-GOは、正常組織への副作用を軽減するだけでなく、薬剤のバイオアベイラビリティを向上させることができます。その結果、Tau-GOは、将来重要な生物医学的用途を持つ可能性のある新しいGOベースのナノ材料として成功裏に開発されました。
実験と方法
資料
グラファイト粉末、リン酸緩衝生理食塩水(PBS)およびジメチルスルホキシド(DMSO)は、Tianjin Laibo Chemical Co.、Ltd。から購入しました。カルボディイミド(EDC)、N-ヒドロキシスクシンイミド(NHS)、塩酸(HCl)、過酸化水素(H 2 O 2 30%)はShandong Yuwang Industrial Co.、Ltd。から購入しました。タウリン(タウ)、5-フルオロウラシル(5-FU)、ヒト肝細胞腫(HepG2)、ペニシリン-ストレプトマイシン溶液およびウシ胎児血清(FBS)は、Dalian Meilun Biotechnology Co.、Ltd。から購入しました。硫酸(H 2 SO 4 98%)および過マンガン酸カリウム(KMnO 4 )Nanjing Chemical Reagent Co.、Ltd。から購入しました。硝酸ナトリウム(NaNO 3 )およびドデシル硫酸ナトリウム(SDS-Na)はShanghai Jinjinle Industrial Co.、Ltd。から購入しました。 MTTはSigma-Aldrich、Incから購入しました。 DMEMはHyClone、Incから購入しました。ラットは本渓長生実験動物センターから購入した。他のすべての試薬と化学物質は分析的に純粋で、市販されていました。
GO合成
GOは、修正されたHummerの方法に従ってグラファイト粉末から調製されました。まず、温度計付きの氷浴に置いた3つ口フラスコのフラスコ壁に沿って168 mLの98%硫酸を加え、温度が5°Cに達したときに5gのグラファイトと4gの硝酸ナトリウムを加えました。次に、22.5 gの過マンガン酸カリウムを1時間バッチでゆっくりと加え、温度を5°C未満に保ちました。その後、三口フラスコを油浴に移し、得られた混合物を35℃で30分間反応させた後、温度を65℃に上げ、反応物を30分間撹拌した。このステップに続いて、温度を85℃に上げ、混合物をさらに1時間反応させて、紫褐色のペーストを得た。この混合物を1週間部屋に置いたままにし、700 mLの熱湯を入れたビーカーに移し、黄褐色になるまで30%過酸化水素を滴下しました。混合物を10,000rpmで遠心分離し、熱水で洗浄し、このプロセスを上澄みのpHが7.0になるまで数回繰り返しました。最後に、生成物を真空凍結乾燥機で乾燥させ、nanoGOを得た。
Tau-GO合成
正確に秤量した50mgのGOを50mLの蒸留水に溶解し、150mgのEDCと100mgのNHSを加えて、氷水浴で20分間超音波処理してGOを活性化しました。次に、10 mLのタウ水溶液(0.1 g / mL)を準備したGO水溶液にゆっくりと(滴下して)加え、HClでpHを6〜7に調整し、暗所で24時間連続して攪拌しました。 5000 rpmで10分間遠心分離して生成物を収集し、蒸留水で3回洗浄しました。 Tau-GOは凍結乾燥後に収集されました。
5-FUの読み込み
20mlのTau-GO溶液を2時間超音波処理しました。正確に秤量した5-FUを適量の蒸留水に溶解し、調製したTau-GO溶液に室温で攪拌しながらゆっくりと滴下し、30℃、暗所で1.5時間超音波処理しました。生成物を5000rpmで10分間、4°Cで遠心分離しました。下側の沈殿物を20mLの蒸留水で洗浄し、遠心分離(5000 rpmで10分間、4°C)し、このプロセスを3回繰り返しました。下層を凍結乾燥し、上澄みをビーカーに入れ、体積を秤量し、5-FUの濃度を1200HPLC(Agilent、USA)によって決定した。検出条件は次のとおりです。クロマトグラフィーカラム:C18(4.6×250 nm、5μm)。カラム温度:25°C;移動相:0.1%KH 2 PO 4 pH5.5の溶液;流量:1.0 mL / min;注入量:20μL;および測定波長:265nm。カプセル化率(EE)と薬物負荷効率(LE)は、次の式で求められました。
$$ \ begin {aligned} {\ text {EE}} \ left(\%\ right)&=\ frac {{M_ {1} --C_ {1} \ times L_ {1}}} {{M_ {1 }}} \ times 100 \%\\ {\ text {LE}} \ left(\%\ right)&=\ frac {{M_ {1} --C_ {1} \ times L_ {1}}} {{ 20C_ {0} + M_ {1} --C_ {1} \ times L_ {1}}} \ times 100 \%\\ \ end {aligned} $$5-FUの総投与量はM 1 として記録されました。 、遊離5-FUの濃度と体積をC 1 として記録しました。 およびL 1 、およびキャリア濃度はC 0 として記録されました 。
特性評価
準備されたナノコンポジットの特性を明らかにするために、フーリエ変換赤外(FT-IR)スペクトルを4000〜400 cm -1 でスキャンしました。 相互作用を確認するためにIRAffinity-1分光計(島津製作所、日本)で。 UV-vis吸収スペクトルは、UV-3600走査型分光光度計(島津製作所、日本)で記録されました。サンプルを蒸留水に溶解し、粒子サイズ、ゼータ電位、およびPDI値をNano-ZS 90 Nano装置(Malvern、UK)で取得しました。サンプルの形態は、JEM-2100透過型電子顕微鏡(TEM)(JEOL、日本)を使用して分析されました。熱重量分析(TGA)は、熱重量分析装置(NETZSCH、ドイツ)を使用して、窒素雰囲気下で0〜800°Cの加熱速度10°C /分で実行されました。サンプルのXRD測定は、銅CuKα放射線(λ)を使用してX線回折計(Bruker、ドイツ)によって実行されました。 =1.5406Å)2θ角度の広角で。 XPS測定は、単色化されたAl Karadiation(Thermo、America)を備えたOmicronESCAプローブを使用して実行されました。
インビトロ薬物放出
インビトロでの薬物放出は、pH 1.2(シミュレートされた胃環境)、pH 6.5(シミュレートされた肝臓癌細胞環境)、およびpH 7.4(シミュレートされた生理学的環境)、37°C(シミュレートされた体温)でそれぞれ実行されました。簡単に説明すると、15 mgの5-FU-Tau-GOを透析膜に入れ、pH 1.2、6.5、7.4の0.1%SDS-Naを含む50mLの緩衝液に浸しました。すべてのサンプルは、100 rpmの速度、37°Cの温度で連続振とう水浴に入れられました。所定の時点(0分、5分、10分、20分、30分、1時間、1.5時間、2時間、2.5時間、3時間、4時間、8時間、12時間、24時間、48時間、 72時間)、各サンプルの1 mLを採取し、0.1%SDS-Naを含む1 mLの新鮮な緩衝液と交換して、同じ量の放出媒体を維持しました。放出された培地を遠心分離し、1200HPLCを使用して分析しました。
インビトロ細胞毒性研究
MTTアッセイ
MTTアッセイは、5-FU、Tau-GO、および5-FU-Tau-GOの細胞毒性を評価するために使用されました。簡単に説明すると、ヒト肝細胞癌HepG2細胞を、10%FBSと1%抗生物質(ペニシリン-ストレプトマイシン溶液)を添加したDEME培地で、37°C、5%CO 2 の加湿雰囲気で培養しました。 。細胞を96ウェルプレートに5×10 3 の密度で播種しました。 FBSと抗生物質を添加した100μLのDEME培地を含むウェルあたりの細胞数。プレートを5%CO 2 を含む37°Cの加湿チャンバーに24時間入れました。 。その後、増殖培地を除去し、さまざまな濃度(5、10、20、40、60、80、および100μg/ ml)の5-FU、Tau-GO、5-FU-を含む100μLの新鮮な培地を再充填しました。それぞれTau-GO。 24時間のインキュベーション後、細胞を20μLのMTT溶液で処理し、さらに4時間インキュベートしました。次に、培地を吸引し、ホルマザン結晶を150μLのDMSOに溶解しました。最後に、ウェルプレートを恒温発振器で37°Cで15分間振とうしました。各サンプルの光学密度(OD)は、マイクロプレートリーダーを使用して570nmで測定されました。実験は3回行った。細胞阻害率は、次の式を使用して結果から計算されました。
$$ {\ text {Cell}} \; {\ text {inhibition}} \; {\ text {rate}} =\ frac {{{\ text {OD}} _ {{{\ text {control}}} }-{\ text {OD}} _ {{{\ text {treatment}}}}}} {{{\ text {OD}} _ {{{\ text {control}}}}}} \ times 100 \ %$$ここで、OD control 未処理のコントロールセル、OD 処理によって得られた吸光度です。 処理された細胞によって得られた吸光度です。
AO / EB染色アッセイ
AO / EB二重染色を使用して、5-FU、Tau-GO、および5-FU-Tau-GOで処理した細胞の形態学的変化を評価しました。簡単に説明すると、対数増殖期のHepG2細胞を6ウェルプレートにウェルあたり10,000細胞の密度で播種し、37°C、5%CO 2 のインキュベーターで培養しました。 雰囲気。 24時間後、細胞を固定濃度の5-FU、Tau-GO、または5-FU-Tau-GOで処理し、さらに24時間インキュベートしました。各ウェルの培地を除去し、細胞をPBSで2回洗浄した。次に、40μLの蛍光色素(1 mg / mLAOと1mg / mL EBを1:1の比率で混合)を添加した1 mL PBSを各ウェルに添加し、光を当てずに10分間インキュベートしました。染色された細胞を蛍光顕微鏡で観察し、ランダムに画像を撮影しました。
薬物動態研究
すべての動物実験は、動物保護倫理委員会によって策定された方針と原則に従って実施されました。体重230〜270 gの合計24匹の雄SDラットを、12時間絶食させ、薬物投与前にランダムに4つのグループに分けました。グループAとBには5-FUと5-FU-Tau-GO溶液を静脈内注射し、グループCとDにはそれぞれ経口5-FUと5-FU-Tau-GO溶液を投与しました。すべてのグループに20mg / kgの用量が投与されました。薬物投与後、血液サンプル(約0.5 mL)を特定の時点(15分、1時間、2時間、4時間、6時間、8時間、12時間、16時間、24時間、および48時間)で抗凝固チューブに収集しました。 h)。血漿サンプルは、7500 rpm、4°Cで10分間の遠心分離によって分離されました。次に、200μLの血漿と50 mg(NH 4 ) 2 SO 4 チューブにまとめました(10μLの40μg/ mL5-BrU内部標準溶液、40°Cのウォーターバスで窒素を用いてブロー乾燥し、5分間ボルテックスし、10800 rpmで3分間遠心分離しました。次に、チューブを900μLの酢酸エチル/イソプロパノール溶液(85:15、v / v)を加え、3分間ボルテックスし、10800 rpmで15分間遠心分離しました。上澄みを取り除き、窒素で乾燥させ、100μLの移動相を加え、チューブを1分間ボルテックスしました。最後に、上澄みから採取した溶液を1200HPLCで測定しました。
分子動力学のシミュレーション
分子動力学シミュレーションは、主に薬物と担体の間の相互作用力と薬物の拡散挙動を分析するために使用されます。 5-FUの化学構造は、Chemdraw of chem office 2014を使用して構築され、Tau-GOおよびGOの構造は、Materials Studio分子シミュレーションソフトウェア(バージョン7.0、Accelrys Inc. 、 米国)。構築されたすべての化合物は、COMPASS II力場の下で幾何学的に最適化され、最も低いエネルギーのコンフォメーションが安定したコンフォメーションとして選択されました。各システムに対して10psのNVT平衡化が実行されました。シミュレーションは100ps MDで実行され、298Kと101.325kPaで1fsのステップサイズでバランスの取れた構造が得られました。最後に、各システムの平均二乗ゆらぎ(MSD)と凝集エネルギー密度(CED)を取得し、拡散係数(D)を次の式で求めました。
$$ D =\ frac {1} {2d} \ mathop {\ lim} \ Limits _ {\ tau \ to \ infty} \ frac {{\ text {d}}} {{{\ text {d}} \ tau }} \ left [{\ left。 {r \ overrightarrow {\ left(t \ right)}-r \ overrightarrow {\ left(0 \ right)}} \ right]} \ right。^ {2} $$
ここで、 d はシステムの次元であり、\(r \ overrightarrow {\ left(t \ right)} \)と\(r \ overrightarrow {\ left(0 \ right)} \)は時間
結果と考察
特性評価
タウ-GOコンジュゲートは、GOとタウのアミド結合によって作製されました。ナノコンポジットの合成が成功したことは、FT-IRスペクトルによって検証されました(図1)。 GOでの酸素官能基の存在は、–OH(〜3405 cm -1 )の吸光度ピークによって確認されました。 )、C =O(1723 cm -1 )、C =C(1628 cm -1 )およびC–OH(1391 cm -1 )。これらの結果は、GOの準備が成功したことを証明しました(図1a)[25]。いくつかのGO特性ピークに加えて、1638 cm -1 の新しいピーク および3427cm -1 アミド基に対応し、1164 cm -1 および1085cm -1 –SOに対応します。 Tau-GOスペクトルは、TauがGO表面で機能化されていることを明確に示しています(図1b)。図2bでは、–SO 3 の特徴的なピーク 1164 cm -1 水素結合の作用によって圧倒され、FT-IRスペクトルでは見えませんでした。したがって、5-FUはTau-GOに正常にロードされました。
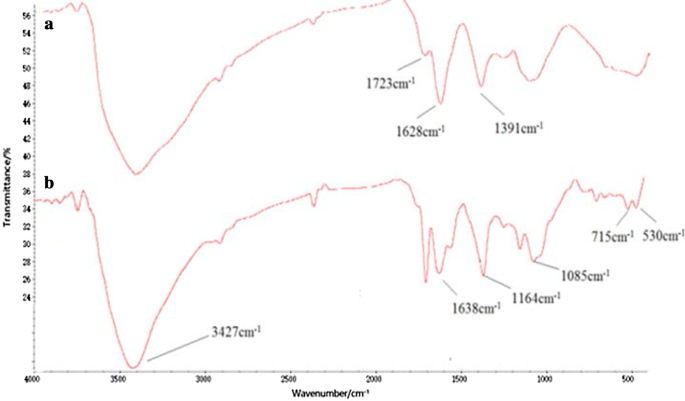
GOのFT-IRスペクトル( a )およびTau-GO( b )
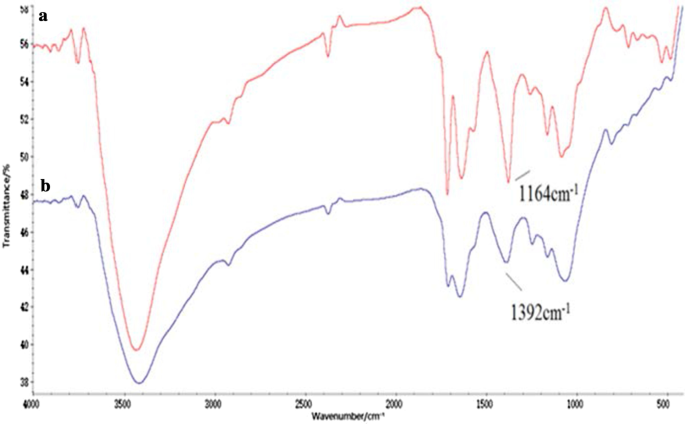
Tau-GOのFT-IRスペクトル( a )および5-FU-Tau-GO( b )
GO UV-Vis吸収スペクトルを図3に示します。234nmでの明らかな吸収ピークは、グラフェンC =C結合のπ–π *遷移に起因していました。さらに、300 nmのショルダーピークは、カルボキシル基またはカルボニル基の酸化グラフェンC =O結合のn–π *遷移に起因していました。 2つの特徴的な吸収ピークは、GOの準備に成功したことが証明されました。
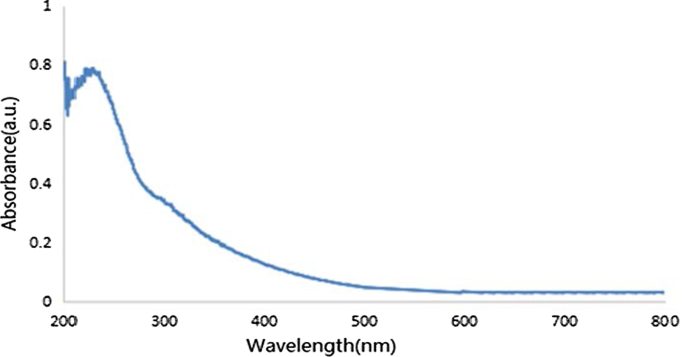
GOのUVスペクトル
GO、Tau-GO、5-FU-Tau-GOのサイズを図4に示します。GO、Tau-GO、5-FU-Tau-GOのゼータ電位を図5に示します。 GOシートは約221nm、PDI値は約0.188であり、準備されたGOが均一な分布と良好な安定性を持っていることを示しています。ゼータ電位は約− 33.3 mVであり、負電荷は主に表面に多くの酸素含有基が存在するためであることを示しています。 GOがアミド結合を介してタウで修飾された場合、アミノ基がいくつかのカルボキシル基と–SO 3 に置き換わりました 溶液中でのイオン化能力が強いほど、ゼータ電位は低下し、− 38.8mVになりました。 Tau-GOのサイズとPDI値は、約242nmと0.190でした。次に、5-FUを非共有結合でTau-GOにロードしました。ゼータ電位は約− 26.7 mVであり、絶対値は20mVを超えていました。また、5-FU-Tau-GOのサイズとPDI値は約264 nm、0.182であり、粒子間の静電反発力が大きく、凝集や析出が起こりにくく、タウの水溶性が良好であることを示しています。 、GOは、その表面が酸素含有官能基によって修飾されているため、水溶性も良好です。 Tau-GOキャリアを使用して5-FUをロードすると、5-FUの水溶性が大幅に向上するため、5-FU-Tau-GOを水溶液に安定して分散させることができます。
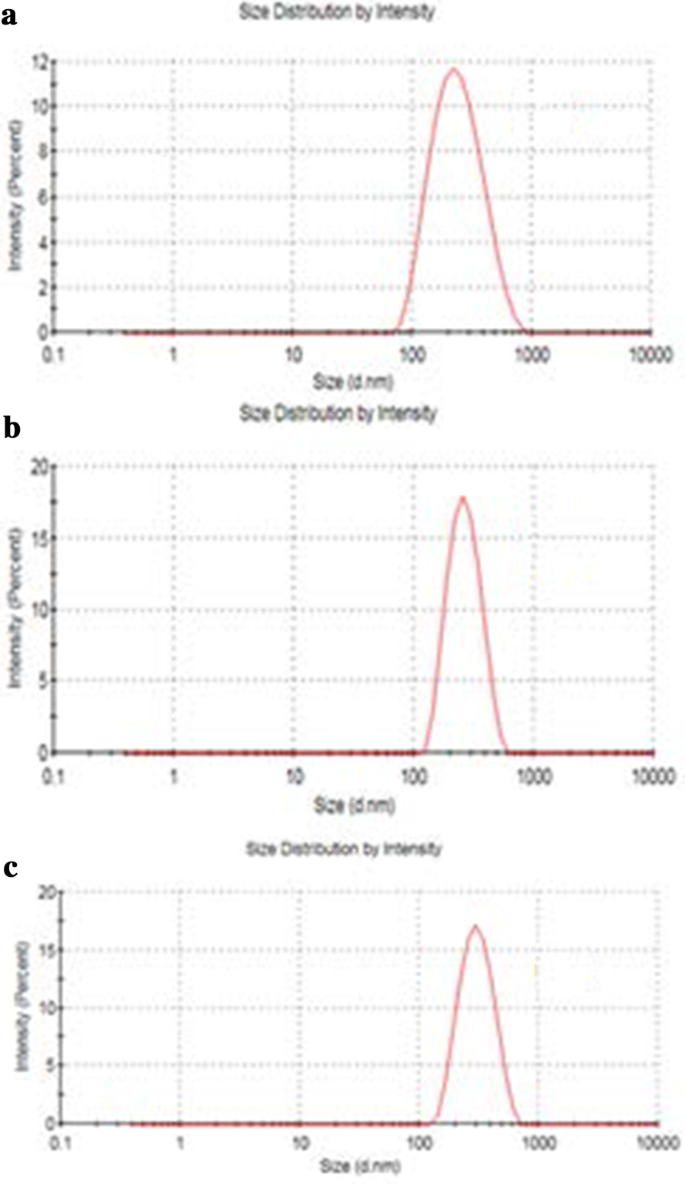
GOの粒子サイズ( a )、Tau-GO( b )、および5-FU-Tau-GO( c )
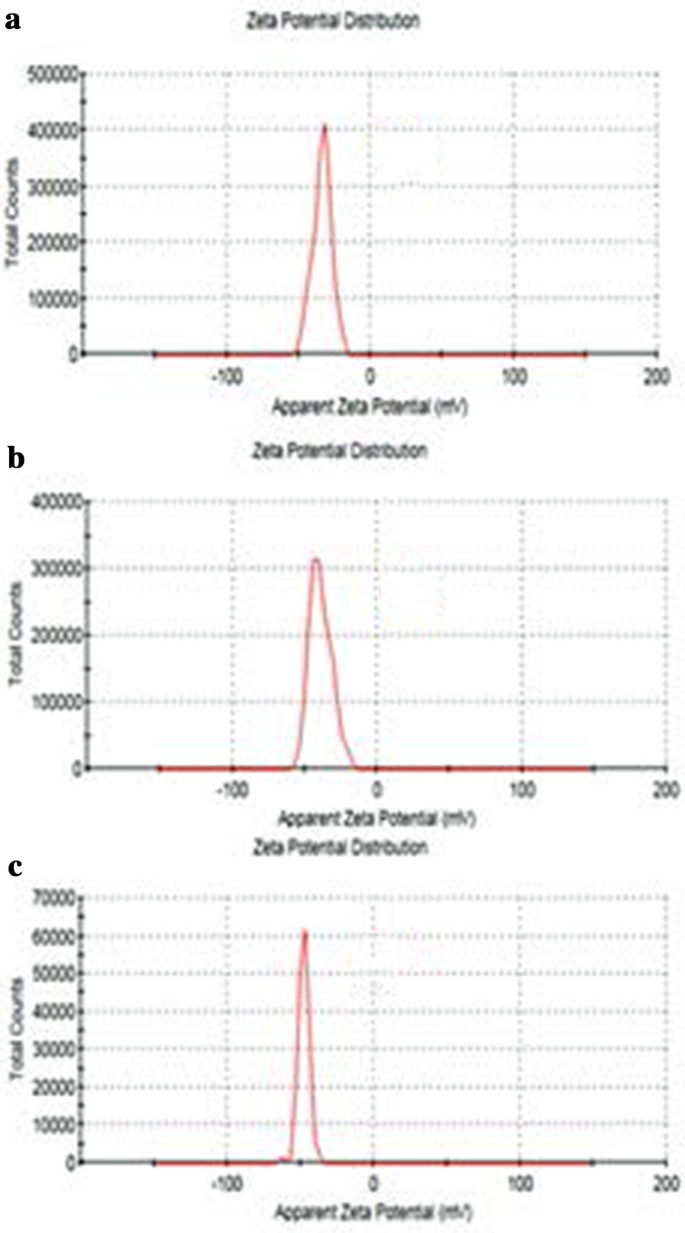
GOのゼータ電位( a )、Tau-GO( b )、および5-FU-Tau-GO( c )
GO、Tau-GO、5-FU-Tau-GOの形態は、TEMによって特徴づけられました(図6)。 GOは、表面にしわのある平らな構造であり、平面の2次元構造であることを示しています(図6a)。 GOと比較すると、Tau-GOのサイズはわずかに大きくなっていますが、それでもラメラ構造を示しています(図6b)。 5-FU-Tau-GO画像は、GOの初期の層状構造が無傷のままで、材料が凝集または変化していないことを示しています(図6c)。その結果、Tau-GOと5-FU-Tau-GOの安定性は良好でした。

GOのTEM( a )、Tau-GO( b )および5-FU-Tau-GO( c )
熱重量分析を使用して、複合材料の組成を定量化しました。 GOとTau-GOのTGA曲線を図7に示します。GOとTau-GOの残留質量は、800°Cの窒素雰囲気で39.73%と34.22%です。したがって、重量変化値を比較すると、Tau-GOのTauの含有量は約13%であると判断されました。
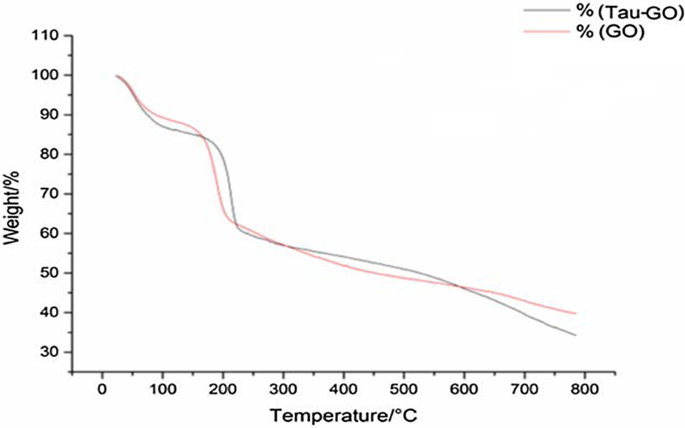
GOとTau-GOのタグ
タウ、GO、タウ-GOのXRDパターンを図8に示します。GOの特徴的なピークは2θ値の10.7°で観察できます。これは、強力な化学酸化および剥離プロセスのための完全な酸化を伴うGOの形成を確認します。 。 GO表面でタウで官能化した後、ピークの回折パターンは2θ値8.2でわずかに減少しました。これは、GOがTauによって正常に機能化されたことを意味します。
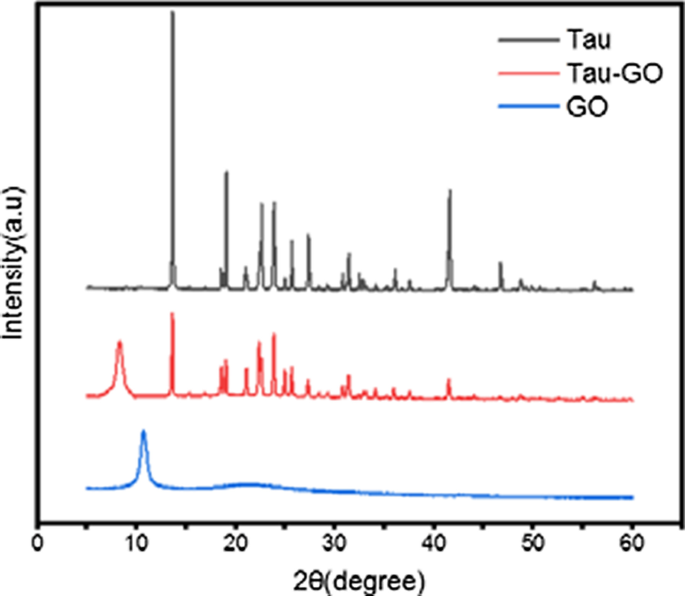
タウ、タウ-GO、GOのXRDパターン
GOおよびTau-GOのC1sXPSスペクトルを図9に示します。GOのC1sXPSスペクトルは、異なる官能基に対応する4つの炭素原子が存在し、かなりの程度の酸化があることを示しています。 Tau-GOのC1sXPSスペクトルも、これらの同じ炭素原子を示しています。さらに、C-N結合に関連する成分のピークの出現は、アミノ基、アミド基に起因していました。これらの結果は、GOがTauによって正常に機能化されていることも示しています。
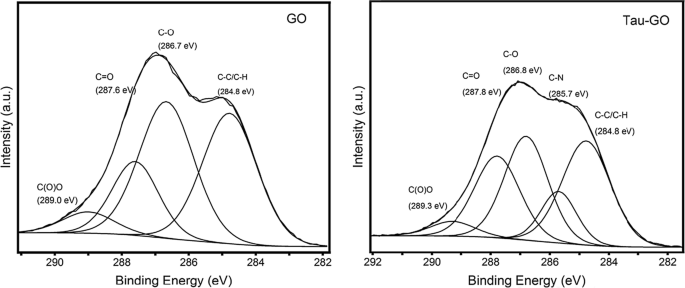
GOおよびTau-GOのC1sXPSパターン
薬物のロードとリリースの動作
5-FUは、非共有相互作用を介してTau-GOナノキャリアに吸着されました。 5-FUの検量線は y でした =62.135 x + 21.873( r =0.9999)、範囲は6.5〜250 µg / mLでした。カプセル化率(EE)と薬物負荷効率(LE)は、薬物負荷性能を評価するために、非結合薬物濃度によって決定されました。その結果、薬物濃度の増加に伴いEEが増加し、EEの最高値は83.2%であった。式によると、LEは33.7%でした。つまり、508.52μgの5-FUを1mgのTau-GOに吸着させることができます。したがって、Tau-GOは、大きな薬剤負荷を達成できる有望な薬剤キャリアです。 Tau-GOへの5-FUの高い負荷容量の考えられるメカニズムは、次の説明によって要約できます。まず、Tauを使用してGOを官能化し、活性官能基を導入します(–SO 3 )。 –SO 3 溶液中で強力なイオン化能力を持ち、GO間の凝集を減らし、Tau-GOへの5-FUのロードを容易にします。次に、5-FU-Tau-GOのゼータ電位はTau-GOのゼータ電位と12.1 mV異なります。これは、5-FUがTau-GOの表面にロードされ、静電相互作用が重要な役割を果たしていることを示しています。 5-FUのローディング。最後に、5-FUとTau-GOキャリアの間には、Tau-GOの-COOHと5-FUの-NH-、Tau-GOの-COOH、5-FU C =Oなど、さまざまな形の水素結合があります。 、–OHはTau-GO、–NH–は5-FU、–OHはTau-GO、–C =Oは5-FU、–COOHと5-FUはTau-GO –FはTau-GO、– Tau-GOのCOOHと5-FUの–F、これらの水素結合により、5-FU-Tau-GOは溶液中で安定します。
pH 1.2、6.5、および7.4のPBS溶液中の37°Cの温度での5-FU-Tau-GOからの5-FUのin vitro累積放出(それぞれ胃環境、肝癌細胞環境、および生理学的環境をシミュレート)を図10に示します。5-FUの放出挙動は、環境のpH値の影響を受けていることがわかります。 pH 7.4の緩衝液では、薬物の放出はゆっくりと継続的であり、72時間後の薬物の総放出量は約70.84%でした。対照的に、pH 7.4での薬物の放出量は、同じ時点でpH1.2およびpH6.5での放出量よりも有意に低かった。 5-FU-Tau-GOから放出された総薬物負荷は、それぞれ約90.29%と85.75%、およびpH1.2とpH6.5で達成できました。これは、5-FUとTau-GOの間のπ-π相互作用と水素結合に起因する可能性があります。 pH値が低いほど、水素結合のプロトン化度が高くなります。したがって、水素結合強度はpH値によって制御され、5-FUが放出されました。このpH感受性ドラッグデリバリーシステムは、抗腫瘍薬において重要な役割を果たし、腫瘍細胞への薬物の放出を達成することができます。
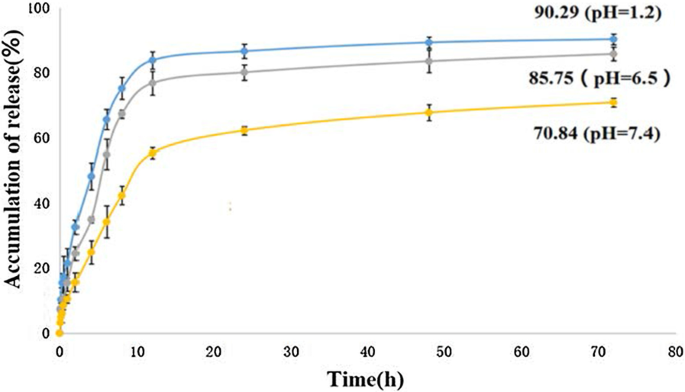
37°Cのリン酸緩衝生理食塩水中の5-FU-Tau-GOのinvitro放出曲線
インビトロ細胞毒性研究
ナノキャリアの潜在的な毒性と腫瘍治療効果を評価するために、MTTアッセイを使用してHepG2細胞でinvitro細胞生存率を実施しました(図11)。 Tau-GOは、さまざまな濃度で有意な細胞毒性を示しませんでした。 5-FUをロードした後、5-FU-Tau-GOは明らかな阻害効果を示したため、用量依存的に、ナノキャリアは抗腫瘍薬を送達する能力を持っていました。 IC 50 5-FU-Tau-GOの値は65.2±0.7μg/ mLであり、遊離の5-FU(196±8.73μg/ mL)よりも毒性が高かった。これは、腫瘍細胞にアポトーシスを誘導するタウリンの能力が原因である可能性があり、それによって細胞に対する5-FUの阻害効果が間接的に増強されます。さらに、in vitro放出実験から、Tau-GOにロードされた5-FUが細胞内で徐々に放出されることがわかりました。したがって、細胞に対する5-FU-Tau-GOの有効時間は、遊離の5-FUの有効時間よりも長く、より良い阻害をもたらしました。
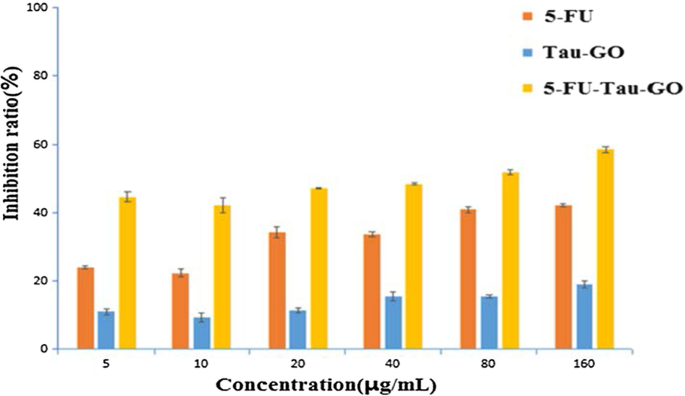
さまざまな濃度の5-FU、Tau-GO、および5-FU-Tau-GOの生存率
AO蛍光剤は、無傷の細胞膜と染色された核を通過したときに緑色の蛍光を発する可能性がありますが、EBは、赤/オレンジの蛍光を発する損傷した細胞の核のみをマークしました。初期および後期アポトーシスを伴う細胞は、それぞれAO / EB染色を伴う緑がかった黄色またはオレンジ色の核を示した。したがって、細胞形態学的変化の特徴を使用して、細胞死がアポトーシスと関連しているかどうかを調査するために、AO / EB染色を実施した。 AO / EB染色から得られた結果を図12に示します。対照細胞は紡錘形で、緑色の核を持っていました。 Tau-GOのみで培養した細胞群では、核のごく一部が陥入し、濃い緑色またはオレンジ色の赤色に染色されていました。クロマチン断片とアポトーシス小体を伴う有意なオレンジ色または赤色のアポトーシス細胞が、5-FU単独群で観察されました。 5-FUと比較して、5-FU-Tau-GOはHepG2細胞の形態により多くの損傷を引き起こし、細胞を破壊するだけでなく、癌細胞に大量のアポトーシスを引き起こしました。写真からわかるように、5-FU-Tau-GOで処理されたほとんどすべての細胞は、形態学的変化、多数の細胞破片およびアポトーシス体を有しており、5-FU-Tau-GOナノドラッグがデリバリーシステムはHepG2細胞に良い殺傷効果をもたらしました。
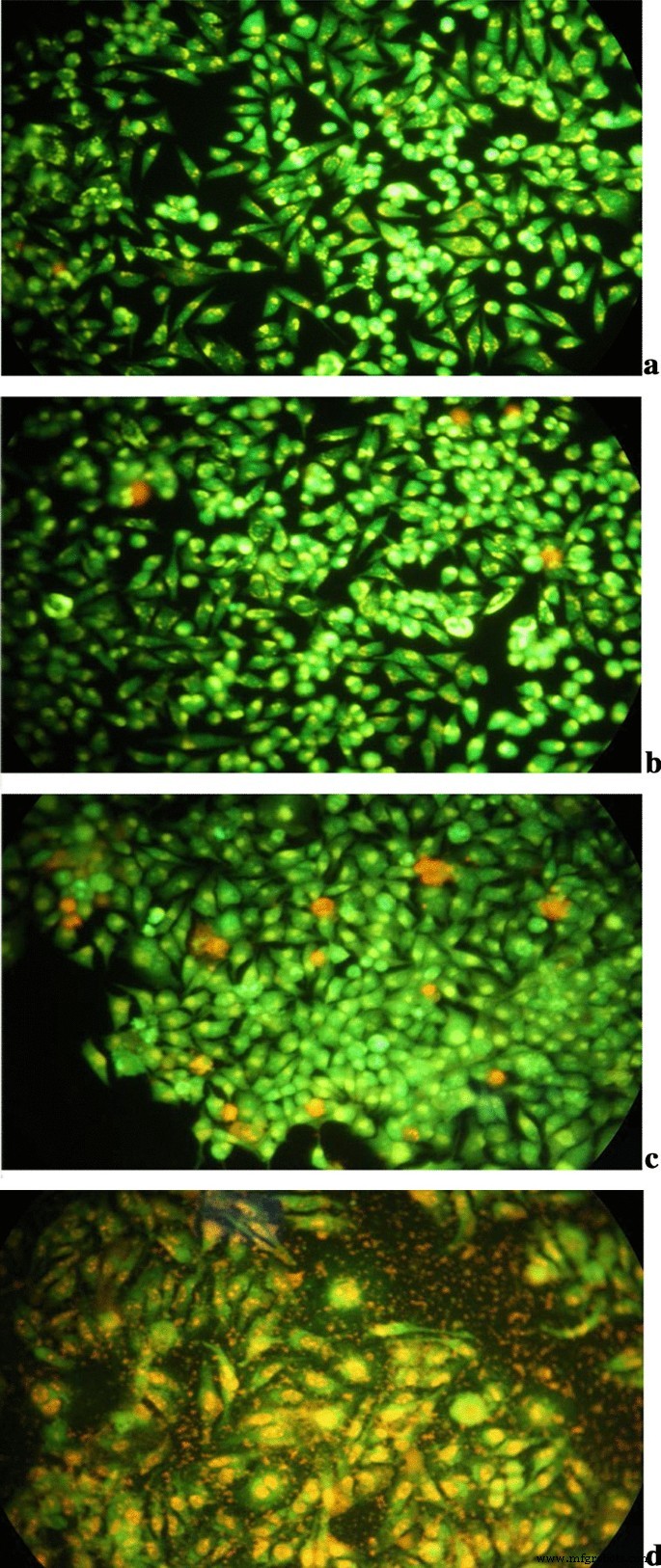
コントロールのAO / EB( a )、Tau-GO( b )、5-FU( c )、および5-FU-Tau-GO( d )
薬物動態研究
5-FUおよび5-FU-Tau-GOの薬物動態研究はSDラットで実施されました。経口投与後の血漿中の5-FU濃度と時間のプロファイルを図13aに示します。 2つの曲線の傾向は類似していることがわかりましたが、5-FU-Tau-GOナノキャリアからの5-FU血漿濃度は、5-FU単独からの血漿濃度よりも高く、これは各測定時点で観察されました。図13bは、尾静脈を介した5-FUのinvivo放出プロファイルを示しています。 5-FU-Tau-GOは、24時間にわたって持続的な薬物放出を達成でき、薬物濃度は最初の数時間で徐々に減少し、5-FUがゆっくりと放出されたことを示しています。
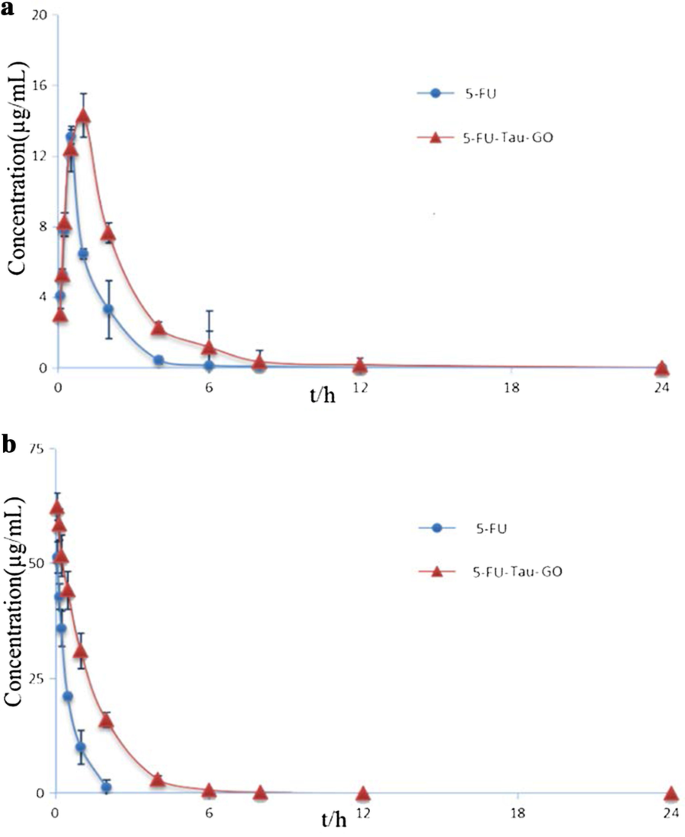
経口投与による5-FUおよび5-FU-Tau-GOのinvivo薬物動態標準曲線( a )。静脈内注射による5-FUおよび5-FU-Tau-GOのinvivo薬物動態標準曲線( b )
2コンパートメントモデルを使用して、ラットにおける経口または静脈内投与の薬物動態パラメーターを分析しました。薬物動態パラメータを表1に示します。5-FUと比較して、5-FU-Tau-GOはより高いT 1 /2βを示しました。 経口投与で2.3倍、静脈内注射で3.0倍でした。さらに、濃度時間曲線下の面積(AUC 0-t )5-FU-Tau-GOナノ複合体は、5-FU溶液と比較して、経口投与で約2.1倍、静脈内注射で2.8倍高かった。したがって、5-FU-Tau-GOはin vivoで5-FUの保持時間を大幅に延長し、バイオアベイラビリティを改善できると結論付けました。さらに、T 1 /2β 経口投与された5-FU-Tau-GOナノ複合体の(1.67±1.15 h)は、静脈内注射のそれ(1.33±0.64 h)よりも長かった。ただし、AUC 0-t 経口投与(36.02±1.83 mg / L * h)は静脈内注射(96.50±8.70 mg / L * h)よりも低かった。これらの結果は、2つの側面に起因する可能性があります。1つは、静脈内注射によって投与された場合、薬物は循環のために血液系に直接入り、再分配のために胃腸の障壁を通過しません。一方、5-FUは胃腸系に一定の損傷を与えやすいため、体内での薬物の効果的な使用にも影響を与える可能性があります。
<図>MDシミュレーション
未修飾のGO、Tau-GO、5-FUのドッキングと分子動力学は、分子ドッキングと分子動力学シミュレーションによってシミュレートされました。 GO、Tau-GO、5-FUの分子ドッキング結果を図14に示します。ここでは、5-FUとGOおよびTau-GOの結合長がそれぞれ3.66Åと2.602Åであることがわかります。 。さらに、計算結果から、GOおよびTau-GOへの5-FUの結合エネルギーは、それぞれ47.69 kcal / molおよび25.04kcal / molでした。これらは、タウ-GOおよび5-FUの結合力がGOおよび5-FUの結合力よりも強いことを示した。これは、SやNなどのタウ極性原子が5-FUとより強い非共有結合を形成し、タウ-GOと5-FUの間の力を強くするためです。
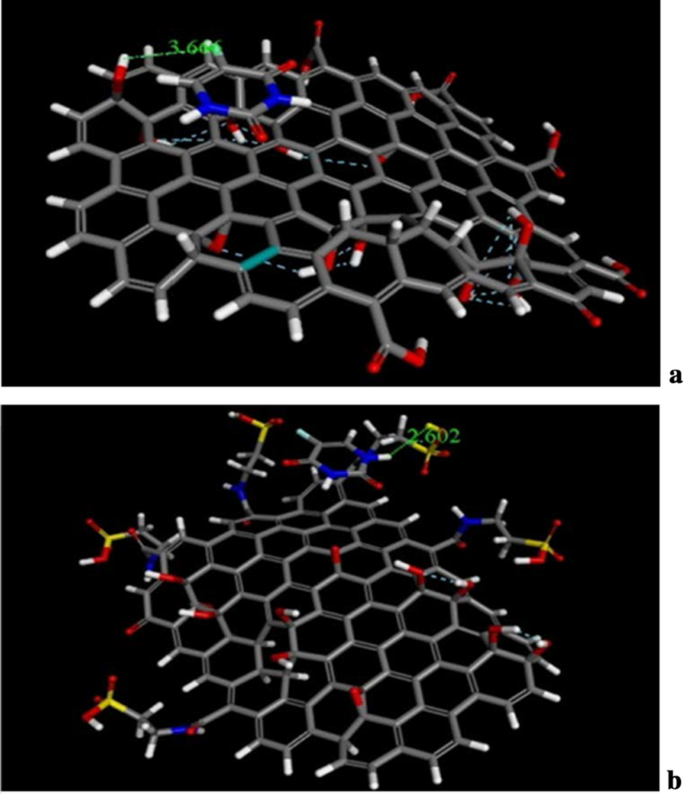
5-FUを使用したGOシートの分子ドッキング( a )。 Tau-GOと5-FUの分子ドッキング( b )
GO、Tau-GO、5-FUの分子動力学シミュレーションの図を図15に示しました。計算結果によると、5-FU-GOと5-FU-Tau-GOのCEDは2.67 * 10でした。 8 および2.83 * 10 8 、 それぞれ。これらの結果は、薬剤とTau-GOの間のより強い相互作用を示しました。 MSDと時間の間のグラフをプロットして(図16)、MSDを介して拡散係数を取得しました。薬物拡散係数は、次のように勾配を6で割って得られました:0.094m 2 / sおよび0.058m 2 / s。これらは、タウ-GOと5-FUの間の力がより強いことを示しており、これは分子ドッキングの結果と一致しています。したがって、機能化されたGOにより、キャリア全体の原子とグループがより豊富になります。したがって、5-FUとの非共有結合を強化し、システム全体をより安定させます。
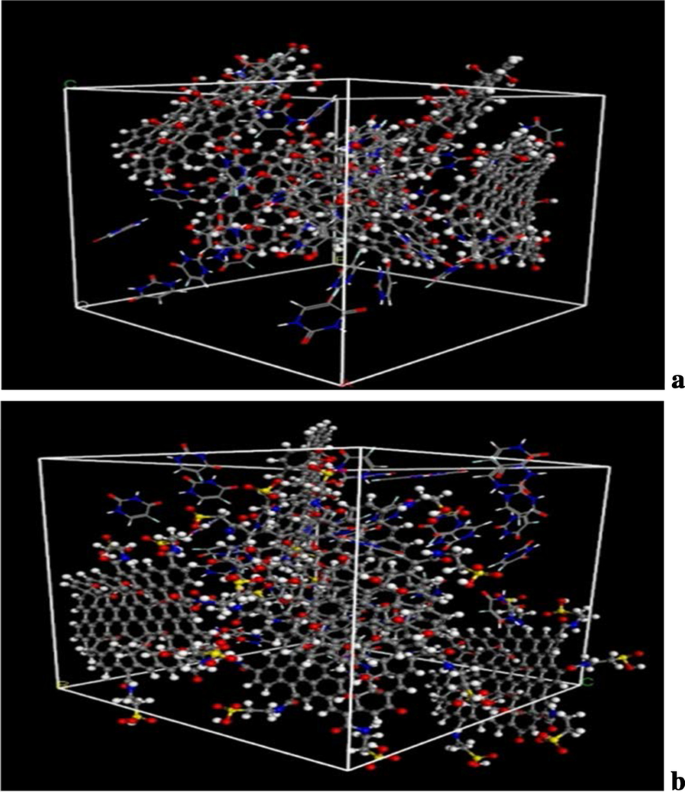
MDの最後にあるGOと5-FUのスナップショット( a )。 MDの最後にあるTau-GOと5-FUのスナップショット( b )
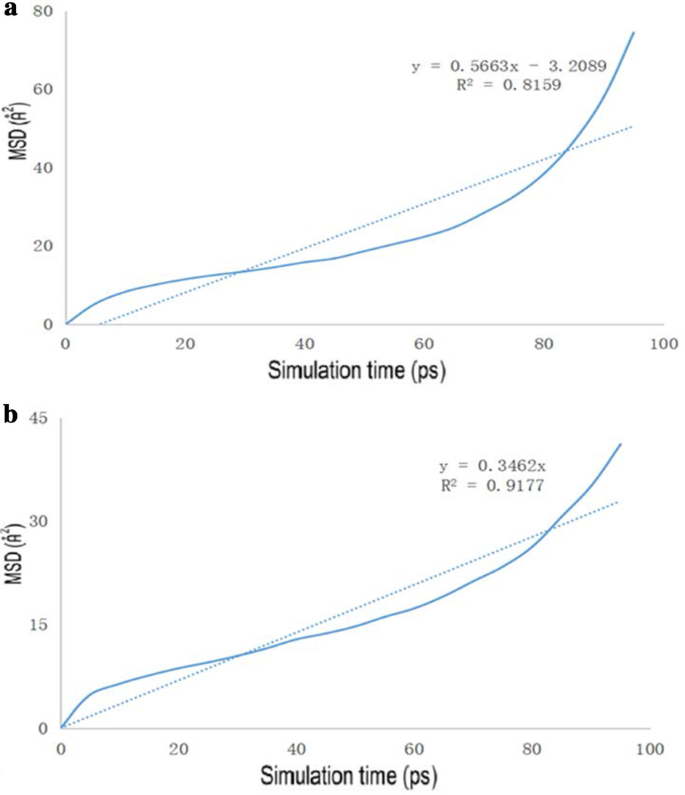
GOおよび5-FUの薬物MSDプロファイル( a )、Tau-GOおよび5-FU( b )
結論
要約すると、簡単な化学的方法でTau-GOナノコンポジットの調製に成功しました。タウによるGO機能化は安定性が高く、生体適合性が向上します。 Tau-GOナノキャリアのユニークな構造と優れた特性は、5-FUのロードとデリバリーに絶好の機会を提供します。 5-FU-Tau-GOは、潜在的な抗腫瘍能力と優れた薬剤循環時間を備えています。したがって、5-FUローディングのためのキャリアタウによるGOの変更は、抗癌剤の送達および抗腫瘍療法のための5-FU-Tau-GOナノドラッグデリバリーシステムを構築するための効果的かつ適用可能なツールであると信じています。 。
データと資料の可用性
現在の研究中に使用および/または分析されたデータセットは、合理的な要求に応じて対応する著者から入手できます。
略語
- GO:
-
酸化グラフェン
- タウ:
-
タウリン
- 5-FU:
-
5-フルオロウラシル
- 5-FU-Tau-GO:
-
タウリン官能化酸化グラフェンローディング5-フルオロウラシル
- EE:
-
カプセル化率
- LE:
-
薬物負荷効率
- FT-IR:
-
フーリエ変換赤外
- TEM:
-
透過型電子顕微鏡
- TGA:
-
熱重量分析
- MSD:
-
平均二乗ゆらぎ
- CED:
-
凝集エネルギー密度
ナノマテリアル
- ドラッグデリバリーを強化するためのナノファイバーとフィラメント
- 生体適合性FePO4ナノ粒子:ドラッグデリバリー、RNA安定化、および機能的活性
- チタン酸塩ナノチューブで装飾された酸化グラフェンナノコンポジット:調製、難燃性、および光分解
- invitroおよびinvivoでのグラフェンおよび酸化グラフェンのバイオセーフティおよび抗菌能力
- RGOと3次元グラフェンネットワークが高性能でTIMを共同修正
- 窒化処理を施したHfO2ベースのRRAMの伝導メカニズムと耐久性の向上
- 異なる粒子サイズのアベルメクチンナノデリバリーシステムの製造、特性評価、および生物活性
- スーパーキャパシター用途の電極としてのグラフェン/ WO3およびグラフェン/ CeOx構造の評価
- 高度に圧縮耐性のあるスーパーキャパシタ電極としての超弾性と高静電容量を備えたグラフェン/ポリアニリンエアロゲル
- ポリオール媒介プロセスによるZnOナノクリップの製造と特性評価
- 酸化グラフェンの低温還元:電気コンダクタンスと走査型ケルビンプローブフォース顕微鏡



