(La0.97RE0.01Yb0.02)層状硫酸ヒドロキシルから変換された2O2Sナノ蛍光体とアップコンバージョンフォトルミネッセンスの調査(RE =Ho、Er)
要約
フェーズピュア(La 0.97 RE 0.01 Yb 0.02 ) 2 O 2 Sアップコンバージョン(UC)ナノ蛍光体(平均結晶子サイズ〜45 nm、RE =Ho、Er)は、1200°Cで1時間、水蒸気を唯一の排気として、水素を流しながら熱水結晶化した層状硫酸ヒドロキシル前駆体からアニールしました。 978 nmのレーザー励起(最大2.0 W)では、Ho 3+ ドープされたリン光物質は、〜546( 5 )で緑(中)、赤(弱)、および近赤外線(強)の発光を示しました。 F 4 → 5 I 8 )、658( 5 F 7 → 5 I 8 )、および763 nm( 5 F 4 → 5 I 7 )、それぞれ、可視光領域(400〜700 nm)で約(0.30、0.66)の安定した色度座標を持っています。 Er 3+ 一方、ドープされたUCリン光物質は、弱い緑色を示しました(〜527 / 549 nm、 2 H 11/2 、 4 S 3/2 → 4 I 15/2 )、弱い赤(〜668 / 672 nm、 4 F 9/2 → 4 I 15/2 )、および強力な近赤外線(〜807 / 58 nm、 4 I 9/2 → 4 I 15/2 )発光。可視領域の発光色は、励起パワーの増加に伴い、黄緑色[(0.36、0.61)]から緑色[(0.32、0.64)]に変化しました。電力依存のUC発光の分析により、RE =HoとErのそれぞれ3光子プロセスと2光子プロセスが見つかり、可能なUCメカニズムが提案されました。
背景
アップコンバージョン(UC)リン光物質は、長波長の放射線を短波長の蛍光に変換する独自の能力により大きな注目を集めており[1、2]、ソリッドステートレーザー[3]、マルチカラーディスプレイ[3]の分野で幅広い用途が見出されています。 4]、薬物送達[5]、蛍光生物学的標識[6]、太陽電池用の波長変換器[7]など。 UCリン光物質は通常、ホスト格子に増感剤/活性剤のペアをドープすることによって形成されます。ここで、増感剤は通常Yb 3+ アクティベーターは頻繁にHo 3+ 、Er 3+ 、またはTm 3+ 。これは、Yb 3+ 980 nmの近赤外レーザー励起を効率的に吸収でき、3種類の活性剤は、連続的な光子吸収とエネルギー移動に有益なはしご状のエネルギーレベルを備えています[8]。ランタニドアップコンバージョンにおけるUC発光とエネルギー移動の基礎は、Auzel [9]とDongetal。による総説に記載されています。それぞれ[10]。 Gai etal。 [8]最近、ソフト化学合成、発光特性、生物医学的応用など、ダウンコンバージョン(DC)およびUCの目的で希土類マイクロ/ナノクリスタルで達成された最近の進歩をまとめました。王ら。 [11]一方、彼らの総説では、光学温度測定における希土類イオンをドープしたUCおよびDCリン光物質の応用について広く要約されています。 UCリン光物質の特性は、ホスト格子のタイプ、増感剤/活性剤の組み合わせ、ドーパント濃度、粒子/結晶子の形態、結晶化度、励起パワー、およびドーパントイオンが存在する実際の格子サイトによって大きく影響されます[8、9、10 、11、12、13]。たとえば、2つの非等価なGd活性化結晶学的部位がEr 3+ で特定されました。 ドープされた六角形のNa 1.5 Gd 1.5 F 6 リン光物質、および時間分解分光法により、 4 からの2つの炭酸ガス放出が証明されました。 S 3/2 Er 3+ のレベル Gd1(540 nm)およびNa2 / Gd2(550–555 nm)の結晶学的サイトから個別に発生し、 4 からの657nmの赤色発光 F 9/2 レベルはNa2 / Gd2サイトからのみ発生します[12]。小説Er 3+ の最近の研究 ドープされた透明なSr 0.69 La 0.31 F 2.31 一方、ガラスセラミックは、 2 の3つの熱結合エネルギーレベル(TCL)から、スペクトル分割、熱消光比、母集団の安定性、および温度感度を示しました。 H 11/2 / 4 S 3/2 、 4 F 9/2(1) / 4 F 9/2(2) 、および 4 I 9/2(1) / 4 I 9/2(2) は980nmレーザーの励起パワーに依存し、蛍光強度比と温度の関係を確立するために新しいフィッティング法が開発されました[13]。希土類(RE)ハロゲン化物(NaYF 4 など) :Yb / Er)は、フォノンエネルギーが低いため(ℏω<400 cm -1 )、現在最も効率的なUCリン光物質です。 )[8、10、11、14]、ただし、多くのハロゲン化物の合成と空気感受性に関与する有毒な原材料は、それらの適用と生産を制限します。広く研究されている別のタイプのUCリン光物質は、RE 2 です。 O 3 (Y 2 など O 3 :Yb / Er)、その比較的高いフォノンエネルギー(ℏω〜600cm -1 ; 〜591cm -1 Y 2 の場合 O 3 および612cm -1 Lu 2 の場合 O 3 )[15]ただし、光子-フォノン結合により、UC発光の効率が低下します。生体適合性の観点から、Li etal。 [16]合成されたYb 3+ -およびHo 3+ -水熱反応による共ドープフルオロアパタイト結晶(16 x 286 nmのナノロッド)、およびHo 3+ のUC発光 543および654nmは、980nmのレーザー励起下での2光子プロセスによって達成されました。表面に親水性デキストランをグラフトした後も、結晶は明確な蛍光細胞イメージングを示しました[16]。
RE 2 O 2 オキシ硫化物は、リン光物質分野における重要な化合物ファミリーであり、発光用途では酸化物よりも有利な場合があります。たとえば、S 2- の出現 →Eu 3+ Eu 3+ の電荷移動遷移 -アクティブ化されたRE 2 O 2 Sは、有効励起波長を約400 nmに大幅に拡張します[17、18、19]。これにより、Ye et al。がレビューしたように、リン光物質は近紫外線(365〜410 nm)励起白色LEDの赤色成分として有用になります。 [20]。 RE 2 を合成するための最も成熟した手法 O 2 Sは固相反応であり、高い収率と利便性という利点がありますが、高い反応温度、制御できない生成物の形態、特に環境に有害な硫黄源の使用は明らかな欠点です[21、22、23]。 RE 2 の硫化 O 3 H 2 による SまたはCS 2 高温のガス[24,25,26]は、RE 2 を生成するために頻繁に使用されるもう1つの戦略です。 O 2 S. RE 2 の制御された合成の方法論以来 O 3 豊富でよく発達している、RE 2 O 2 このように、さまざまな粒子形態のSが硫化ルートで製造されていますが、複雑な手順は工業生産には適していません。 RE 2 の他のテクニック O 2 S合成には、沈殿[27]、水熱反応[28]、2段階溶液ゲルポリマー熱分解[29]、ゼラチンテンプレート合成[30]、ゲル熱分解[31]、ソルボサーマル圧力解放合成[32]、および燃焼[33]。有害な硫黄源または副産物(C 2 など)の関与 S、H 2 S、およびチオ尿素)は、しかし、それでも避けるのは難しいです。硫酸塩型層状希土類水酸化物(RE 2 (OH) 4 SO 4 ∙2H 2 O、SO 4 2- -LREH)2010年[34]は、このグループの化合物のRE / Sモル比がRE 2 とまったく同じであるため、前述の問題を解決するユニークな機会を提供しました。 O 2 S. RE 2 の均一な加水分解 (SO 4 ) 3 ・8H 2 Na 2 の存在下でのO SO 4 およびヘキサメチレンテトラミン(C 6 H 12 N 4 )は、SO 4 を生成するための古典的な手法です。 2- -LREHですが、ランタニドファミリーではRE =Pr–Tbに制限されています[34]。 RE(NO 3 の水溶液を反応させることにより、化合物のグループをRE =La–Dyに拡張しました。 ) 3 ・ n H 2 Oおよび(NH 4 ) 2 SO 4 熱水条件下で[17、18、19]、その後RE 2 O 2 Sは、SO 4 の熱分解によって容易に生成できます。 2- -還元性雰囲気でのLREH [17、18、19]。 RE 2 O 2 Sは最近、フォノンエネルギーが比較的低いことが確認されました(ℏω〜500cm -1 )[1]、良好な化学的安定性、およびハロゲン化物に匹敵する特に高いUC効率[35、36]が、このタイプの有望なUCリン光物質に関する研究はまだ十分ではありません[8、10、11、37、38]。 La 3+ 空いている4 f はありません サブオービタルであり、光学的に不活性であるため、その化合物は発光に適したホスト格子です。このようにして、この作業でLa 2 を合成しました。 O 2 熱水結晶化したSO 4 のアニーリングによるS:Yb / RE UCリン光物質(RE =Ho、Er) 2- -流れるH 2 のLREH 、および発光特性とUCプロセスが詳細に説明されました。
メソッド
RE(NO 3 の出発材料 ) 3 ・6H 2 O(RE =La、Ho、Er、およびYb;> 99.99%純度)、(NH 4 ) 2 SO 4 (> 99.5%純度)、およびNH 3 ・h 2 O溶液(28%、超高純度)は関東化学株式会社(東京、日本)から購入し、受け取ったままの状態で使用しました。 Yb 3+ / Ho 3+ -およびYb 3+ / Er 3+ ドープされたLa 2 (OH) 4 SO 4 ・2H 2 Oは水熱反応により別々に合成された。 Yb 3+ のドーパント含有量は2at。%です。 Ho 3+ の両方で1at。% およびEr 3+ 文献[39]によると。典型的な合成[17]では、6ミリモルの(NH 4 ) 2 SO 4 希土類の水溶液60mlに溶解しました(総RE 3+ に対して0.1mol / L )、続いてNH 3 を滴下します。 ・h 2 pH =9になるまでO。15分間連続撹拌した後、得られた懸濁液を、100°Cに予熱した電気オーブンで24時間水熱結晶化するために容量100mlのテフロンで裏打ちしたオートクレーブに移しました。得られた生成物を遠心分離により収集し、濾過水で3回、エタノールで1回洗浄し、最後に空気中、70℃で24時間乾燥させた。 La 2 O 2 次に、S:Yb / REUCリン光物質をSO 4 からアニーリングしました。 2- -流れるH 2 のLREH前駆体 (200 mL / min)1200°Cで1時間、ランプ段階で5°C /分の加熱速度。
相の同定は、ニッケル濾過されたCu- K を使用して、40 kV / 40 mAでX線回折法(XRD;モデルRINT2200、リガク、東京、日本)を介して実行されました。 α線(λ=0.15406 nm)および1°/分のスキャン速度。製品の構造パラメータは、TOPASソフトウェアを使用してXRDデータから導出されました[40]。粒子形態は、10kVの加速電圧下で電界放出走査型電子顕微鏡(FE-SEM;モデルS-5000、日立、東京)によって観察された。 UC発光スペクトルは、FP-6500蛍光分光光度計(JASCO、東京)を使用して、連続波長(CW)レーザーダイオード(モデルKS3–12322-105、BWT北京)によるリン光物質の978nm近赤外レーザー励起下で室温で取得しました。 Ltd.、北京、中国)。分光計の信号/ノイズ比(S / N)は200以上であり、リン光物質の強いUC発光のために感度は低く設定されています。実験のセットアップは、追加ファイル1:図S1にあります。
結果と考察
図1は、熱水生成物のXRDパターンを示しています。いずれの場合も、すべての回折ピークは、La 2 の層状化合物で十分にインデックス化できることがわかります。 (OH) 4 SO 4 ・2H 2 O [17、18]。 SO 4 を含む水溶液中 2- 、希土類(RE)カチオンは、水和と部分加水分解を受けて、[RE(OH) x の錯イオンを形成します。 (H 2 O) y (SO 4 ) z ] 3- x -2 z [17、18、19]。より高い温度または溶液のpHは、RE 3+ を促進します 加水分解、より多くのOH - SO 4 は少ないですが 2- (小さいSO 4 2- / OH − 錯イオン中のモル比)。 100°CおよびpH =9 [17,18,19]の最適化された熱水条件下では、錯イオンは適切なSO 4 を持つ可能性があります。 2- / OH − モル比、したがって、目的のSO 4 2- -LREH化合物は、縮合反応によって結晶化することができます。熱水生成物の構造パラメータを表1にまとめています。(La 0.97 Ho 0.01 Yb 0.02 ) 2 (OH) 4 SO 4 ・2H 2 Oの格子定数は大きくなります( a 、 b 、 c )およびセルボリューム( V )より(La 0.97 Er 0.01 Yb 0.02 ) 2 (OH) 4 SO 4 ・2H 2 O. Ho 3+ を考慮すると、これは理解できます。 (CN =9の場合は1.072Å)はEr 3+ よりも大きい (CN =9の場合は1.062Å)。どちらの製品も、ドープされていないLa 2 よりもセル定数とセルボリュームが小さくなっています。 (OH) 4 SO 4 ・2H 2 O(SO 4 2- -LLaH)、La 3+ は、4種類のREイオンの中で最大(CN =9の場合は1.216Å)です。異なるセルパラメータは、固溶体形成の直接的な証拠を提供しました。
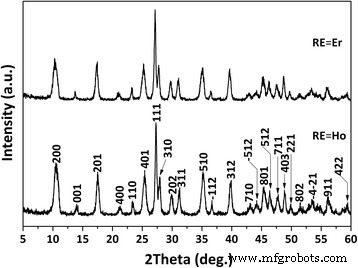
(La 0.97 のXRDパターン RE 0.01 Yb 0.02 ) 2 (OH) 4 SO 4 ・2H 2 100°CおよびpH =9で24時間の水熱反応によって得られたO層状化合物
図2は、SO 4 からアニーリングされた製品のXRDパターンを示しています。 2- -流れるH 2 で1200°Cで1時間のLREH前駆体 。回折ピークは、六角形の構造化されたLa 2 で完全にインデックス化できます。 O 2 いずれの場合もS(空間群: P- 3 m 1; JCPDSカード番号00-075-1930)。 SO 4 2- -LLaHはLa 2 に分解されます O 2 SO 4 La 2 の反応により、空気中で最大1200°C (OH) 4 SO 4 ・2H 2 O→La 2 (OH) 4 SO 4 + 2H 2 O(脱水)およびLa 2 (OH) 4 SO 4 →La 2 O 2 SO 4 + 2H 2 O(脱ヒドロキシル化)[17]。 H 2 で 雰囲気、S 6+ SO 4 で 2- S 2- に縮小されます La 2 の反応に続いて O 2 SO 4 + 4H 2 →La 2 O 2 S + 4H 2 O、したがってLa 2 O 2 Sは、唯一の副産物として水蒸気を伴う可能性があります[17]。 (La 0.97 の格子定数とセル体積 RE 0.01 Yb 0.02 ) 2 O 2 Sは、La 2 のSと一緒に表2に示されています。 O 2 S [17]。より小さなRE 3+ に向かって減少するセルの寸法 固溶体の形成が成功したことを示します。
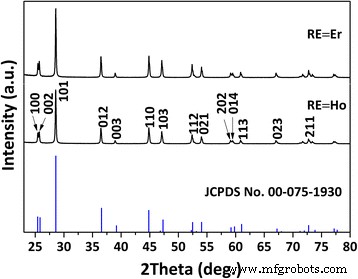
(La 0.97 のXRDパターン RE 0.01 Yb 0.02 ) 2 O 2 流れるH 2 で層状前駆体から焼成されたSアップコンバージョンリン光物質 (200 ml / min)1200°Cで1時間。 La 2 の標準回折 O 2 Sは比較用のバーとして含まれています
図3は、層状前駆体と得られたUCリン光物質の粒子形態を示しています。 SO 4 2- -LREHは、横方向のサイズが約150〜550 nm、厚さが約20〜30nmのナノプレートとして結晶化しました。ナノプレートは、1200°Cでの煆焼時にかなりの崩壊を受け、丸い粒子を生成しました。平均結晶子サイズは、シェラーの式を使用して、UCリン光物質で約45nmであると分析されました。

(La 0.97 のFE-SEM粒子形態 Ho 0.01 Yb 0.02 ) 2 (OH) 4 SO 4 ・2H 2 O( a )および(La 0.97 Er 0.01 Yb 0.02 ) 2 (OH) 4 SO 4 ・2H 2 O( b )層状前駆体と(La 0.97 Ho 0.01 Yb 0.02 ) 2 O 2 S( c )および(La 0.97 Er 0.01 Yb 0.02 ) 2 O 2 S( d )アップコンバージョンリン光物質
図4aは、(La 0.97 Ho 0.01 Yb 0.02 ) 2 O 2 978nmのレーザー励起下でのSリン光物質。 〜546、658、および763 nmでの発光は、 5 に起因します。 F 4 → 5 I 8 、 5 F 7 → 5 I 8 、および 5 F 4 → 5 I 7 Ho 3+ の遷移 、それぞれ[36]、763nmのNIR放射が支配的です。 Yb 3+ の増感効果 は重要であり、2 at。%Yb 3+ の同時ドーピングにより、それぞれ〜15倍および20倍強い緑色(546 nm)およびNIR(763 nm、人間の目に敏感ではない)放出が生成されました。 (追加ファイル1:図S2a)。 50 mWのレーザーポンピングでは、(La 0.97 Ho 0.01 Yb 0.02 ) 2 O 2 図4aの挿入図に示すように、肉眼でSリン光物質。励起パワーにもかかわらず、可視光領域(400〜700 nm)の発光スペクトルから計算されたCIE色座標は、鮮やかな緑色に典型的な約(0.30、0.66)で安定しています(追加ファイル1:表S1および図S3)。
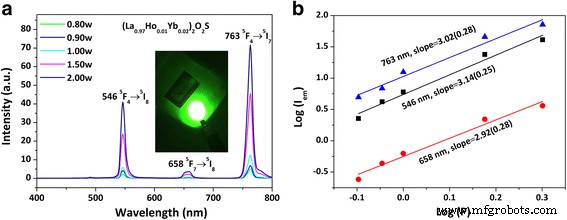
アップコンバージョン発光スペクトル( a )とlog( I em )およびlog( P )( b )(La 0.97 Ho 0.01 Yb 0.02 ) 2 O 2 Sリン光物質、ここで I em および P は、それぞれ発光強度と励起パワー(ワット単位)です。 a の挿入図 50mWの978nmレーザー励起下での強いUC発光の外観を示す写真です
一般に、不飽和条件下で上部発光状態を占めるのに必要な光子の数は、 I の関係から取得できます。 em ∝ P n [41]、ここで I は発光強度、 P ポンプ力、および n レーザー光子の数。図4bは、ログ( I em )-log( P )上記の関係のプロット、そこから n 線形フィッティングの傾きから、値は、UC排出量がそれぞれ約546、658、および763 nmでピークに達した場合に約3.02、3.14、および2.92(約3)であると決定されました。したがって、結果は、観察されたUC発光を生成するために3光子プロセスが関与したことを示唆しています。
原則として、3つの基本的な集団メカニズム、すなわち励起状態吸収(ESA)、エネルギー移動(ET)、および光子なだれがUCプロセスに関与している可能性があります[8、9、10]。この研究の範囲では電力閾値が観察されなかったため、光子なだれメカニズムは無視できます。 Yb 3+ のエネルギー図 / Ho 3+ La 2 で O 2 Sが報告されることはめったになく、比較することはできません。それにもかかわらず、3つのフォノンを含むUC発光は、Yb 3+ に関する以前の研究から見られました。 / Ho 3+ -共ドープされた他の材料システム[42、43]。したがって、(La 0.97 のエネルギー図とUCプロセス Ho 0.01 Yb 0.02 ) 2 O 2 Sは、これらの以前の研究を参照して図5に作成され、以下に詳しく説明されています。(1)Yb 3+ の励起 レーザー光子による[ESA; 2 F 7/2 (Yb 3+ )+ hν (978 nm)→ 2 F 5/2 (Yb 3+ )]; (2) 5 の人口 I 6 Ho 3+ のエネルギーレベル Yb 3+ の後 最初のレーザー光子を吸収し、エネルギーをHo 3+ に転送します [ET1; 2 F 5/2 (Yb 3+ )+ 5 I 8 (Ho 3+ )→ 2 F 7/2 (Yb 3+ )+ 5 I 6 (Ho 3+ )]; (3) 5 への非放射(NR)緩和 I 7 Ho 3+ のレベル [NR; 5 I 6 (Ho 3+ )〜 5 I 7 (Ho 3+ )]; (4)Ho 3+ の励起 5 から I 7 〜 5 F 5 Yb 3+ 後のレベル 2番目のレーザー光子を吸収し、エネルギーをHo 3+ に転送します [ET2; 2 F 5/2 (Yb 3+ )+ 5 I 7 (Ho 3+ )→ 2 F 7/2 (Yb 3+ )+ 5 F 5 (Ho 3+ )]; (5) 5 へのNR緩和 I 5 Ho 3+ のレベル [ 5 F 5 (Ho 3+ )〜 5 I 5 (Ho 3+ )]; (6)Ho 3+ の励起 5 から I 5 〜 5 F 4 / 5 S 2 Yb 3+ 後のレベル 3番目のレーザー光子を吸収し、エネルギーをHo 3+ に転送します [ET3; 2 F 5/2 (Yb 3+ )+ 5 I 5 (Ho 3+ )→ 2 F 7/2 (Yb 3+ )+ 5 F 4 / 5 S 2 (Ho 3+ )]; (7)ポピュレートされた 5 からの励起された電子のバックジャンプ F 4 / 5 S 2 5 のレベル I 8 緑の発光を生成する基底状態(〜546 nm; 5 F 4 、 5 S 2 → 5 I 8 )。電子は 5 まで緩和することもできます F 5 および 5 I 4 NRプロセスを介したレベル、そこから赤(〜658 nm; 5 F 5 → 5 I 8 )および近赤外線(〜763 nm; 5 I 4 → 5 I 8 )排出が発生しました。 〜763 nmでの強い近赤外UC発光は、 5 へのNR緩和を意味している可能性があります。 I 8 エネルギーレベルは重要です。
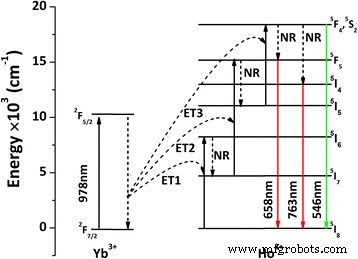
(La 0.97 のエネルギーレベルとUCプロセスの概略図 Ho 0.01 Yb 0.02 ) 2 O 2 Sリン光剤
2 F 5/2 → 2 F 7/2 Yb 3+ の発光遷移 および 4 I 15/2 → 4 I 11/2 Er 3+ の励起遷移 エネルギーがよく一致しているため、Yb 3+ / Er 3+ さまざまなタイプのホスト格子におけるUC発光について最も広く研究されている活性剤/増感剤のペア[8、9、10、11、12、13]。 Ho 3+ に似ています 、Er 3+ のUC放出 Yb 3+ によっても劇的に強化されました 同時ドーピング(追加ファイル1:図S2b)。 527 nmの緑色発光を例にとると、Yb 3+ の2at。% Er 3+ を改善しました 〜14倍の発光。978nmのレーザー励起下では、(La 0.97 Er 0.01 Yb 0.02 ) 2 O 2 S UCリン光物質は、緑(〜527および549 nm)、赤(〜668および672 nm)、および近赤外(〜807および858 nm)領域に発光バンドを示します(図6a)。 sup> 2 H 11/2 / 4 S 3/2 → 4 I 15/2 、 4 F 9/2 → 4 I 15/2 、および 4 I 9/2 → 4 I 15/2 Er 3+ の遷移 、それぞれ[32]。可視光領域(400〜700 nm)のUC発光について決定された色座標は、CIE色度図の黄緑色[(0.36、0.61)]領域から緑色[(0.32、0.64)]領域にドリフトしました。 0.7〜2.0 Wの励起電力(追加ファイル1:図S3bおよび表S2)。色の変化は、緑と赤の発光の強度比が徐々に大きくなることともよく一致します( I 549 / 私 668 および私 527 / 私 668 、追加ファイル1:表S3)より高い励起パワーで。 Yb 3+ の励起パワーに依存する発光色の調整 / Er 3+ ペアは以前にY 2 で観察されました O 2 S [44]。放出状態を生成するために必要なポンピングフォトンの数は、log( I )の傾きから導き出されました。 em )-log( P )プロット(図6b)、および排出量の3つのグループが同様の n を持っていることがわかりました 〜2の値。これは、2フォノンプロセスが観測されたUC発光の主な原因であることを示しています。
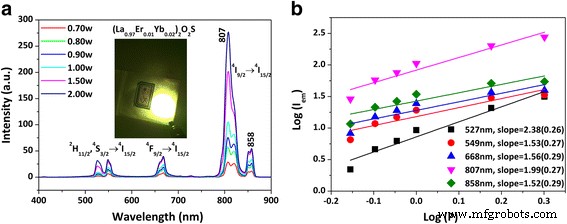
アップコンバージョン発光スペクトル( a )とlog( I em )およびlog( P )( b )(La 0.97 Er 0.01 Yb 0.02 ) 2 O 2 Sリン光物質、ここで I em および P は、それぞれ発光強度と励起パワー(ワット単位)です。 a の挿入図 (La 0.97 の強いUC発光を示す写真です Er 0.01 Yb 0.02 ) 2 O 2 50mW未満の978nmレーザー励起のS
(La 0.97 のUC発光につながるエネルギー図と光子過程 Er 0.01 Yb 0.02 ) 2 O 2 Sを図7に模式的に示します。励起状態の吸収とYb 3+ →Er 3+ エネルギー伝達励起は主にUCメカニズムに関与し、後者が支配的です[8,9,10,11,12,13,14、39,43]。 978 nmレーザーで励起すると、 2 F 7/2 Yb 3+ の基底状態の電子 2 にポンプで送られます F 5/2 励起状態(ESA)。 2 以降 F 5/2 Yb 3+ のレベル および 4 I 11/2 Er 3+ のレベル Yb 3+ からのエネルギー伝達は、互いによく一致しています。 Er 3+ へ すぐに行われます。 Er 3+ したがって、電子は 4 から励起できます。 I 15/2 4 への基底状態 I 11/2 Yb 3+ から伝達されたエネルギーと同じレベル (1光子、ET1)。 Er 3+ の吸収断面積 Yb 3+ よりも小さい 〜980 nm [42、45]であるため、エネルギー伝達(ET)がEr 3+ の実際の励起を支配します。 。 4 での励起エネルギー I 11/2 レベルは非放射(NR)で 4 に緩和される場合があります I 13/2 レベル。そこから電子を 4 に励起できます。 F 7/2 2番目のレーザー光子(ET2)のETによる状態。 NRプロセスの後、3つのグループの放出(図6a)は、図7に示す電子遷移を介して生成できます。UCプロセス全体の光子反応は、次のように表すことができます。(1) 2 F 7/2 (Yb 3+ )+ hν (978 nm)→ 2 F 5/2 (Yb 3+ )および 4 I 15/2 (Er 3+ )+ h ν(978 nm)→ 4 I 11/2 (Er 3+ ); (2) 2 F 5/2 (Yb 3+ )+ 4 I 15/2 (Er 3+ )→ 2 F 7/2 (Yb 3+ )+ 4 I 11/2 (Er 3+ ); (3) 4 I 11/2 (Er 3+ )〜 4 I 13/2 (Er 3+ ); (4) 2 F 5/2 (Yb 3+ )+ 4 I 13/2 (Er 3+ )→ 2 F 7/2 (Yb 3+ )+ 4 F 7/2 (Er 3+ ); (5) 4 F 7/2 (Er 3+ )〜 2 H 11/2 / 4 S 3/2 (Er 3+ )、 4 F 9/2 (Er 3+ )、および 4 I 9/2 (Er 3+ );および(6) 2 H 11/2 / 4 S 3/2 (Er 3+ )→ 4 I 15/2 (Er 3+ )+ hν (〜527および549 nm)、 4 F 9/2 (Er 3+ )→ 4 I 15/2 (Er 3+ )+ hν (〜668および672 nm)、および 4 I 9/2 (Er 3+ )→ 4 I 15/2 (Er 3+ )+ hν (〜807および858 nm)。前述の発光色の変化は、 4 のより効率的な集団を示唆している可能性があります F 7/2 (Er 3+ )より高い励起パワーの下でのエネルギーレベル、および 4 F 7/2 (Er 3+ )〜 2 H 11/2 / 4 S 3/2 (Er 3+ )NRプロセスは 4 よりも連続的に強くなります F 7/2 (Er 3+ )〜 4 F 9/2 (Er 3+ 。
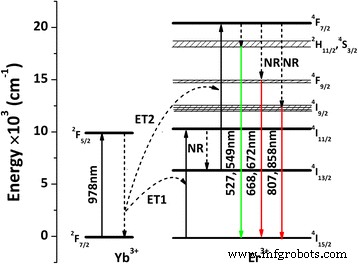
(La 0.97 のエネルギーレベルとUCプロセスの概略図 Er 0.01 Yb 0.02 ) 2 O 2 Sリン光剤
結論
(La 0.97 RE 0.01 Yb 0.02 ) 2 O 2 Sアップコンバージョン(UC)ナノ蛍光体(RE =Ho、Er)は、流れるH 2 で層状の硫酸ヒドロキシル前駆体を熱分解することで正常に生成されました。 1200°Cで、唯一の排気として水蒸気を使用します。前駆体は、横方向のサイズが〜150〜550 nm、厚さが〜20〜30 nmのナノプレートとして結晶化し、熱分解すると丸いナノ粒子(平均結晶子サイズ:〜45 nm)に崩壊しました。オキシ硫化物リン光物質は、Ho 3+ の3光子プロセスにより、978nmのレーザー励起下で強いUC発光を示します。 Er 3+ の2光子プロセス 。可視領域(400〜700 nm)のUC発光の場合、色度座標は(La 0.97 Ho 0.01 Yb 0.02 ) 2 O 2 Sは(0.30、0.66)付近で安定していますが、(La 0.97 Er 0.01 Yb 0.02 ) 2 O 2 Sは約(0.36、0.61)から(0.32、0.64)に変化し、励起電力は0.7から2Wに増加しました。
ナノマテリアル
- 表面および層間の修飾による油中の層状リン酸ジルコニウムナノプレートレットのトライボロジー性能の調整
- パラジウム(II)イオンインプリント高分子ナノスフェアの調製と水溶液からのパラジウム(II)の除去
- 修飾BiOClの合成と特性評価および水溶液からの低濃度染料の吸着におけるそれらの応用
- 層状グラフェンおよびh-BNフレークにおけるラマン活性面内E2gフォノンの温度依存性
- 金および銀ナノ粒子のグリーン合成のためのPlatycodiRadix(Platycodon grandiflorum)からのPlatycodonサポニン
- 湿度にさらされた状態でのCH3NH3PbI3ペロブスカイトマイクロワイヤーのフォトルミネッセンス、ラマン、および構造の進化
- メタマテリアルの複数の磁気双極子共鳴からの光周波数での単層グラフェンのマルチバンドおよびブロードバンド吸収増強
- エレクトロスピニングとその場熱分解に由来する高活性で安定なFe-N-C酸素還元電極触媒
- 高度なナトリウムイオン電池のアノード材料としてのCuGeO3ナノワイヤの合成と調査
- InGaAs / InPコアシェルナノワイヤの自己シードMOCVD成長と劇的に増強されたフォトルミネッセンス
- PEG-PCCLナノ粒子の毒性評価とパクリタキセル負荷の抗腫瘍効果に関する予備調査



