MnFe2O4ナノ粒子で装飾された還元型酸化グラフェンによるテトラサイクリンの吸着
要約
ナノマテリアルは、テトラサイクリン汚染の環境修復のための効率的な吸着剤として広く使用されていました。ただし、吸着剤の分離は、それらの実際のアプリケーションに課題をもたらしました。この研究では、磁性MnFe 2 を成長させました O 4 MnFe 2 を形成するための還元型酸化グラフェン(rGO)上のナノ粒子 O 4 / rGOナノコンポジットとワンステップ方式。テトラサイクリンの吸収剤として使用した場合、41 mg / gの吸着容量を示しました。吸着速度論と等温線は、それぞれ疑似二次モデルとフロイントリッヒモデルによく適合しました。 MnFe 2 O 4 / rGOナノコンポジットは、外部磁場を使用して溶液から簡単に抽出し、酸洗浄で再生することができます。
はじめに
テトラサイクリン(TC)は、毒性が低く、広域スペクトルの活性があるため、世界で最も広く使用されている抗生物質の1つです[1]。しかし、近年、代謝によるTCの分解が少ないため、懸念が高まっています。その結果、残留TCは糞便を介して環境に直接排出され、近くの水域や水を含む土壌に拡散し、これらの地域の非点源汚染を引き起こします[1,2,3]。残留TCが人体に蓄積した後、慢性毒性を示します。一方、それは水生光合成生物と固有の微生物集団に影響を与える可能性があります[4、5]。 TC汚染水を処理するために、吸着は効率的で費用効果が高いため、有望な方法として浮上しています。吸着に使用される吸着剤には、スメクタイト粘土[6]、モンモリロナイト[7]、ジアトマイト[8]、活性炭[9]、アルミナ[10]、およびカーボンナノチューブ[11]が含まれます。最近では、TCとグラフェンベースの材料の間にπ-π相互作用、H結合、およびカチオン-π結合が存在するため、グラフェンベースのナノ材料が最も効果的な吸着剤として使用されています[12、13]。したがって、これらのナノ材料は、TCの高い吸着能力を示します。たとえば、吸着容量の理論上の最大値( q m )酸化グラフェンと還元型酸化グラフェンは、それぞれ313と558 mg / gに達する可能性があります[14、15]。グラフェンベースの複合材料は、さらに高い吸着能力を示します。 TiO 2 / GOコンポジットは q を示します m 1805 mg / gの値[16]。しかし、汚染された水からナノマテリアルに基づく吸収剤を分離することは、それらの実際の用途に挑戦をもたらします。吸収剤の分離を容易にするために、磁性吸収剤が使用された。私たちのグループは、チオール官能化マグネタイト/酸化グラフェンハイブリッドがHg 2+ の再利用可能な吸着剤として使用できることを実証しました。 除去[17]。チャンドラらヒ素除去に水分散性マグネタイト還元酸化グラフェン複合材料を利用しました[18]。この研究では、GOの形成にMnを利用して、磁性MnFe 2 を合成しました。 O 4 ワンポット方式の/ rGOコンポジット。 MnFe 2 O 4 吸着剤としての/ rGOは、初期TC濃度10 mg / Lで41mg / gという比較的高い吸着容量を示しました。磁性吸着剤は、外部磁場の助けを借りて水溶液から簡単に抽出でき、HCl水溶液に浸して再生した後に再利用できます。
材料と方法
GOの合成
GOは、修正されたHummerの方法で作成されました。簡単に言うと、H 2 SO 4 (75.0 ml、98 wt%)を1.0gのフレークグラファイトと0.75gのNaNO 3 を入れたフラスコにゆっくりと加えました。 氷水浴中で機械的に攪拌しながら。 10分後、4.5 g KMnO 4 フラスコに徐々に加えた。激しく攪拌し続けると、混合物はペースト状の茶色がかった色になり、次に脱イオン水で希釈した。 H 2 O 2 次に水溶液(20 ml、30 wt%)をゆっくりと混合物に加え、Mn 2+ とのGO混合物を形成しました。 イオン。
MnFe 2 の合成 O 4 / rGOコンポジット
MnFe 2 を合成しました O 4 以前に報告された/ rGOコンポジット[19]。簡単に説明すると、上記の混合物を脱イオン水でさらに3000mlに希釈しました。 FeCl 3 (9.237 g)を400 mlの脱イオン水に溶解し、混合物に加えた。アンモニア水溶液(30 wt%)を加えて、2時間でpHを10に調整しました。混合物を90℃に加熱した後、ヒドラジン水和物(98 wt%、30 ml)をゆっくりと加え、4時間撹拌して、黒色の懸濁液を得た。懸濁液を冷却し、磁石で分離し、脱イオン水とエタノールで数回洗浄し、最後に60℃の真空で乾燥させた。
MnFe 2 の特性評価 O 4 / rGOコンポジット
X線回折(XRD)分析は、CuKα放射線(40 kV、40 mA)を使用した回折計(Bruker D8 Discover)を使用して実施しました。サンプルの形態を透過型電子顕微鏡(TEM、JEOL 2100F)で観察した。この研究では、振動試料型磁力計(VSM 7410、レイクショア)を使用して、ナノコンポジットの磁気特性を分析しました。
TCの濃度の決定
恒温発振器(ZD-85A)を使用して、安定した制御可能な吸着プロセスを確保しました。原子吸光分光光度計(GTA 120、Agilent)を使用して、紫外線特性の吸収ピークを検出しました。 UV分光光度計(UV-1100、上海マパダ)を使用して、溶液の吸光度を測定することにより、溶液中のTC残留物の濃度を調査した。この研究に関与した他の機器には、pHメーター(PHS-3C)、乾燥オーブン(DHG-9240A)、超音波洗浄機(KQ5200E)、電子スケール(TP-214)などが含まれていました。線形検量線用にTC(10 mg / L)溶液を調製しました。図1aは、TCのUVスペクトルを示しています。の特徴的な吸着ピークは276nmと355nmです。この研究では、TC吸着の走査波長として355nmを選択しました。検量線を図1bに示しました。ランベルト・ベールの法則[20]によれば、溶液の吸光度を測定することにより、濃度を決定することができます。吸着容量( Q t 、mg / g)および吸着率( r )は式によって計算されます。 (1)と式。 (2)。
$$ {Q} _t =\ frac {\ left({C} _0- {C} _t \ right)\ times V} {m} $$(1)$$ \ mathrm {r} =\ frac {\ left ({\ mathrm {C}} _ 0-{\ mathrm {C}} _ {\ mathrm {t}} \ right)} {{\ mathrm {C}} _ 0} \ times 100 \%$$(2)<図> <画像>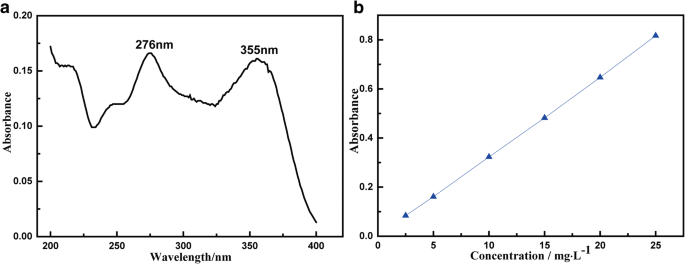
a UVスペクトルと( b )TCの濃度を測定するための校正済み曲線
ここで C 0 (mg / L)および C t (mg / L)は、最初と時間 t、での溶液中のTC残留物の濃度です。 それぞれ。 V(mL)は溶液の体積を表し、この研究では30 mLであり、m(g)はMnFe 2 の重量です。 O 4 / rGOサンプルを使用しました。
結果と考察
MnFe 2 の合成と特性評価 O 4 / rGO
MnFe 2 O 4 / rGOナノコンポジットは、報告されているようにワンポット法で合成されました。その過程で、精製せずに修正されたハマーの方法でGOを含む混合物を準備しました。後で、十分なH 2 O 2 水溶液を混合物に加えて、高原子価のMnイオンをMn 2+ に還元しました。 スラリー中。それらはFe 3+ と共沈しました アルカリ性環境でMnFe 2 を形成します O 4 N 2 の外観でグラフェンに還元されたGOナノシート上のナノ結晶 H 4 。 MnFe 2 O 4 / rGOナノコンポジットがついに形成されました。図2aは、ナノコンポジットのX線回折パターンを示しています。回折ピークは29.9、35.5、42.9、56.8、および62.3 o MnFe 2 の(220)、(311)、(400)、(511)、および(440)の平面に対応します。 O 4 キュービック相(JCPDSカード番号10-319)を使用。複合材料のラマンスペクトル(図2b)では、600 cm − 1 のピーク MnFe 2 の振動に関連していた O 4 他のピークは1351と1575cm -1 それぞれrGOのDバンドとGバンドでした[21、22]。 BET比表面積は42.7m 2 でした / g(追加ファイル1:図S1)。表面積が大きいのは、以下の理由による。合成プロセス中、GOナノシートは精製または乾燥せずに使用されました。一方、MnFe 2 O 4 ナノ粒子は核を形成し、それらの上で成長し、それらが積み重なるのを防ぎます。 rGOシートとMnFe 2 の重量比 O 4 MnFe 2 のコンポーネント O 4 –rGOナノコンポジットは、空気中の熱重量分析(追加ファイル1:図S2)によって、それぞれ約12%と88%と評価されました。ナノコンポジットのTEM画像(図2c)は、MnFe 2 O 4 30nm未満のサイズのナノ粒子がナノシートに装飾されました。ナノコンポジットの高分解能TEM画像(図2d)は、MnFe 2 の(220)面に対応する、0.29nmの面間距離を持つ明確な格子縞をさらに示しました。 O 4 立方相で。ナノコンポジットの磁気特性を磁力計で調べた。 MnFe 2 のヒステリシスループ O 4 25°Cでの/ rGOを図3aに示します。飽和磁化と残留磁化は、それぞれ22.6 emu / gと1.1emu / gと測定されました。飽和磁化が小さかったのは、マグネタイトのサイズが小さく、複合材料にGOが出現したためです。ナノコンポジットの保磁力は39.0Oeでした。室温での残留磁化と保磁力が小さい吸着剤は、小さな外部磁場でも引き付けられ、分離される可能性があります。実際、MnFe 2 O 4 水溶液に分散した/ rGOナノコンポジットは、図3bの光学画像で確認できるように、磁石を使用して水から簡単に抽出できました。
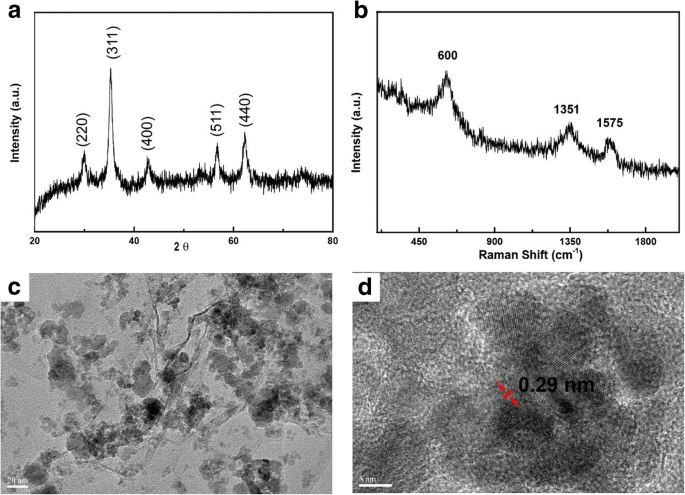
MnFe 2 の特性評価 O 4 / rGOナノコンポジット。 a XRDパターンと( b )ナノコンポジットのラマン分析; TEM画像( c )およびHRTEM画像( d )ナノコンポジットの
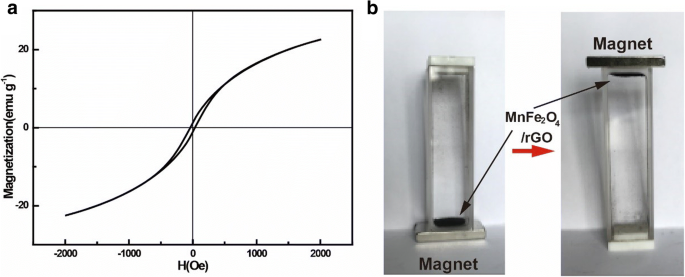
MnFe2O4 / rGOナノコンポジットの磁気特性。 a ヒステリシスループと( b )水からのナノコンポジットの磁気分離
MnFe 2 へのTCの吸着 O 4 / rGO
吸着速度を調べるために、MnFe 2 O 4 / rGO(5 mg)を25°Cの温度でTC溶液(10 mg / L)に添加して吸着させました。次に、十分な混合を確実にするために、溶液を温度一定の発振器に入れた。異なる時間にサンプルを採取し、分光光度計を使用してサンプルの吸光度を測定しました。検量線を比較することにより、吸着プロセス中の異なる時間での溶液中のTC濃度を決定することができます。図4は、それぞれTC吸着と吸着平衡に対する時間の影響を示しています。 MnFe 2 へのTCの吸着プロセス O 4 適度に速かった。 TCの濃度が最初の5時間で劇的に減少したことが示されました。その後、吸着プロセスが遅くなりました。約8時間の吸着後、TC溶液の濃度は安定しており、吸着が平衡に達したことを意味します。吸着速度は、純粋なGO分散液[14]よりも低速でしたが、磁性酸化グラフェンスポンジ[23]よりは高速でした。また、アルギン酸ナトリウム/ GOへのシプロフロキサシンの吸着よりもはるかに高速です。吸着速度は、GOのスタッキング構造と、TCがアクティブな吸着サイトに容易に拡散する方法に関連している可能性があります。図4bによると、吸着容量は41 mg / gと推定され、初期TC濃度は10 mg / Lでした。この値は、GO磁性粒子の値(39 mg / g)よりも少し高かった[24]。ここでは、吸着メカニズムの研究のために、疑似1次モデルと疑似2次モデルの2つの速度論モデルを適用しました。疑似一次動的方程式は、固液吸着システムをシミュレートするためによく使用され、式(1)に示す線形式を使用します。 (3)[25]:
$$ \ mathit {\ ln} \ left({q} _e- {q} _t \ right)=\ mathit {\ ln} {q} _e- {K} _1t $$(3)ここで、 q e ( mg / g)は平衡状態の吸着量であり、 q t (mg / g)は、時間 t での吸着量です。 。 K 1 は、疑似一次反応速度の速度定数です。同時に、疑似二次反応速度モデルは、イオンの吸着反応速度により広く適用されます。疑似二次反応速度式の線形式を式(1)に示します。 (4)[26]:
$$ \ frac {t} {q_t} =\ frac {1} {K_2 {q} _e ^ 2} + \ frac {1} {q_e} t $$(4)<図> <画像> <ソースタイプ="image / webp" srcset ="// media.springernature.com / lw685 / springer-static / image / art%3A10.1186%2Fs11671-018-2814-9 / MediaObjects / 11671_2018_2814_Fig4_HTML.png?as =webp">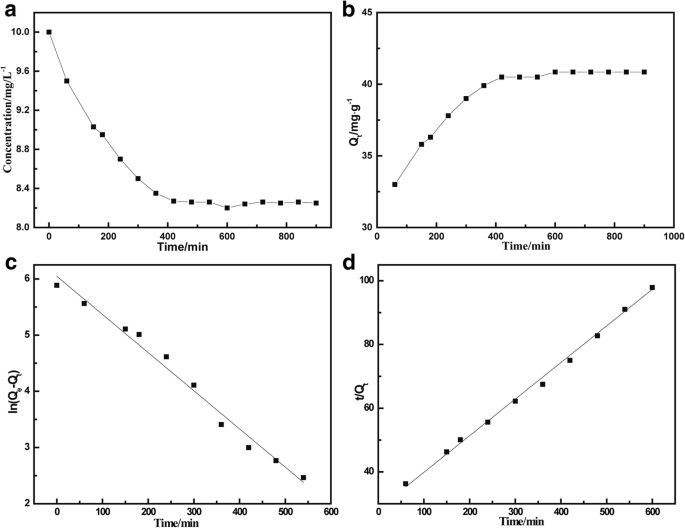
MnFe 2 のTC吸着速度論 O 4 / rGOナノコンポジット。 a TC濃度と( b )吸着容量と吸着時間の関係、および( c )疑似一次速度論モデルおよび( d )疑似2次反応速度モデル
ここで K 2 この方程式では、疑似2次反応速度の速度定数を表します。
この研究の実験結果に基づいて、図4c、dは、それぞれ1次吸着速度論と2次吸着速度論を適用することによる吸着のフィッティングラインを示しています。 2つの反応速度モデルの詳細なパラメータを表1に示します。
<図>相関係数( R 2 、0.99)疑似2次モデルのフィッティングは、疑似1次モデルのフィッティング(0.98)よりも高かった。それは、彼の疑似二次速度論モデルが、MnFe 2 へのTCの吸着速度論を記述するのに適していることを示した。 O 4 / rGOナノコンポジット。運動定数 K 2 114.87 g mg min -1 でした 。 TCがMnFe 2 とどのように相互作用したかを理解する O 4 / rGOナノコンポジット、LangmuirおよびFreundlich等温線モデルを使用して吸着データを適合させました。ラングミュアモデルは一般的に式として表されます。 (5)[27]:
$$ \ frac {C_e} {q_e} =\ frac {1} {K_L {q} _m} + \ frac {C_e} {q_m} $$(5)ここで C e (mg / L)は平衡濃度、 q e (mg / g)は平衡状態の吸着量、 q m (mg / g)は、吸着剤の最大単分子層吸着容量 K L 、ラングミュア定数は、吸着剤と吸着質の間の親和性に関連しています。 q の値 m および K L 方程式の傾きと切片によって得られます。一方、Freundlich等温線モデルは次の式で表されます[28]:
$$ \ mathit {\ ln} {q} _e =\ mathit {\ ln} {K} _F + \ frac {1} {n} \ mathit {\ ln} {C} _e $$(6)ここで K F Freundlich定数であり、 n 強度を表す吸着指数です。
この種の吸着の等温線モデルを理解するために、LangmuirモデルとFreundlichモデルの両方を使用した線形フィッティングを図5に示し、関連するパラメーターを表2に示します。表2からわかるように、吸着MnFe 2 の O 4 / rGO to TCは、Langmuir等温線よりもFreundlich等温線の方が適していました。 Freundlich吸着モデルは、吸着が不均一な表面に基づいていることを前提としていますが、Freundlichモデルは、さまざまな表面の非理想的な吸着や多層吸着によく使用されます。 rGOへのテトラサイクリンの吸着は、テトラサイクリンとrGOの分子構造に関連していた。 TCには、π-π相互作用によってrGOに容易に吸着できる4つの芳香環がありました。このような相互作用により、多層吸着が可能になりました。 TC分子間の同じ相互作用により、追加のTC分子を引き付けることができます。吸着指数 n このモデルでは2〜3の範囲であり、この吸着システムが「好ましい」と予測されました。温度が上昇すると、ナノコンポジット上のTCの吸着容量も増加しました。これは、吸着プロセスが吸熱性であることを示しています。
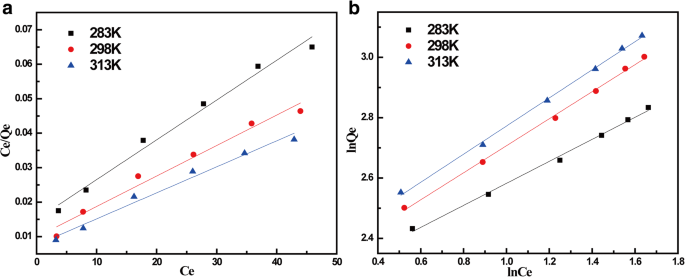
MnFe 2 のTC吸着等温線 O 4 / rGOナノコンポジット。 ( a を備えた吸着等温線 )ラングミュアモデルと( b )それぞれ283、298、313Kでのフロイントリッヒ等温線
吸着に対するpHの影響を調べるために、30 mLのTC溶液(10 mg / L)と5mgのMnFe 2 O 4 / rGO粉末を混合し、各テストで溶液のpHを2.0、3.3、5.0、7.7、9.0、9.7、および10.5に調整しました。溶液を25℃の温度で発振器に入れました。濃度を測定するために、吸着平衡でサンプルを採取した。さまざまなpHでの吸着挙動を調査し、pH 2.0〜10.5でテストした結果を図6に示しました。MnFe 2 の最大吸着容量 O 4 TCでの/ rGOは、溶液のpHが3.3のときに発生します。 pHが3.3未満の場合、酸性度の増加とともに吸着が減少しました。これは主に、TCH 3+ 間の吸着サイトでの競合が原因でした。 大量のH + 溶液中のイオン。 pHが3.3から7.7の間のとき、TCはTCH 2 の形で存在していました。 0 。静電相互作用は1週間でした。溶液がよりアルカリ性になると、OH - が増加しました MnFe 2 からの金属イオンで沈降を引き起こす可能性があります O 4 / rGO、したがって吸着を減らします。 pH =9.7では、これはまさに、溶液中で形成された主要なTCがTCH - から変化する遷移点でした。 TC 2- へ 。したがって、pH =9.7でのピークの存在は、溶液中のイオン形態の変化によるものと考えられます。この研究では、HCl溶液(0.1 mol / L)を溶離液として使用して、MnFe 2 の吸着-再生特性を調べました。 O 4 / rGOからTCへ。吸着は25°Cで5mgのMnFe 2 を使用して行いました。 O 4 / rGOを10mg / LTCソリューションに追加します。吸着平衡後、MnFe 2 O 4 / rGOはHCl溶液で溶出しました。次に、溶出したMnFe 2 O 4 / rGOを再度吸着に使用し、吸着容量を測定しました。溶出は3回行い、各溶出後の吸着容量を比較することにより、吸着-再生特性を導き出しました。この調査では、すべてのテストが少なくとも3回実行されました。すべての実験の発振器は180rpmの固定速度に設定されました。図6bは、MnFe 2 の吸着-再生挙動を示しています。 O 4 TC吸着に関する/ rGO。初期除去率は86%でした。 HClで溶出した後、最初の4サイクルでTCの除去率は85%、82%、79%、71%でした。吸着剤は簡単に再生して再利用できることが示されました。
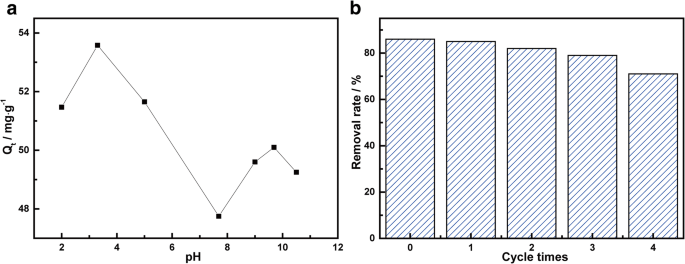
a MnFe 2 へのTCの吸着に対するpHの影響 O 4 / rGOナノコンポジットおよび( b )初期TC濃度が10 mg / Lの場合の除去率とサイクリング数の関係
全体として、rGOは主にTCの吸着に寄与していると考えました。まず、MnFe 2 のサイズ O 4 数十ナノメートルに達した。全体の表面積に大きく貢献することはできませんでした。第二に、全体的な吸着容量はTCで〜40 mg / gであり、初期濃度は〜10 mg / mLでした。この値は、報告されているGOの吸着容量とほぼ同じでした[14]。磁性MnFe 2 の出現 O 4 吸着剤rGOの抽出とリサイクルを簡単に行いました。
結論
MnFe 2 O 4 / rGOナノコンポジットはワンポット法で合成に成功しました。ナノコンポジットは、初期TC濃度が10 mg / Lの場合、41 mg / gの吸着容量を持つTCの効率的な吸着剤として使用できます。吸着プロセスの速度論と等温線は、それぞれ疑似二次モデルとフロイントリッヒモデルとして記述されました。磁性吸着剤は分離して再生することができ、MnFe 2 を示します。 O 4 / rGOナノコンポジットは、TC汚染の環境修復のための有望な再利用可能な吸着剤になる可能性があります。
略語
- GO:
-
酸化グラフェン
- rGO:
-
還元型酸化グラフェン
- TC:
-
テトラサイクリン
- TEM:
-
透過型電子顕微鏡
ナノマテリアル
- 化学センシング用の貴金属ナノ粒子で装飾されたエレクトロスピニングポリマーナノファイバー
- チタン酸塩ナノチューブで装飾された酸化グラフェンナノコンポジット:調製、難燃性、および光分解
- 多機能GaN / Feナノ粒子による内皮細胞の標的化
- invitroおよびinvivoでのグラフェンおよび酸化グラフェンのバイオセーフティおよび抗菌能力
- クルクミンの処理効果を持つPEGコーティングされたCoFe2O4ナノ粒子の毒性
- 粒子サイズと感度を大幅に低減するためのナノスケールCL-20 /酸化グラフェンのワンステップボールミル調製
- 抗菌剤として銀ナノ粒子で装飾された酸化グラフェンベースのナノコンポジット
- 酸化グラフェンの低温還元:電気コンダクタンスと走査型ケルビンプローブフォース顕微鏡
- 高性能スーパーキャパシター用のアニオン性界面活性剤/イオン液体挿入還元グラフェン酸化物
- 非常に濃縮された亜鉛源を用いた水/グリセロール中のナノサイズの酸化亜鉛の調製のための簡単なアプローチ
- ミルストーン剥離:大型の数層酸化グラフェンの真のせん断剥離



