リチウムイオン電池用のカーボンナノチューブとグラフェンで修飾されたFeF3・0.33H2Oの高性能カソード材料
要約
FeF 3 ・0.33H 2 Oカソード材料は、変換反応で複数の電子を移動させることにより、高容量、高エネルギー密度を発揮することができ、研究者から大きな注目を集めています。ただし、FeF 3 の低導電率 ・0.33H 2 Oはその適用を大幅に制限します。一般に、カーボンナノチューブ(CNT)とグラフェンは、活物質の導電性を向上させるための導電性ネットワークとして使用できます。この作品では、FeF 3 ・0.33H 2 Oカソード材料は液相法で合成され、FeF 3 ・0.33H 2 O / CNT +グラフェンナノコンポジットは、CNTとグラフェン導電性ネットワークの導入により成功裏に製造されました。電気化学的結果は、FeF 3 ・0.33H 2 O / CNT +グラフェンナノコンポジットは、234.2 mAh g -1 の高い放電容量を提供します 1.8〜4.5 Vの電圧範囲で(vs. Li + / Li)0.1 Cレートで、卓越したサイクリングパフォーマンスを示します(193.1 mAh g -1 0.2 Cレートで50サイクル後)、およびレート機能(140.4 mAh g -1 5 Cレートで)。したがって、FeF 3 の電子伝導性と電気化学的性能 ・0.33H 2 CNTとグラフェン複合導電性ネットワークで修飾されたOカソード材料は効果的に改善することができます。
はじめに
充電式リチウムイオン電池(LIB)は、携帯型電子機器の最も効果的な電力貯蔵システムであり、電気自動車(EV)およびハイブリッド電気自動車(HEV)の有望な候補と見なされています[1]。従来の化石エネルギーと比較して、LIBは再生可能でクリーンなエネルギーであり、環境に優しいものです。最近、LIB技術の急速な発展に伴い、エネルギーと電力密度の両方に対する需要が継続的に増加しています。重要な課題の1つは、高性能の電極活物質の開発であり、カソード材料は、比容量、サイクリング能力、レート能力など、LIBの電気化学的特性を改善するための重要な要素です[2、3]。 LiCoO 2 などの市販のカソード材料 [4]、LiMn 2 O 4 [5]、およびLiFePO 4 [6]は、単一電子反応のみを伴うインターカレーション反応のために理論容量が低く、EVの要求を満たすことができません。過去数年間、多電子材料は、変換反応によって複数の電子の移動を実現できるため、大きな関心を集めています[7]。金属フッ化物は、高い理論容量、エネルギー密度、および動作電圧を備えた理想的なカソード材料です。その中で、FeF 3 712 mAh g -1 の高い理論比容量により、最も適切なカソード材料と見なされています。 (3e − 転送)および237 mAh g -1 (1e − 転送)、約2.7 Vでの高放電電圧プラトー、および優れた熱安定性[8,9,10]。
これらの顕著なメリットにもかかわらず、FeF 3 カソード材料にはまだいくつかの欠点があり、それが実際の用途を制限している。 FeF 3 の主な欠点 は、高いイオン性によって引き起こされるその電子絶縁挙動であり、Fe-F結合の大きなバンドギャップを引き起こし、最終的には実際の比容量が低くなり、レート能力が低下し、エネルギー効率が低下します[11、12、13]。これらの問題を解決するために、電子伝導性とイオン伝導性の低さを克服するためにさまざまな戦略が採用されてきました。一般に、導電率を改善する方法は、次の3つの側面に要約できます。(1)元素のドーピング。元素のドーピングは、バンドギャップを効果的に減少させ、微結晶の成長に積極的に影響を与える可能性があります[14、15]。 Rahman etal。調製したCoドープフッ化鉄(Fe 0.9 Co 0.1 F 3 ・0.5H 2 O)非水沈殿法により、227 mAh g -1 の高い排出容量が得られます。 0.1 C、1.8〜4.5 V [14]。 (2)表面コーティング。コーティング層を導入することによる変更は、Li + を大幅に短縮することができます 輸送長と体積変化の緩和[16]。 Ma etal。正常に製造されたFeF 3 新しいinsitu重合法により、ポリ(3,4-エチレンジオキシチオフェン)(PEDOT)でコーティングされ、サンプルは120 mAh g -1 の高出力能力を示しました。 1 A g -1 電極内のイオンおよび電子輸送が改善されているため、室温で[17]。 (3)導電性添加剤を使用した複合材料の製造。これにより、FeF 3 のサイクリングとレートのパフォーマンスを大幅に向上させることができます。 カソード材料[18、19、20、21]。ユングら得られたFeF 3 /高い可逆比容量(178 mAh g -1 )を示した秩序化メソポーラスカーボン(OMC)ナノコンポジット バルクFeF 3 よりも優れたサイクル安定性(容量フェージング8.8%)と2.0〜4.5Vの電圧範囲での2番目のサイクル中の0.1Cで (容量の低下は約42%)30サイクルで[22]。注目すべきことに、導電性ネットワークを備えた複合材料の製造は、イオン伝導性と電子伝導性の両方を改善して、最終的にカソード材料の電気化学的性能を向上させるための最も有益なアプローチです。
水和水の量が異なるフッ化鉄(III)カソード材料、たとえばFeF 3 ・0.33H 2 O [23]、FeF 3 ・0.5H 2 O [24]、FeF 3 ・3H 2 O [25]、およびFeF 3 [26]、広く報告されています。その中で、六角形のタングステンブロンズ型FeF 3 ・0.33H 2 Oは、最高の電気化学的特性により、その特徴的な1次元六角形キャビティが効率的なLi + に便利であることを示しました。 輸送し、電解質の浸透を促進することができます[27]。さらに、独自の構造により、水の動きを効果的に制限し、結晶構造を安定させることができます。さまざまな機能化カーボンマトリックスが導電性ネットワークとして使用されてきましたが、全体として、カーボンナノチューブ(CNT)とグラフェンは、その卓越した電子伝導性と優れた安定性により、導電性媒体として大きな可能性を示します[28、29、30、31]。グラフェンは、その大きな比面積により、電極と電解質の界面で十分な接触を促進することができ、グラフェンネットワークは電子移動とイオン移動において重要な役割を果たします。さらに、グラフェンは優れた機械的安定性を提供し、電極の曲げと伸びに寄与します[32、33]。
この研究では、ナノ構造のFeF 3 ・0.33H 2 Oカソード材料を液相法で合成した後、前駆体をCNTで粉砕した後、焼結してFeF 3 を得た。 ・0.33H 2 バインダーなしでグラフェン導電性ペーストとさらに混合されたO / CNT複合材料。最後に、CNTとグラフェンが共修飾されたFeF 3 ・0.33H 2 Oナノコンポジットの調製に成功しました。固有の柔軟性と大きな比表面積を備えたCNTは、電子輸送を大幅に促進し、高い機械的強度と高い化学的安定性を備えたグラフェンは、体積変化を効果的に緩衝し、電気化学反応をサポートします[31、34、35]。さらに、CNTとグラフェンシートの相互接続により、統合された3次元導電性フレームワークを構築でき、Li + を大幅に促進します。 拡散と同時に構造の安定性を高めます。したがって、FeF 3 と比較して ・0.33H 2 CNTと純粋なFeF 3 の単一の導電性ネットワークを備えた複合材料 ・0.33H 2 O、FeF 3 ・0.33H 2 CNTとグラフェンネットワークを備えたOナノコンポジットは、優れた電気化学的特性を示します。すべてのサンプルの形態、結晶構造、および電気化学的性能を体系的に調査しました。
結果と考察
構造および形態の分析
熱重量分析-示差走査熱量測定(TG-DSC)測定を実施して、FeF 3 の脱水温度を確認しました。 ・3H 2 O前駆体とその結果を図1aに示します。減量曲線の4つの段階は、30〜110°C、110〜250°C、250〜450°C、および450〜700°Cの領域に見られます。 30〜110°Cの最初の段階では、約3%のわずかな重量減少は、結晶の相変態に起因する可能性があります。 110〜250°Cの第2段階では、TG曲線の重量が約15%急速に減少し、DSC曲線は170°C付近に明らかな吸熱ピークを示します。対応する反応プロセスは、水和水(2.67 H 2 )の除去です。 O)FeF 3 から ・3H 2 O. 250〜450°Cの第3段階では、重量の減少は約6%です。これは、FeF 3 の水和水が除去されたことが原因である可能性があります。 ・0.33H 2 OはFeF 3 に変換します そして、DSC曲線から弱い発熱ピークが観察されます。 450〜700°Cの最終段階では、約4%のわずかな重量減少は、おそらくFeF 3 の分解によるものです。 。これらの結果によると、前駆体を真空オーブン内で80°Cで乾燥させて吸収水を除去し、240°Cで煆焼してFeF 3 を得ました。 ・0.33H 2 O。
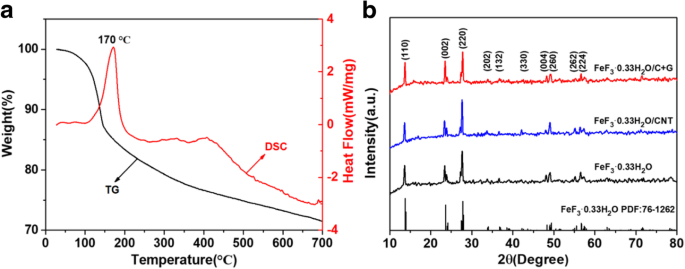
a FeF 3 のTG-DSC曲線 ・3H 2 O前駆体は、10°C分 -1 の加熱速度で30〜700°Cで測定されました アルゴン雰囲気下。 b FeF 3 のXRDパターン ・0.33H 2 O、FeF 3 ・0.33H 2 O / CNT、およびFeF 3 ・0.33H 2 O / C + G
合成されたサンプルの結晶構造を調査するために、X線回折(XRD)測定が行われました。 FeF 3 のXRDパターン ・0.33H 2 O、FeF 3 ・0.33H 2 O / CNT、およびFeF 3 ・0.33H 2 O / C + Gを図1bに示します。すべてのサンプルは、(110)、(002)、および(220)ファセットに従って2θ=13.79°、23.62°、および27.80°に位置する回折ピークを示しています。これは、六角形のタングステンブロンズ構造FeF <の標準スペクトルとよく一致しました。 sub> 3 ・0.33H 2 O(PDF No. 76-1262)[36]。 FeF 3 のXRDパターンでは、CNTとグラフェンの明らかな特徴的なピークは観察されません。 ・0.33H 2 O / CNTおよびFeF 3 ・0.33H 2 O / C + Gサンプル。これは主に、CNTとグラフェンの含有量が少ないためです。
複合材料の微細構造を分析するために、SEMおよびEDS測定を実施しました。 FeF 3 の形態と粒子サイズ ・0.33H 2 O、FeF 3 ・0.33H 2 O / CNTおよびFeF 3 ・0.33H 2 O / C + Gナノコンポジットを図2に示します。図2aから明確にわかるように、純粋なFeF 3 の粒子サイズ ・0.33H 2 Oは約100nmで、粒子のサイズは均一でよく分布しており、わずかな凝集が観察され、FeF 3 の粒子サイズは ・0.33H 2 Oは、図2eに示す粒度分布図でさらに確認できます。図2bは、FeF 3 の形態を示しています。 ・0.33H 2 O / CNTナノコンポジット。明らかに、CNTの導電性ネットワークはFeF 3 の表面で密接に絡み合っています。 ・0.33H 2 O粒子。 FeF 3 の場合 ・0.33H 2 O / C + Gナノコンポジット、FeF 3 の表面 ・0.33H 2 O粒子はCNTとグラフェンシートで包まれています。図2cに示すように、FeF 3 ・0.33H 2 O粒子とCNTはグラフェンシートで十分に覆われています。さらに、グラフェンシートはFeF 3 で良好な層状構造を維持しています。 ・0.33H 2 O / C + Gナノコンポジット。Li + に高速チャネルを提供できます。 輸送。 FeF 3 間の導電性接点 ・0.33H 2 O材料と集電体は、優れた電子伝導性により、CNTとグラフェンによって大幅に改善できます。特に表面積の大きいグラフェンは、Liイオン拡散のための追加の輸送チャネルを提供でき、FeF 3 になります。 ・0.33H 2 優れた電気化学的性能を備えたO / C + Gナノコンポジット。 FeF 3 の元素組成をさらに調査するために、EDSテストが実施されました。 ・0.33H 2 O / C + Gナノコンポジット。図2dのEDS画像から、Fe、F、O、Cの元素を観察できます。
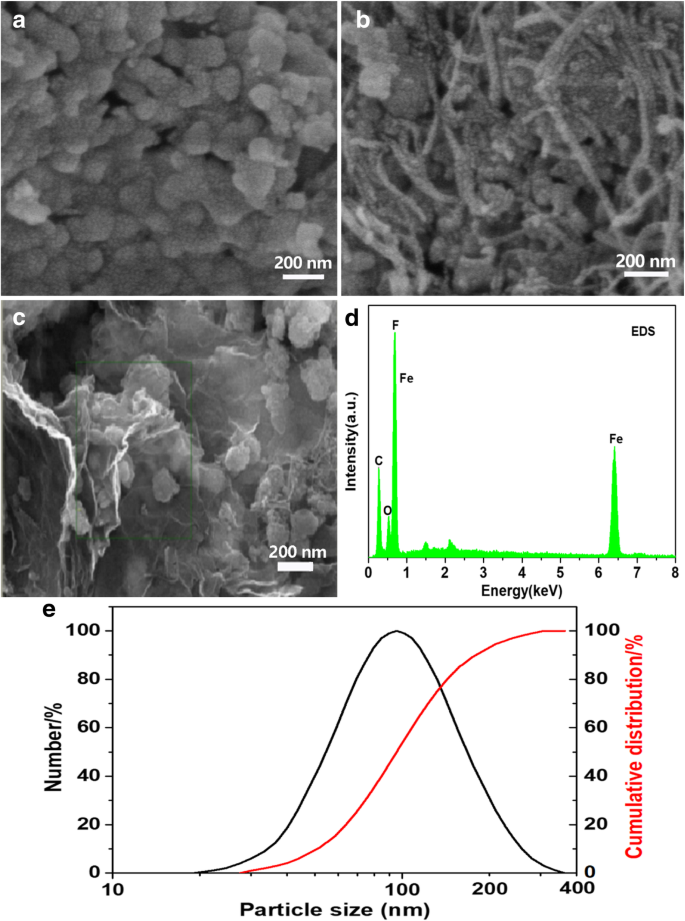
SEM画像、 a FeF 3 ・0.33H 2 O、 b FeF 3 ・0.33H 2 O / CNT、および c FeF 3 ・0.33H 2 O / C + G。 d FeF 3 のEDS ・0.33H 2 O / C + G。 e FeF 3 の粒度分布図 ・0.33H 2 O
FeF 3 の形態と詳細な微細構造 ・0.33H 2 O / C + GナノコンポジットはTEMによってさらに研究され、TEM画像が図3に表示されています。図3a、bに示すように、FeF 3 ・0.33H 2 O粒子とCNTおよびグラフェンシートは互いに密接に相互接続されており、これはSEM画像の結果と一致しています。図3cに示されているHRTEM画像は、バルク層とラッピング層の間に明確な描写を提供していません。 0.64 nmの格子縞間隔は、FeF 3 の(110)ファセットと一致します。 ・0.33H 2 O. FeF 3 のSAEDパターン ・0.33H 2 O / C + Gナノ粒子を図3dに示します。 (110)、(002)、(220)、(132)、および(004)の平面は、六角形のタングステンブロンズ構造FeF 3 にインデックス付けされたXRD結果に対応します。 ・0.33H 2 O. FeF 3 ・0.33H 2 小さな粒子サイズと優れた導電性ネットワーク構造を備えたO / C + Gナノコンポジットは、電極材料と電解質の間の十分な接触を促進し、リチウムイオン輸送を促進します。したがって、より優れた電気化学的性能を実現できます。
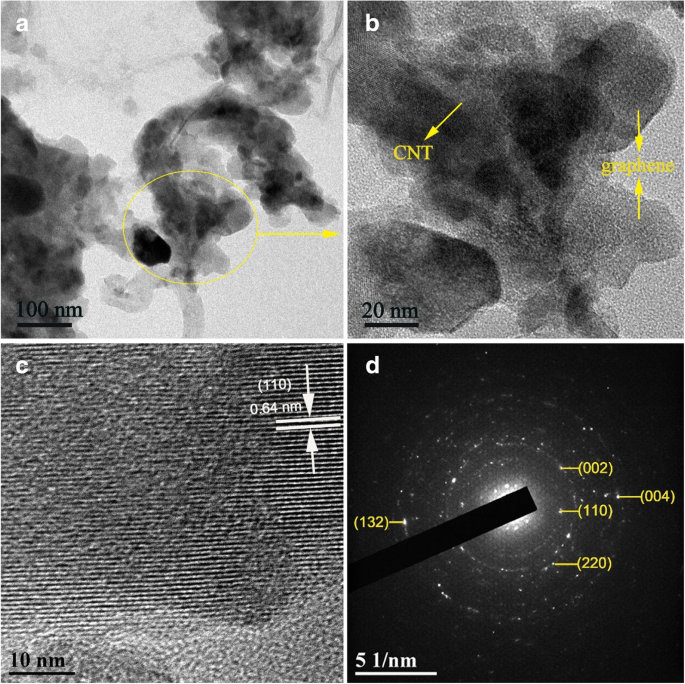
a 、 b FeF 3 のTEM画像 ・0.33H 2 O / C + Gナノコンポジット。 c FeF 3 のHRTEM画像 ・0.33H 2 O / C + Gナノコンポジット。 d FeF 3 のSAED画像 ・0.33H 2 O / C + Gナノコンポジット
電気化学的特性評価
すべてのサンプルの電気化学的特性を調査するために、1.8〜4.5 Vの電圧範囲で定電流充電/放電テストを実施しました(vs. Li + / Li)であり、この電圧範囲では1つの電子反応のみが発生します。すべてのサンプルの充放電プロファイルを図4に示します。0.1C(1 C =237 mAh g -1 )での3つの電極の初期充放電曲線 )レートは図4aに示されています。手付かずのFeF 3 ・0.33H 2 O電極は、217.5 mAh g -1 という最低の初期放電容量を示します。 、FeF 3 の電子伝導性が低いことが原因である可能性があります ・0.33H 2 O. FeF 3 ・0.33H 2 O / CNTおよびFeF 3 ・0.33H 2 O / C + G電極は、約225.1 mAh g -1 のより高い初期放電容量を提供します および234.2mAh g -1 、 それぞれ。私たちのテストでは、FeF 3 の初期放電容量 ・0.33H 2 O / C + G電極はわずか16.7mAh g -1 手付かずのFeF 3 よりも高い ・0.33H 2 CNTとグラフェンを示すO電極は、FeF 3 ではほとんど容量を提供しません ・0.33H 2 O / C + Gサンプル。容量がわずかに増加したのは、CNTとグラフェンの取り込みにより、電子輸送が強化され、電気化学的分極が減少したためと考えられます。すべての電極の初期の充放電曲線から、挿入反応(Li + )により、すべての曲線に2.7Vで明らかな放電プラトーがあります。 + e − + FeF 3 ∙0.33H 2 O→LiFeF 3 ∙0.33H 2 O)。 0.2 Cレートでのさまざまなサイクルの充放電プロファイルを図4b–dに示します。図4bに示すように、FeF 3 ・0.33H 2 O電極は、146.2 mAh g -1 の容量しか提供しません 50サイクル後に0.2Cの速度で。 FeF 3 ・0.33H 2 O / CNT電極は170.3mAh g -1 の容量を提供します 図4cに示す50サイクル後。 FeF 3 は注目に値します ・0.33H 2 O / C + G電極は193.1mAh g -1 の容量を保持します 図4dに示す50サイクル後でも。さらに、FeF 3 ・0.33H 2 O / C + G電極は、最低の充電電圧プラトーと最高の放電電圧プラトーを示し、電気化学的分極が最小で可逆性が優れていることを示しているため、電圧ヒステリシスが緩和されます。 FeF 3 のパフォーマンスの向上 ・0.33H 2 O / CNTおよびFeF 3 ・0.33H 2 O / C + G電極は、CNTとグラフェンを追加するとFeF 3 の導電率を効果的に改善できることを示しています。 ・0.33H 2 Oカソード材料。特に、FeF 3 ・0.33H 2 O / C + G電極は、CNTのインターレースにより最高の電気化学的性能を示し、グラフェンは3次元の導電性構造を形成し、Liイオンの輸送を大幅に促進し、Liイオンのインターカレーションプロセスを促進します[ 37、38]。
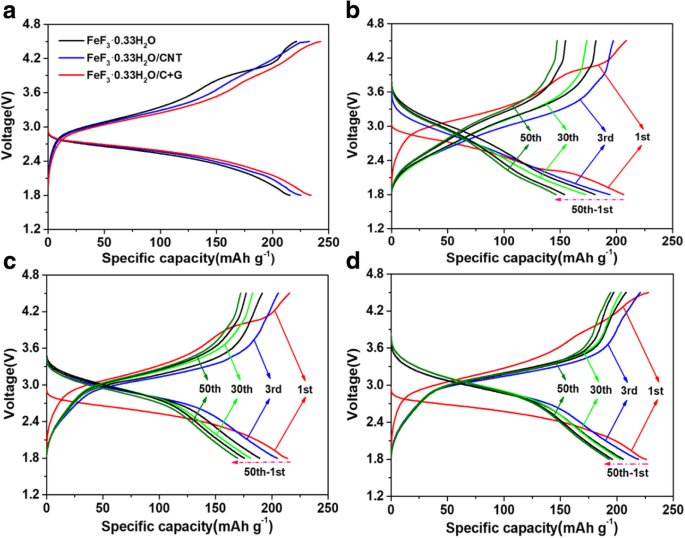
a FeF 3 の初期充放電プロファイル ・0.33H 2 O、FeF 3 ・0.33H 2 O / CNT、およびFeF 3 ・0.33H 2 0.1CレートでのO / C + G電極。 0.2 Cレート、 b でのさまざまなサイクル(1、3、30、50)の充電および放電プロファイル FeF 3 ・0.33H 2 O、 c FeF 3 ・0.33H 2 O / CNT、および d FeF 3 ・0.33H 2 O / C + G
FeF 3 の優れたサイクリング安定性をさらに実証するため ・0.33H 2 O / C + Gナノコンポジット、FeF 3 のサイクリング機能 ・0.33H 2 O、FeF 3 ・0.33H 2 O / CNT、およびFeF 3 ・0.33H 2 O / C + G電極、1.8〜4.5Vの電圧範囲で0.2Cレートで50サイクルまで(vs. Li + / Li)を図5aに示します。 FeF 3 ・0.33H 2 急速な容量低下と50サイクル後の約70.83%(1サイクルあたり0.58%の容量低下率)の不十分な容量保持を備えたO電極。 FeF 3 ・0.33H 2 O / CNT電極は、50サイクル後に約79.65%(1サイクルあたり0.41%のフェード)の容量保持を示します。特に、FeF 3 ・0.33H 2 O / C + G電極は、50サイクル後に85.48%(1サイクルあたりわずか0.29%のフェード)という最高の容量保持を実現します。さらに、FeF 3 のクーロン効率 ・0.33H 2 O / C + G電極は、Li + の間に99%以上に達する可能性があります 挿入および抽出プロセス。上記の結果は、CNTとグラフェンが電子伝導性を改善し、FeF 3 の放電容量を向上させることができることを示しています。 ・0.33H 2 O.特に、FeF 3 ・0.33H 2 O / C + G電極は最高のサイクリング性能を示し、CNTとグラフェンを添加した後、より高い導電率、より優れた可逆性、およびより低い分極を示します。表面積の大きいCNTは電子移動に十分な経路を供給し、グラフェンは高速Li + を可能にする優れた導電性ネットワークとして機能します。 電解質と電極間の輸送[28、35]。さらに、FeF 3 ・0.33H 2 O粒子とCNTは、グラフェンシートの積み重ねを妨げるスペーサーとして機能し、高い活性表面積を提供します。したがって、FeF 3 の相互作用 ・0.33H 2 O粒子とCNTおよびグラフェンは、サイクリング性能を大幅に向上させることができます。
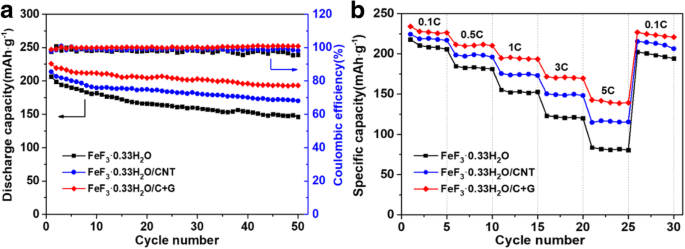
a FeF 3 のサイクリングパフォーマンス ・0.33H 2 O、FeF 3 ・0.33H 2 O / CNT、およびFeF 3 ・0.33H 2 0.2CレートのO / C + G電極。 b FeF 3 のパフォーマンスを評価する ・0.33H 2 O、FeF 3 ・0.33H 2 O / CNT、およびFeF 3 ・0.33H 2 異なる電流密度でのO / C + G電極
FeF 3 のレート機能 ・0.33H 2 O、FeF 3 ・0.33H 2 O / CNT、およびFeF 3 ・0.33H 2 O / C + G電極は、0.1 C、0.5 C、1 C、3 C、および5 Cの速度で評価され、次に再び0.1 Cの速度で評価され、結果が図5bに表示されます。すべてのサンプルの放電容量は、電流密度の増加とともに減少します。予想通り、FeF 3 ・0.33H 2 O / C + G電極は、3つの電極の中で優れたレート性能を示し、228 mAh g -1 の平均放電容量を提供します。 、210.7 mAh g -1 、194.4 mAh g -1 、170.5 mAh g -1 、および140.4 mAh g -1 0.1 C、0.5 C、1 C、3 C、および5Cのレートで。レートを0.1Cに戻しても、電極は226.7 mAh g -1 の放電容量を提供できます。 。比較のために、FeF 3 ・0.33H 2 OおよびFeF 3 ・0.33H 2 O / CNT電極は劣ったレート性能を示します。それらは81.7mAh g -1 の不十分な放電容量を提供します および115.7mAh g -1 FeF 3 よりも著しく低い5Cレートで ・0.33H 2 O / C + G電極。その結果、FeF 3 のレート機能 ・0.33H 2 O / C + G電極は、FeF 3 の電極と比較して大幅に改善されています。 ・0.33H 2 O単一のCNT導電性ネットワークの有無にかかわらず。したがって、FeF 3 の良好なレート機能 ・0.33H 2 O / C + G電極は、電子伝導性を強化したCNTとグラフェン導電性ネットワークから生じます。とりわけ、構築された3次元導電性ネットワークは、電極間のLiイオンの挿入と抽出に役立ちます。
FeF 3 の電気化学的特性をさらに調べるために、サイクリックボルタモグラム(CV)測定を実施しました。 ・0.33H 2 O、FeF 3 ・0.33H 2 O / CNT、およびFeF 3 ・0.33H 2 1 mV s -1 のスキャンレートでのO / C + G電極 1.8 V〜4.5 V(vs。Li + / Li)図6に示されています。3つの曲線は、脱リチウム化/リチウム化プロセスに対応する見かけの酸化/還元ピークを持つ同様の形状を示しています。 FeF 3 の酸化と還元のピーク ・0.33H 2 O / C + G電極は3.32Vと2.78Vで検出され、電位間隔(ΔE p )は0.54Vです。ΔE p FeF 3 の値 ・0.33H 2 OおよびFeF 3 ・0.33H 2 O / CNT電極はそれぞれ0.59Vと0.62Vです。小さいΔE p 値は、電気化学的分極が小さく、電極の可逆性が高いことを示します。さらに、FeF 3 ・0.33H 2 O / C + G電極は、FeF 3 よりも高い電流と大きな面積を示します。 ・0.33H 2 OおよびFeF 3 ・0.33H 2 O / CNT電極。 CV曲線で囲まれた領域は、材料の容量を表します。面積が大きいほど容量が大きくなり、面積の変化率は容量の減衰率を表します。結果は、FeF 3 ・0.33H 2 O / C + G電極は、より高い容量とより優れた可逆性を備えており、定電流充電/放電テストとよく一致しています。
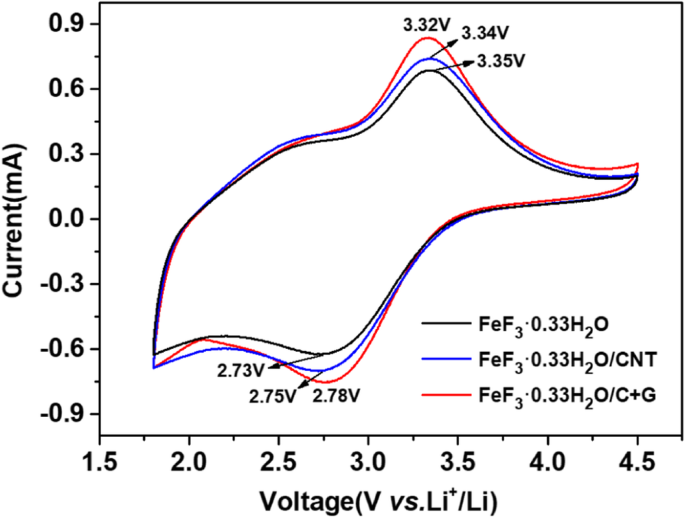
FeF 3 のCV曲線 ・0.33H 2 O、FeF 3 ・0.33H 2 O / CNT、およびFeF 3 ・0.33H 2 1 mV s -1 のスキャンレートでのO / C + G電極
電気化学インピーダンス分光法(EIS)測定を実行して、FeF 3 の電気化学反応速度論的挙動を調査しました。 ・0.33H 2 O、FeF 3 ・0.33H 2 O / CNT、およびFeF 3 ・0.33H 2 3サイクル目と50サイクル後のO / C + G電極、および結果を図7a、bに示します。活性化後の電極のすべてのナイキスト線図は、半円と傾斜した線で構成されています。高周波の半円は、電荷移動抵抗( R )に関連しています。 ct )、これは電極の反応速度を表します。半円の半径が小さいほど、Li + の輸送が容易であることを示しています。 電解質と電極の界面間の電子移動、および低周波数の傾斜線は、ウォーバーグ抵抗( Z )に関連しています。 w )のLi + カソード材料の大部分での拡散[39]。対応する等価回路モデルは、図7eに示すインピーダンススペクトルを示すために作成されました。補償されていないオーム抵抗( R s )は電解質と電極材料の抵抗を表し、定位相角要素(CPE)は二重層静電容量と不動態皮膜静電容量を表します[40]。 R のインピーダンス値 s および R ct 3番目と50番目のサイクル後の3つの電極について、表1にリストされています。 R に有意差はありません。 s 3番目のサイクル後の3つの電極の値が示されています。ただし、 R ct FeF 3 の値(50.9Ω) ・0.33H 2 O / C + G電極は、FeF 3 の電極よりも明らかに低いです。 ・0.33H 2 O(115.7Ω)およびFeF 3 ・0.33H 2 O / CNT(68.2Ω)電極。これは、FeF 3 の分極が少ないことを示しています。 ・0.33H 2 O / C + G電極。さらに、 R ct FeF 3 の値 ・0.33H 2 O / C + G電極は50サイクル後86.5Ωであり、これも3つの電極の中で最小です。下の R ct 活性化後の電極の値は、より良い電荷移動速度論的挙動を示唆しました。リチウムイオン拡散係数(D Li + )FeF 3 の ・0.33H 2 O、FeF 3 ・0.33H 2 O / CNT、およびFeF 3 ・0.33H 2 O / C + G電極は、次の式から計算されます[41]、
$$ {D} _ {\ mathrm {Li} +} =\ frac {{\ mathrm {R}} ^ 2 {\ mathrm {T}} ^ 2} {2 {\ mathrm {A}} ^ 2 {\ mathrm {n}} ^ 4 {\ mathrm {F}} ^ 4 {\ mathrm {C}} ^ 2 {\ upsigma} _ {\ upomega} ^ 2} $$(1)<図> <画像> <ソースtype ="image / webp" srcset ="// media.springernature.com / lw685 / springer-static / image / art%3A10.1186%2Fs11671-019-2925-y / MediaObjects / 11671_2019_2925_Fig7_HTML.png?as =webp">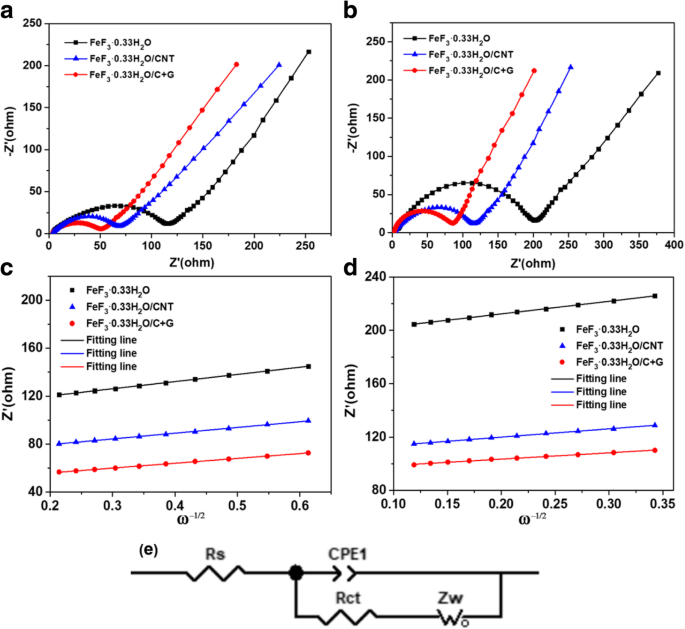
FeF 3 のナイキスト線図 ・0.33H 2 O、FeF 3 ・0.33H 2 O / CNT、およびFeF 3 ・0.33H 2 O / C + G電極; a 3番目のサイクルと b 50サイクル目。 FeF 3 の関係プロット ・0.33H 2 O、FeF 3 ・0.33H 2 O / CNT、およびFeF 3 ・0.33H 2 Z ’間のO / C + G電極 およびω −1/2 低周波領域で; c 3番目のサイクルと d 50サイクル目。 e EISの対応する等価回路モデル
<図>式で。 (1)、 R はガス定数、 T は絶対温度、 A は電極の表面積、 n はレドックス反応に関与する電子の数、 F はファラデー定数、 C Li + のモル濃度です 、およびσ ω は、次の関係から得られるウォーバーグ係数です。
$$ {\ mathrm {Z}} ^ {\ hbox {'}} ={R} _ {\ mathrm {s}} + {R} _ {\ mathrm {ct}} + {\ upsigma} _ {\ upomega } {\ upomega} ^ {-1/2} $$(2)ここで、 Z ’ はインピーダンスの実数部であり、ω は低周波数領域の角周波数です。 Z ’の線形性 およびω − 1/2 3番目のサイクルと50番目のサイクルの後を図7c、dに示します。 Li + 3つの電極の拡散係数を表1に示します。 D Li + 値(1.67×10 -12 cm 2 s -1 )FeF 3 の ・0.33H 2 3サイクル後のO / C + G電極は、FeF 3 の電極よりも高くなっています。 ・0.33H 2 O / CNT(1.19×10 -12 cm 2 s -1 )およびFeF 3 ・0.33H 2 O(7.63×10 -13 cm 2 s -1 )。さらに、 D Li + FeF 3 の値 ・0.33H 2 O、FeF 3 ・0.33H 2 O / CNT、およびFeF 3 ・0.33H 2 50サイクル後のO / C + G電極は2.96×10 -13 cm 2 s -1 、7.10×10 −13 cm 2 s -1 、および1.21×10 −12 cm 2 s -1 、 それぞれ。どうやら、 D Li + FeF 3 の値 ・0.33H 2 O / C + G電極は、3つの電極の中で最も高く、FeF 3 ・0.33H 2 O / C + Gは、より優れた電極反応速度を示します。結果は、CNTとグラフェンによって構築された導電性ネットワークがFeF 3 の分極を効果的に低減できることを確認しています。 ・0.33H 2 優れた電気化学的性能に寄与するO / C + G電極。
結論
要約すると、FeF 3 ・0.33H 2 Oカソード材料は液相法で合成に成功し、FeF 3 ・3H 2 O前駆体をCNT導電性ネットワークで粉砕した後、焼結してFeF 3 ・0.33H 2 O / CNTナノコンポジット、次にバインダーなしでグラフェン導電性ペーストと混合して、FeF 3 を取得します。 ・0.33H 2 O / C + Gナノコンポジット。 CNTとグラフェンで構成される機能ネットワークは、FeF 3 の電子伝導性を改善するための効果的な戦略を提供します。 ・0.33H 2 Oカソード材料。 FeF 3 ・0.33H 2 O / C + Gナノコンポジットは、純粋なFeF 3 よりも、比容量の増加、サイクル寿命の延長、およびレート能力の向上により、優れた電気化学的性能を示します。 ・0.33H 2 O. EISの結果は、FeF 3 ・0.33H 2 O / C + G電極は、最高の電気化学反応速度論的挙動を示します。 FeF 3 の卓越した電気化学的性能 ・0.33H 2 O / C + Gは、CNTとグラフェンによって構築された3次元導電性ネットワークに起因する可能性があり、電子伝導性を改善し、Li + を促進します。 と電子伝達、したがってサイクリングとレート機能を強化します。したがって、FeF 3 ・0.33H 2 CNTとグラフェンで修飾されたOカソード材料は、優れた電気化学的特性を示し、LIBアプリケーションのカソード材料として大きな期待を示しました。
メソッド
FeFの合成 3 ・0.33H 2 Oパウダー
FeF 3 ・0.33H 2 O粉末は液相法とそれに続く焼鈍処理により合成された。 FeF 3 の合成用 ・0.33H 2 O粉末、Fe(NO 3 ) 3 ・9H 2 O(アラジン、99.99%)およびNH 4 鉄およびフッ素源としてそれぞれF(アラジン、98%)を使用し、分散剤としてポリエチレングリコール(PEG400、アルドリッチ、20%)を使用しました。まず、3.1 g Fe(NO 3 ) 3 ・9H 2 テフロンで裏打ちされたステンレス鋼のオートクレーブでOを20mLのエタノールに溶解し、次にPEG400を3滴加えました。次に、溶液を10分間超音波処理して、溶液Aを取得しました。次に、0.85 g NH 4 Fを5mLの脱イオン水に溶解し、超音波処理して溶液Bを形成しました。絶えず攪拌している溶液Aに溶液Bを滴下すると、黄色の溶液は徐々に無色になり、最終的には塊状の沈殿物が得られました。室温で12時間煮込んだ後、沈殿物を脱イオン水とエタノールで数回交互に洗浄し、真空オーブンで80°Cで12時間乾燥させました。自然に室温まで冷却した後、沈殿物を粉砕して粉末にし、FeF 3 を得た。 ・3H 2 O前駆体をチューブ炉に移し、アルゴン雰囲気下で240°Cで3時間焼成して、結晶水を除去します。最後に、FeF 3 ・0.33H 2 O粉末が得られた。
FeF 3 の準備 ・0.33H 2 O / CNT +グラフェン組み合わせ電極
FeF 3 を準備するには ・0.33H 2 CNTとグラフェン導電性ネットワークを使用したOで、最適化された量の5 wt%CNTを調製したままの前駆体に添加し、均一に粉砕し、アルゴン雰囲気下で管状炉(240°Cで3時間)で加熱してFeF 3を得ました。 ・0.33H 2 O / CNTパウダー。次に、0.5 g FeF 3 ・0.33H 2 O / CNT粉末を1.5mLグラフェン N に添加しました -メチルピロリドンペースト(アラジン、グラフェン含有量:1–1 .5wt%)、4時間攪拌して、均一なスラリーを形成します。スラリーをAl箔に貼り付け、85°Cで一晩乾燥させてFeF 3 を得ました。 ・0.33H 2 O / CNT +グラフェン(FeF 3 と表記) ・0.33H 2 O / C + G)組み合わせ電極。特に、コンビネーション電極を作成するプロセスでは、バインダーを追加する必要はありませんでした。
特性評価
前駆体の熱重量分析-示差走査熱量測定(TG-DSC)測定は、30〜700°Cの温度範囲で10°Cmin -1 の加熱速度で実行されました。 アルゴン雰囲気下。すべてのサンプルの結晶構造は、8°min -1のスキャン速度で10°〜80°の2θ範囲のCuKα放射線を用いたX線回折(XRD、Bruker AXS D8、ドイツ)によって特徴づけられました。 。材料の形態と粒子サイズは、走査型電子顕微鏡(SEM、JEOL JSM-6610 LV)およびエネルギー分散型分光法(EDS、JEOL JSM-6610 LV)によって観察されました。透過型電子顕微鏡(TEM)と選択領域電子回折(SAED)を実施し、透過型電子顕微鏡(JEOL JSM-2100F)を使用して材料の微細構造をさらに調査しました。
電気化学的測定
準備されたカソード材料の電気化学的性能は、CR2032コイン型ハーフセルによって特徴づけられました。作用電極は、カソード材料(FeF 3 ・0.33H 2 OまたはFeF 3 ・0.33H 2 N で90:5:5の重量比のO / CNT)、カーボンブラック(Super P Liカーボン)、およびポリフッ化ビニリデン(PVDF) -メチルピロリドン(NMP)。スラリーが均一に攪拌されたら、Al箔に貼り付け、85°Cで一晩乾燥させました。 FeF 3 ・0.33H 2 O / C + Gコンビネーション電極は上記のように作製した。陰極電極をプレスしていくつかのディスクに切断し、重さを量った後、真空オーブン内で85°Cで4時間乾燥させました。コインタイプのセルは、アルゴンが充填されたグローブボックス内で組み立てられ、酸素と水分の含有量が0.1 ppm未満に制御され、アノードとして金属Liフォイル、セパレーターとしてCelgard2400メンブレンが使用されました。 1.0 M LiPF 6 電解質として、体積比1:1:1のエチレンカーボネート(EC)、プロピレンカーボネート(PC)、およびジエチルカーボネート(DEC)を使用しました。すべてのコイン電池は、テスト前に4時間エージングされました。定電流充電/放電テストは、1.8〜4.5 Vの電圧範囲で実行されました(vs. Li + / Li)室温でのLandバッテリーテストシステム(LAND CT-2001A、武漢、中国)。作用電極の比容量は、活性カソード材料の質量に基づいて計算されました。サイクリックボルタンメトリー(CV)および電気化学インピーダンス分光法(EIS)は、電気化学ワークステーション(CorrTest CS310)によって測定されました。 CVテストのスキャンレートは1mV s -1 でした。 1.8〜4.5 Vの電圧範囲で(vs. Li + / Li)。 EISの周波数範囲は、5mVの定電位信号振幅で100kHz〜0.01Hzでした。
略語
- CNT:
-
カーボンナノチューブ
- CPE:
-
一定の位相角要素
- CV:
-
サイクリックボルタンメトリー
- DEC:
-
炭酸ジエチル
- D Li + :
-
リチウムイオン拡散係数
- EC:
-
エチレンカーボネート
- EDS:
-
エネルギー分散型分光法
- EIS:
-
電気化学インピーダンス分光法
- EV:
-
電気自動車
- FeF 3 ・0.33H 2 O / C + G:
-
FeF 3 ・0.33H 2 O / CNT +グラフェン
- HEV:
-
ハイブリッド電気自動車
- LIB:
-
リチウムイオン電池
- NMP:
-
N -メチルピロリドン
- OMC:
-
注文したメソポーラスカーボン
- PC:
-
炭酸プロピレン
- PEDOT:
-
ポリ(3,4-エチレンジオキシチオフェン)
- PEG:
-
ポリエチレングリコール
- PVDF:
-
ポリフッ化ビニリデン
- R ct :
-
電荷移動抵抗
- R s :
-
オーム抵抗
- SAED:
-
選択領域電子回折
- SEM:
-
走査型電子顕微鏡
- TEM:
-
透過型電子顕微鏡
- TG-DSC:
-
熱重量分析-示差走査熱量測定
- XRD:
-
X線回折
- Z w :
-
ウォーバーグの抵抗
ナノマテリアル
- スーパーキャパシター用途向けのグラフェンおよびポリマー複合材料:レビュー
- リチウムイオン電池の電気化学的性能が向上したLiNi0.8Co0.15Al0.05O2 /カーボンナノチューブの機械的複合材料
- リチウムイオン電池用のCr3 +およびF-複合ドーピングを用いたLiNi0.5Mn1.5O4カソード材料の合成と電気化学的性質
- リチウムイオン電池用の効率的なアノード材料としての数層のMoS2 /アセチレンブラック複合材料
- スーパーキャパシターの電極材料としての階層的多孔質構造を持つ単分散カーボンナノスフェア
- RGOと3次元グラフェンネットワークが高性能でTIMを共同修正
- 水性ナトリウムイオン電池用の高電気化学的性能材料としてのNa4Mn9O18 /カーボンナノチューブ複合材料
- スーパーキャパシター用途の電極としてのグラフェン/ WO3およびグラフェン/ CeOx構造の評価
- 高度に圧縮耐性のあるスーパーキャパシタ電極としての超弾性と高静電容量を備えたグラフェン/ポリアニリンエアロゲル
- リチウムイオン電池のアノード材料としてのマグネシウム-熱還元によって製造された埋め込みSi /グラフェン複合材料
- Co3O4ナノワイヤの環境にやさしく簡単な合成とリチウムイオン電池でのグラフェンによるそれらの有望な応用



