新規エモジン負荷ステアリン酸-g-キトサンオリゴ糖ナノミセルの調製と評価
要約
この研究の目的は、エモジンをロードしたステアリン酸-g-キトサンオリゴ糖(CSO-SA / EMO)を調製および特性評価し、その抗腫瘍活性をinvitroで評価することでした。この研究では、ステアリン酸-g-キトサンオリゴ糖を担体として使用し、その物理化学的特性をさまざまな方法で測定しました。細胞取り込み挙動は、FITC標識ステアリン酸-g-キトサンオリゴ糖を使用して調べました。 CSO-SA / EMOは、超音波処理と透析を使用して調製しました。粒子サイズ、表面電位、捕捉効率、および薬物放出挙動をインビトロで研究した。胃癌細胞に対するCSO-SA / EMOの効果は、MTTアッセイとフローサイトメトリーを使用して調査されました。結果は、CSO-SA / EMOの粒子サイズがステアリン酸-g-キトサンオリゴ糖よりも大きく、電位が小さいことを示しました。 MGC803およびBGC823細胞による12時間のミセル取り込みは十分であり、ミセルはマウスの病変部位に豊富に蓄積することができ、したがって良好な受動的EPRターゲティングを達成しました。 MTTおよび細胞周期停止アッセイは、遊離エモジンと比較して、MGC803およびBGC823細胞に対して有意にCSO-SA / EMO増強抗腫瘍活性を示しました。腫瘍体積、ヘマトキシリンおよびエオシン染色、およびターミナルデオキシヌクレオチドトランスフェラーゼdUTPニックエンドラベリングアッセイは、CSO-SA / EMOがinvivoで腫瘍組織に有意な抗腫瘍効果を有することを証明しました。結論として、超音波透析法は、CSO-SA / EMOを調製するための簡単で効果的な方法を提供しました。ミセルシステムを使用したエモジンの送達は、その抗腫瘍効果を効果的に改善しました。
はじめに
エモジン(EMO)は、ルバーブ、カスピダタム、マルチフローラムなどの伝統的な中国のハーブから主に抽出される天然のアントラキノン誘導体です。漢方薬(TCM)は、毒性が低く、副作用が少なく、コストが低いため、臨床研究で広く使用されています[1]。
研究によると、EMOには、免疫抑制、抗百日咳、抗高血圧、抗炎症、抗菌、および抗癌作用を含む幅広い薬理作用があります。 EMOは癌細胞の増殖を阻害し[2,3,4]、関連する遺伝子を調節して腫瘍細胞のアポトーシス、腫瘍形成、細胞増殖、浸潤、および転移を制御することがわかっています[5,6,7,8,9]。研究によると、EMOは、ヒト結腸直腸腺癌細胞、肝癌細胞、リンパ性白血病細胞[10]、およびヒト舌癌SCC-4 [11]などの多様な癌細胞を阻害できることが示されています。 EMOは、胃がん、乳がん、および前立腺がんの腫瘍細胞の増殖を抑制することができます[7、12]。しかし、EMOは、正常なヒト歯肉線維芽細胞[13]、ヒト気管支上皮細胞[14]、およびヒト乳腺細胞[15]などの正常細胞に対して細胞毒性効果を示しません。これらは、EMOが正常細胞と比較して腫瘍細胞に対して選択的な細胞毒性を示すことを示しています。
天然の多糖類であるキトサンは、キチンの脱アセチル化された形態です。この天然高分子は、優れた水溶性、生体機能性、血液適合性、微生物分解性を備えており、さまざまな生物医学的用途で知られています。酸性条件下でキトサナーゼを用いて高分子量キトサン(450 kDa)を分解し、低分子量キトサンオリゴ糖(CSO、18 kDa)を得た。 CSOは細胞膜に強く浸透することができ[16]、ステアリン酸(SA)は糖タンパク質経路を介して核に入ることができます。 CSOは、両親媒性ステアリン酸-g-キトサンオリゴ糖(CSO-SA)を合成するためのカップリング試薬としてカルボジイミド(EDC)を使用して、SAで疎水的に修飾されました。
EMOは広範な生物活性を持っていますが、そのアントラキノン構造は水に溶けにくいです。治療薬は血流を介して輸送されるため、その溶解度は吸収と分布に直接影響します。 CSO-SA移植片は、水溶液中で自己組織化して、内側が疎水性で外側が親水性のナノミセルを形成します。超音波プローブを使用して、集めた状態からナノミセルを分散させました。 EMOとCSOはどちらも疎水性であるため、EMOはミセルの中心にカプセル化されていました。
いくつかのモデル薬物がCSO-SAに適用されます。これには、モデル薬物の分子量、構造、および疎水性が必要です。既存の研究には、クルクミン[17]、ドキソルビシン[18]、ステアリン酸ラミブジン[19]、およびオキサリプラチン[20]が含まれ、これらは抗腫瘍効果を大幅に改善することができます。 CSO-SA / EMOの最適な負荷条件を検討しました。 CSO-SA / EMOは、より高い溶解性と利用効率を備えた新しい剤形を作成します。 CSO-SA / EMOは、モデル薬物または担体の選択、およびミセルの臨床応用のためのアイデアを提供できます。
実験資料と方法
実験資料
BALB / C + / nu雄ヌードマウスは、浙江大学実験動物センターから入手した。低分化胃癌細胞株MGC803およびBGC823はATCCセルバンクから購入しました。 RPMI-1640培地とFBSは、Hangzhou Holly Leaf BiotechnologyCompanyから入手しました。 EMO、MTT、FITC、Hoechst 33342、DiR、トリニトロベンゼンスルホン酸、およびピレンは、SigmaAldrichから提供されました。浙江大学はCSO-SAを提供しました。購入した他の試薬はARグレードのものでした。
CMCと 1 の決定 CSO-SAのHNMRスペクトル
このレポートでは、CSO-SAの臨界ミセル濃度(CMC)は、蛍光プローブとしてピレンを使用した蛍光分光光度法によって決定されました。様々な濃度のCSO-SA溶液をピレンアセトン溶液に加え、その後アセトンを一晩蒸発させた。異なる濃度のCSO-SA溶液中のピレンの発光スペクトルとピーク値を蛍光分光光度法で分析しました。最初のピーク( I 1 =374 nm)および3番目のピーク( I 3 =385 nm)のスペクトルが記録されました。横軸に対数濃度(Log C)をプロットし、 I 1 / 私 3 縦座標として、ポリマーミセルのCMCを計算しました。
CSOとCSO-SAはD 2 に溶解しました 10 mg / mlの濃度のO。 1 H NMRスペクトルを記録、比較、分析して、特徴的なCSOおよびCSO-SAピークを調べました。
検出されたアミン置換度
アミン置換度(SD%)は、トリニトロベンゼン硫酸(TNBS)法を使用して検出されました。
異なる濃度のCSOおよびCSO-SA溶液を調製し、その後4%NaHCO 3 と0.1%TNBSを連続して追加しました。水浴中で37℃で2時間インキュベートした後、2 mol / L塩酸を加えた。吸光度は、超音波処理の30分後に紫外可視分光光度法によって344nmで測定されました。標準曲線を描き、CSO-SAサンプルのSD%を計算しました。
CSO-SAの粒子サイズと可能性
1.0 mg / mlのCSO-SA溶液を調製し、超音波セルディスラプタープローブでミセルを完全に分散させました。 CSO-SAの粒子サイズと電位は、粒子サイズと表面電位アナライザーを使用して決定されました。
CSO-SAの細胞取り込み
FITCおよびCSO-SA溶液を混合し、一晩撹拌し、透析バッグに移しました。未反応のFITCと無水エタノールは、脱イオン水で24時間透析することにより除去しました。最後に、1.0 mg / mLの濃度のFITC標識CSO-SA(FITC-CSO-SA)溶液が得られました。
MGC803およびBGC823細胞を標的細胞として使用して、CSO-SAの細胞取り込みを調べた。細胞増殖率に基づいて、細胞を24ウェルプレートに播種し、完全に付着するまで一晩培養しました。次に、80μLのFITC-CSO-SA溶液を設定された時点で添加しました。細胞を10μLのHoechst33342(1 mg / mL)と15分間インキュベートして、細胞核を染色しました。 FITC-CSO-SAによるCSO-SAの取り込みは、レーザー走査型共焦点顕微鏡によって検出されました。
CSO-SAのinvivo配布
インビボでのCSO-SAの分布は、DiR蛍光色素染色によって決定された。 CSO-SA / DiR溶液は透析によって調製されました。
実験モデルとして6週齢の雄ヌードマウスを使用した。ヌードマウスに1×10 8 を皮下接種した / mLMGC803セル。 CSO-SA / DiRは、約200mm 3 の腫瘍細胞体積で尾静脈を介して投与されました。 。次に、マウスを設定された時点で麻酔した。 CSO-SA / DiRの生体内での時間分布は、小動物の生体イメージャを使用して記録されました(波長範囲、580〜700 nm、露光時間1000 ms)。
HPLCによるEMO濃度の検出
EMO濃度はHPLCで測定しました。 EMOは、保護カラム(4.6×10 mm、5μm)を備えたEclipse XDB-C18パックドカラム(4.6×250 mm、5μm)に適用されました。カラム温度は30°C、流量は1.0 mL / min、検出波長は254 nm、注入量は20μLに設定しました。移動相はメタノール/0.1%リン酸(85:15、v / v)でした。 EMO濃度を横軸に、ピーク面積を縦軸にプロットしました。最適な線形範囲を決定するために、EMOの標準曲線が描かれました。カラムを保護するために、HPLCで注入されたすべてのサンプルを0.45μmの有機フィルターでろ過しました。
CSO-SA / EMOの準備
この研究では、EMOは超音波プローブでカプセル化されました。出発点として、10%の初期配合比(EMO:CSO-SA、w / w)を使用しました。 EMO溶液を、氷浴中のミセル溶液に滴下してゆっくりと加えた。次に、超音波プローブを20サイクル適用しました(400 W、作業2 s、停止3 s)。
薬物を充填したミセルを透析バッグ(MWCO、3.5 kDa)に移し、脱イオン水に対して24時間透析して、溶媒からエタノールを除去しました。純粋なCSO-SA / EMOは、透析液を遠心分離して遊離EMOを除去することで得られました。
CSO-SA / EMOの特性(粒子径ポテンシャル、TEM、EE%)
CSO-SA / EMOの粒子サイズと表面電位は、粒子サイズと表面電位アナライザーで測定されました。
0.1 mg / mlのCSO-SA / EMO溶液を、炭素膜で覆われた銅線に滴下し、2%リンタングステン酸で染色して乾燥させました。 CSO-SA / EMOの形態と粒子サイズは透過型電子顕微鏡で観察されました。
CSO-SA / EMOの捕捉効率(EE%)と薬物負荷(DL%)は、有機溶媒抽出とHPLCによって検出されました。 CSO-SA / EMOミセル溶液の200μLサンプルに、1.8 mLのメタノールを添加してミセルを分散させ、薬物を抽出しました。 EMO濃度はC EMO として測定されました。 。さらに400μLのCSO-SA / EMOミセル溶液を限外ろ過遠心分離管に入れ、遠心分離(12,000 rpm、5分)して上清を得ました。 EE%とDL%は、次の式に従って計算されました。
$$ \ mathrm {EE} \%=\ left(10 \ times {C} _ {\ mathrm {EMO}}-C \ right)\ times V / {M} _ {\ mathrm {EMO}} \ times 100 \%$$$$ \ mathrm {DL} \%=\ left(10 \ times {C} _ {\ mathrm {EMO}}-C \ right)\ times \ mathrm {V} / \ left [\ left( 10 \ times {C} _ {\ mathrm {EMO}}-C \ right)\ times V + {M} _ {\ mathrm {CSO}-\ mathrm {SA}} \ right] \ times 100 \%$$ここで C EMO ミセル中のEMOの濃度、 C 限外濾過遠心分離後の薬物負荷ミセルのEMO濃度、 V 透析を受けた薬物負荷ミセルの量、 M EMO は、薬物の装填中に投与されるEMOの量です。 M CSO-SA はCSO-SAの質量です。
インビトロでの薬物放出の評価
CSO-SA / EMOからの薬物放出は、放出媒体としてPBS(pH 7.2)を使用して調査されました。 1ミリリットルの薬物を充填したミセル溶液を3.5kDaの透析バッグに入れ、両端を密封してから、チューブを含む適切な放出媒体に入れました。透析バッグを37℃の水平サーモスタットシェーカーに入れました。設定された時点でサンプルを採取し、同量の新鮮な放出培地と交換しました。サンプル中のEMOの含有量は、HPLCによって決定され、放出されたEMOの累積量が計算されました。
CSO-SA / EMOの細胞毒性
CSO-SA / EMO、CSO-SA、およびEMOで処理された胃癌細胞の生存率はMTTアッセイによって検出されました。細胞を96ウェルプレートに約10 5 の濃度で播種しました。 / ml。 CSO-SA / EMO、CSO-SA、およびEMOをさまざまな濃度で添加しました。さまざまな時間のインキュベーション後、20μLのMTTワーキング溶液を添加しました。 4時間のインキュベーション後、200μLのDMSOを添加し、570 nmでの溶液の光学密度(OD)をマイクロプレートリーダーで測定しました。
細胞周期に対するCSO-SA / EMOの影響
2つの細胞株の細胞を6ウェルプレートに10 5 の密度で播種しました。 / mL。 12時間の培養後、CSO-SA、CSO-SA / EMO、およびEMOを添加し、24時間インキュベートしました。次に、細胞を消化し、収集し、そして洗浄した。次に、500μLのPI染色液を各細胞サンプルに添加し、細胞ペレットをゆっくりと再懸濁し、細胞を暗所で37℃で30分間インキュベートしました。赤色蛍光は、488nmの励起波長でフローサイトメーターによって検出されました。 DNA含有量はFlowJoソフトウェアによって分析されました。
InVivoおよび組織学的分析によって評価されたCSO-SA / EMOの抗腫瘍効果
動物実験は、浙江大学の動物管理使用ガイドライン委員会に従って実施されました。 MGC803セル(1×10 6 )5〜6週齢のオスのヌードマウスの右前脇腹に皮下注射した。腫瘍を直径約5mmまで成長させた。その時点で、マウスをランダムに対照群、EMO注射群およびCSO-SA / EMO注射群に分け、各群に3匹の動物を入れた。すべてのマウスに、関連する試薬を尾静脈から1日1回2週間静脈内注射しました。電子ノギスを使用して、腫瘍の長径(a)と短径(b)を測定しました(b)。腫瘍体積は、式 V に従って計算されました。 =a×b 2 / 2。各マウスの体重を記録した後、組織学的分析のために腫瘍を収集した。腫瘍抑制率は、ヘマトキシリンおよびエオシン(HE)染色後の腫瘍組織で測定されました。ターミナルデオキシヌクレオチドトランスフェラーゼdUTPニックエンドラベリング(TUNEL)は、製造元の指示に従って、insitu細胞死検出キットを使用して回腸末端組織の細胞アポトーシスを検出するために実行されました。
結果と考察
CMCおよび 1 CSO-SAのHNMRスペクトル
両親媒性ポリマーは、親水性媒体中でミセルに自己集合します。より低いCMCはより大きなミセル形成をもたらしました。これは、静脈内投与後のミセル構造の維持に有益でした。 CSO-SAがミセルを形成すると、ピレン蛍光プローブがミセルの疎水性コアに容易に侵入し、荷電ピレンの蛍光強度が増加し、発光スペクトルの強度が増加します。この時点で、私 3 I よりも大幅に速く増加しました 1 したがって、 I 1 / 私 3 蛍光強度比が急激に低下しました。 I で重要なブレークポイントが観察される可能性があります 1 / 私 3 プロットとLogC値(図1)。変曲点の計算では、CMCは179.02μg/ mLであることが示されました。 CMCが小さいほど、ミセルを形成する能力が強くなり、希釈に対する耐性が強くなり、静脈内投与後のミセル構造の保護が向上します。
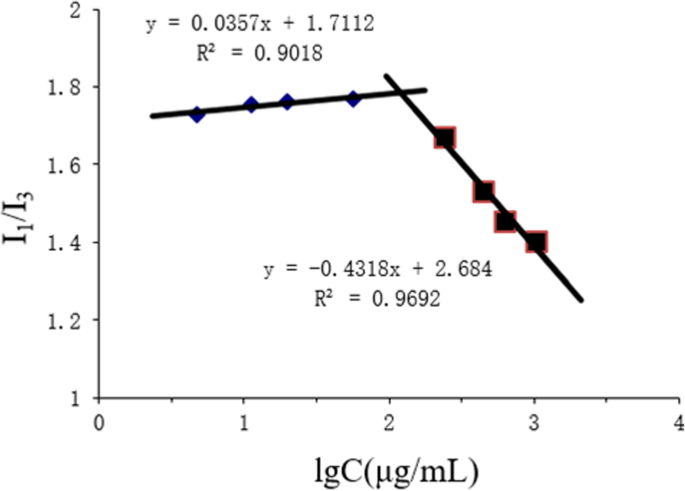
蛍光強度比の変化( I 1 / 私 3 )対CSO-SAの対数濃度
EDCは、SAのカルボキシル基と反応し、活性中間体-OO-アシルイソ尿素誘導体を形成するための架橋カップリング剤として使用されました。これは、CSOの第一級アミン基と反応してアミド結合を形成する可能性があります。 CSO-SAの構造は、核磁気共鳴陽子スペクトルに基づいて決定および確認されました。 1 H NMR(400 MHZ、D 2 O)δ1.06(m、CH2)、1.02(m、CH3)は、それぞれSAのメチレンプロトンとメチルプロトンに対応します。
アミノグループの代替度
CSO-SAのSD%は、キトサンのステアリン酸置換アミノ基のパーセンテージです。 TNBSはキトサンの遊離アミノ基と反応し、344nmでUV吸収を示すトリニトロベンゼン誘導体を形成しました。キトサンのトリニトロベンゼン誘導体の標準曲線は、344nmでのUV吸収によって決定されました。 CSO-SAのSD%は9.3±8%と計算されました。これにより、CSOとSAがグラフト率に基づいて正常にリンクされていることが確認されました。
CSO-SA、CSO-SA / EMOの粒子サイズと可能性
表1は、CSO-SAのZ平均が139.3±2.2nmであることを示しています。 PDIは0.179±0.03であり、比較的均一な分散を示しています。 CSO-SAと比較して、CSO-SA / EMOのZ平均とPDIは増加しました。 EMOをロードした後、CSO-SA / EMOの表面正電荷はCSO-SAのそれよりも高かった。
<図>細胞の取り込み
FITCはCSO-SAの物理化学的性質に影響を与えませんでした。フルオレセインFITCをCSO-SAにグラフトすることによりFITC-CSO-SAを得た。細胞をHoechst33342で染色した後、共焦点レーザー走査顕微鏡を使用してFITC-CSO-SA細胞の取り込みを観察しました。 MGC803の取り込みは時間の経過とともに徐々に増加し、FITC蛍光は徐々に増加することがわかりました。 BGC823のミセル取り込みは、時間依存的にMGC803と同様でした。 FITC-CSO-SAは細胞透過性が高く、胃がん細胞の細胞質に均一に分布していました(図2)。
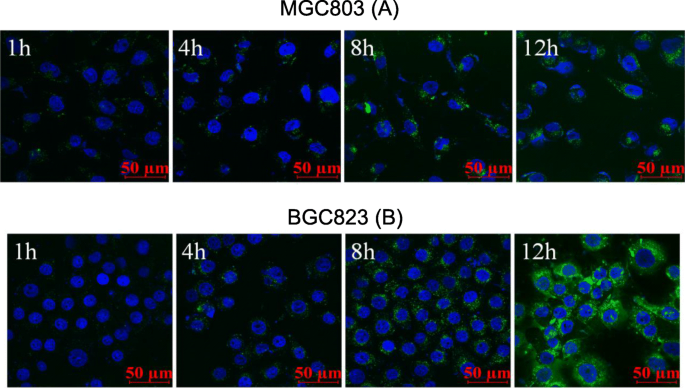
MGC803におけるCSO-SAミセルのinvitro細胞時間依存性取り込み( a )およびBGC823( b )それぞれ1、4、8、12時間のセル(青、Hoechst 33342、緑、FITC、スケールバー=50μm)
CSO-SA InVivoの配布
近赤外線(NIR)イメージング技術は、生体材料や組織に浸透するのに有利です。 CSO-SA / DiRをヌードマウスの尾静脈に注射した後、CSO-SA / DiRの分布を観察し、小動物の生体イメージャーを使用してさまざまな時間に記録しました。図3に示すように、CSO-SA / DiRの分布は、尾静脈注射後4時間で他のミセルと同様であり、主に肝臓、脾臓、および腫瘍組織に分布していました。腫瘍内のナノミセルの分布は、時間の経過とともに強度が徐々に増加しました。これは、主にナノミセルのEPR効果により、CSO-SAグラフトが優れた受動的ターゲティング能力を持っていることを示しています(図3)。
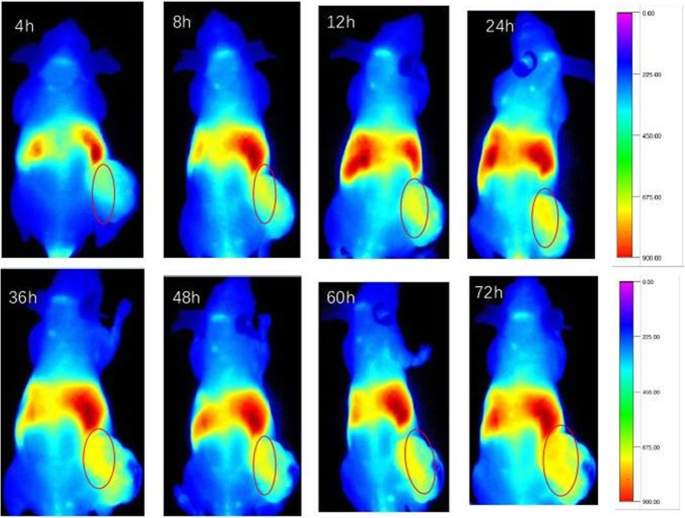
静脈内投与後のさまざまな時点でのCSO-SA / DiRの全身画像。注射
CSO-SA / EMOの準備
薬物負荷に対するさまざまなpH環境の影響
CSO-SA溶液を調製し、CSO-SAのpHを調整して、薬物負荷に対するpHの影響を調査しました。図4に示すように、CSO-SAは良好な薬物負荷容量を持ち、pH 6.4〜6.8の範囲で放物線状の傾向を示しました。最高レベルの薬物負荷はpH6.6で見られ、この値が薬物負荷に最適なpHになりました(図4)。
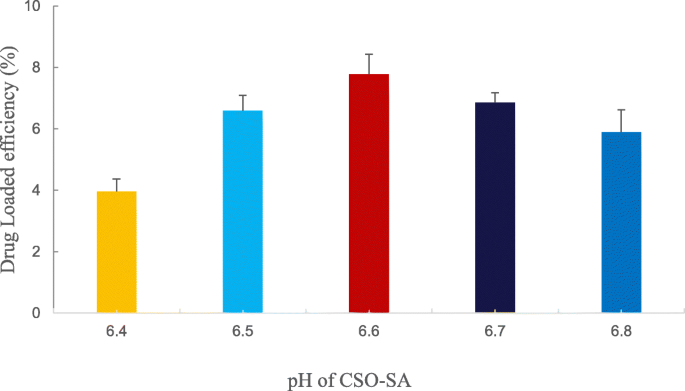
薬物負荷に対するCSO-SAグラフトの異なるpH値の影響。データは平均値±SD( n =3)
カプセル化効率、TEM、および薬物負荷
CSO-SAは自己組織化してシェルコアナノコンポジットミセルになります。疎水性部分は自発的に疎水性コア構造を形成し、親水性媒体をはじきます。この構造は、EMOがその疎水性構造のために疎水性コアに容易にカプセル化できるため、薬物負荷の重要な手段を提供します。 EMOの投与量を変化させることにより、EMOの負荷容量に対するCSO-SAの影響を調査しました。図5に示すように、EMOの投与量を増やすと、薬物の負荷量が増加します。 CSO-SAの負荷率は、比率が30%のときに21.16%に達しました(図5)。
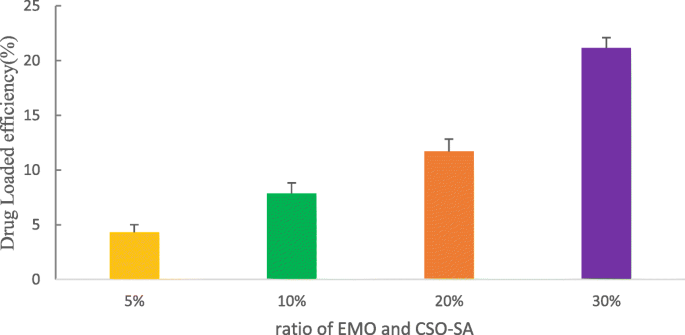
薬物負荷に対するEMOとCSO-SAの異なる比率(5-30%)の影響。データは平均値±SD( n =3)
CSO-SA / EMOは透過型電子顕微鏡で30,000倍に拡大されました。ナノミセルの形状とサイズが観察され、記録されました。
CSO-SA / EMOからのEMOリリース
薬物を充填したミセル溶液を3.5kDaの透析バッグに加え、PBS(pH 7.2)を放出媒体として使用しました。サンプルを取り除くたびに、同じ量の新しい放出培地と交換しました。
異なる時点でのEMOの濃度は、HPLCによって決定され、その後、累積放出パーセンテージが計算されました。図6に示すように、CSO-SA / EMOは、遊離EMOと比較して有意な徐放効果を示しました。これらの結果は、遊離EMOの放出率が0.5 hで38.4%であったのに対し、CSO-SA / EMOからのEMOの放出率は約6.6%であることを示しています。 4時間後の遊離EMOの放出率は83.7%、CSO-SA / EMOの放出率は約32.5%でした。 72時間以内に、CSO-SA / EMOからのEMOの放出が78.4%であったのに対し、無料のEMOの放出は97.2%に達しました。 EMOは、主に2つの方法でCSO-SA / EMO薬物負荷ミセルから放出されました。ミセル核からのEMO解離と、ミセルコアから放出媒体への浸透です。
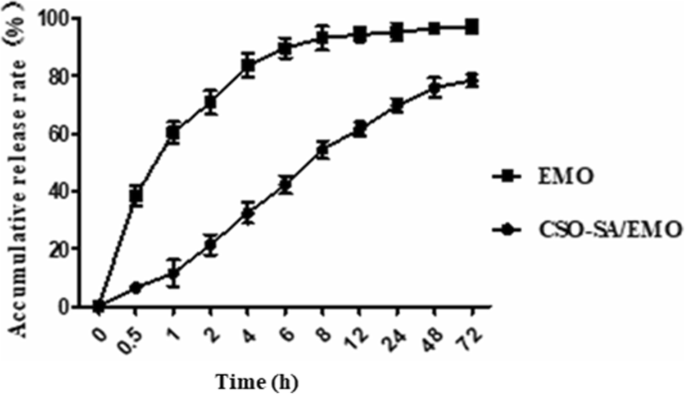
72時間にわたるCSO-SA / EMOからのEMOリリースプロファイル。グラフのエラーバーは標準偏差( n )を表します =3)
CSO-SA / EMOの胃がん細胞に対する毒性
MTTアッセイは、細胞生存率を検出するための標準的な方法です。遊離EMO、CSO-SA、およびCSO-SA / EMOのMGC803およびBGC823胃癌細胞に対する細胞毒性を、MTTアッセイを使用して測定しました。それは、EMOおよびCSO-SA / EMOがMGC803およびBGC823細胞を用量および時間依存的に阻害できることを示した。ただし、同じ濃度では、CSO-SA / EMOは、遊離EMO溶液と比較してMGC803およびBGC823細胞に対してより高い阻害効果を示しました。 IC 50 胃癌細胞のEMOおよびCSO-SA / EMOの値(表2)を計算しました。 IC 50 CSO-SA / EMOの値は、各時点(24 h、48 h、72 h)でEMOの値よりも大幅に低かった。 IC 50 CSO-SAの値は、CSO-SAが生物学的毒性がほとんどない安全な生物学的担体であることを示し、CSO-SA / EMOの細胞毒性がEMOによって引き起こされたことを確認しました(図7)。
<図>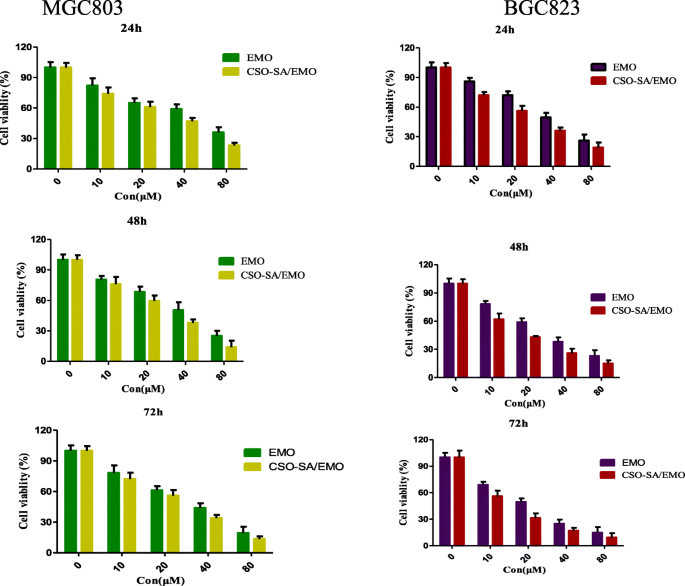
CSO-SA、EMO、およびCSO-SA / EMOで24時間、48時間、および72時間処理されたMGC803およびBGC823胃癌細胞の細胞生存率。データは平均値±SD( n =3)
表2および図7は、CSO-SA / EMOドラッグデリバリーシステムの細胞毒性が遊離EMOの細胞毒性よりも有意に高いことを示しています。ただし、invivo環境でのCSO-SA / EMOと遊離EMOの放出をシミュレートした場合、遊離EMOの放出は0.5時間で38.4%に達しましたが、CSO-SA / EMOの放出はわずか6.6%でした。全体として、遊離EMOの濃度は、各時点でCSO-SA / EMOの濃度よりも高かった。
この現象は簡単に説明できます。 CSO-SA / EMOはEMOを比較的ゆっくりと放出しましたが、CSO-SA / EMOの抗腫瘍効果は遅くなったり低下したりしません。多くの研究は、ナノドラッグデリバリーシステムが化学療法薬の抗腫瘍活性を改善できることを示しています[21]。
まず、遊離EMOは最初の活性バーストを示しますが、EMOは細胞に効率的に取り込まれませんが、CSO-SAはエンドサイトーシスまたは食作用によって細胞の取り込みを大幅に加速しました。
第二に、CSO-SA / EMOが細胞膜に近づくと、ナノ粒子と細胞膜の間の相互作用が、ナノミセルの構造と特性、およびイオンチャネルなどの生体高分子の機能に影響を与える可能性があります。したがって、CSO-SA / EMOを細胞膜に付着させると、単純な物理吸着は生じませんが、細胞の動的バランスが変化し、CSO-SA / EMOの細胞毒性がさらに促進される可能性があります。
最後に、遊離EMOは疎水性のアントラキノン構造を持っているため、血中の分布が悪くなります。 CSO-SA / EMOドラッグデリバリーシステムは、EMOの溶解性を高め、溶解性を改善して、周囲の細胞の分子濃度を高めます。
FCMによる細胞周期停止の検出
細胞周期分析は、悪性腫瘍の臨床治療の重要な側面です。薬剤感受性期間中の腫瘍細胞へのサイクル特異的薬剤の適用は、大きな効果があることが示されています。臭化エチジウム類似体は正常な細胞に浸透することはできませんが、損傷した細胞膜に浸透することで細胞核を染色することができます。 PIを埋め込んだ二本鎖DNAは赤色の蛍光を発し、蛍光強度は二本鎖DNAのレベルに比例します。 DNA含有量は、PIでDNA染色した後、フローサイトメトリー(FCM)によって決定されました。細胞周期の分布とアポトーシスは、DNA含有量の分布に基づいて分析されました。
研究によると、EMOは細胞周期の分布に影響を及ぼします[11、22]。 FCM分析は、CSO-SA / EMOおよびEMOが細胞周期のG2 / M期にMGC803およびBGC823細胞をブロックできることを示しました。
MGC803細胞は、同じ濃度(20μM)のCSO-SA、遊離EMOおよびCSO-SA / EMO溶液に24時間曝露されました。 G2 / M期のMGC803細胞の割合は、それぞれ8.95%、15.29%、23.12%でした。対照群の割合は6.47%でした。同じ条件下で20μMCSO-SA、遊離EMO、またはCSO-SA / EMOで処理されたG2 / MのBGC823細胞の割合は、それぞれ14.25%、16.79%、35.71%であり、対照群よりも高い値でした。 (13.66%)。これらのデータは、CSO-SA / EMOがMGC803およびBGC823細胞のG2 / M期を、同じ濃度の遊離EMOよりも効率的かつ有意にブロックしたことを示しています。 CSO-SAは、コントロールとの違いを示しませんでした(図8)。
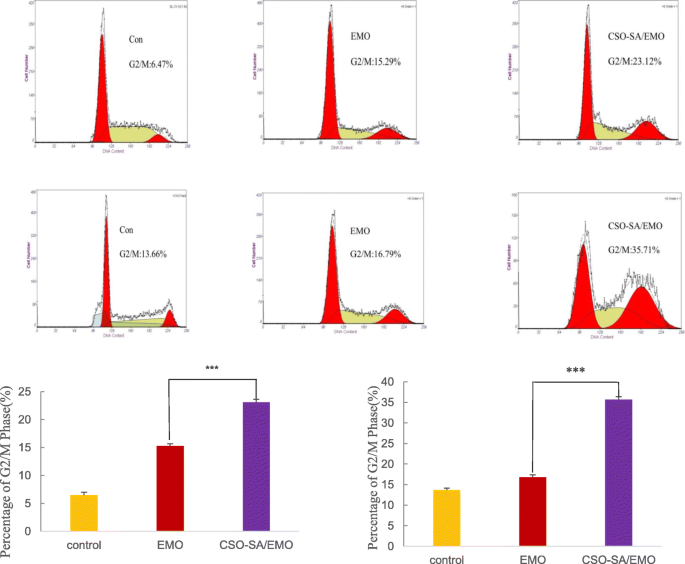
EMOおよびCSO-SA / EMOで24時間処理したMGC803およびBGC823細胞の細胞周期分布。学生の t テストが計算され、データは平均値±SD( n =3)、(* p <0.05、 ** p <0.005、 *** p <0.001)
CSO-SA / EMO InVivoの抗腫瘍効果
CSO-SA / EMOの抗腫瘍効果をさらに研究するために、腫瘍阻害率と細胞アポトーシスレベルをinvivoで評価しました。結果は、CSO-SA / EMOとEMOの両方が腫瘍増殖に対して顕著な阻害効果を持っていることを示しました(図9a)。 CSO-SA / EMO群の腫瘍抑制率はEMO群の3倍でした(図9d)。各グループのマウスの体重は有意に変化しなかった(図9b)。これは、CSO-SA / EMOとEMOの両方が比較的安全であることを示しています。各グループの腫瘍組織における形態学的変化とアポトーシスは、CSO-SA / EMOが有意な抗腫瘍効果を持っていることを示しました(図9e、f)。
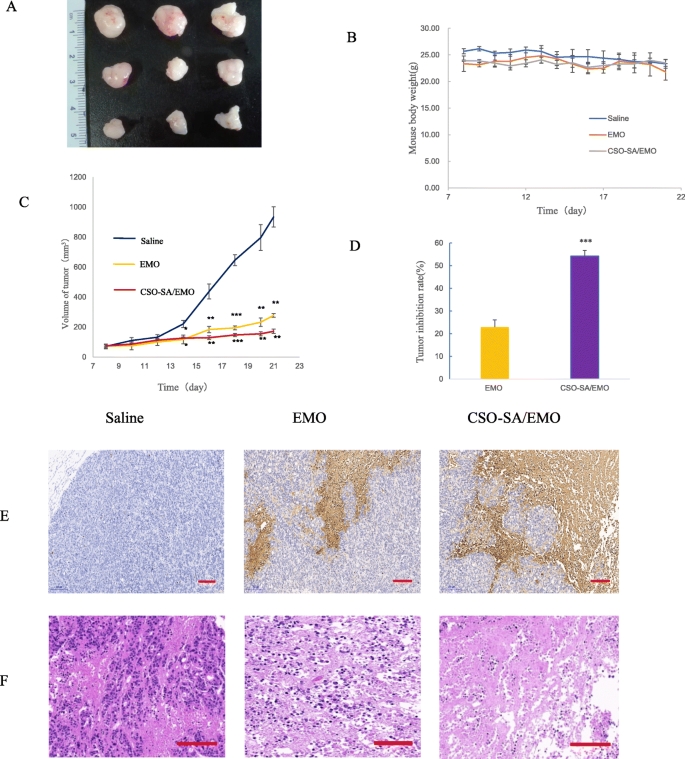
インビボでのCSO-SA / EMOの抗腫瘍効果。 a 各グループの腫瘍の形。 b 各グループのマウスの体重。 c 各グループの腫瘍体積。 d 腫瘍抑制率。 e 各グループのTUNEL染色腫瘍組織の代表的な画像(スケールバー=200μm)。 f 各グループのHE染色腫瘍組織の代表的な画像(スケールバー=200μm)
結論
この研究では、さまざまな方法でCSO-SAの構造、CMC、SD%、粒子サイズ、およびポテンシャルを検出しました。結果は、両親媒性CSO-SAが担体として良好に機能したことを証明しています。胃癌細胞の蛍光強度は、CSO-SAが12時間以内に急速に取り込まれたことを示しました。ヌードマウスは、72時間以内のCSO-SAの分布を研究するためのモデルとして使用されました。時間の経過とともに、病変内のCSO-SA分布はより集中し、優れた受動的ターゲティング効果を示しました。
CSO-SA/EMO was prepared with ultrasound-dialysis method. CSO-SA had strong drug-loading capacity. When environment pH was set at 6.6, the level of drug loading reached 21.6% at a 30% formulation ratio. Compared with CSO-SA, CSO-SA/EMO had bigger particle size and zeta potential. The shape of CSO-SA/EMO could be recorded directly using TEM. The release of EMO from CSO-SA/EMO was 78.4% within 72 h, it indicated a smooth and continuous process in body. Considering the antitumor effect of CSO-SA/EMO compared with free EMO, we confirmed it with various experiments.
CSO-SA toxicity to gastric cancer cells was detected by MTT assay. The results showed that CSO-SA was a safe biological carrier. Compared with that of free EMO, CSO-SA/EMO significantly enhanced the antitumor activity against gastric cancer cells. MGC803 and BGC823 cell cycle could be arrested in the G2/M phase more effectively by CSO-SA/EMO. Tumor volume, HE staining, and TUNEL assay proved more significant antitumor effect of CSO-SA/EMO than free EMO.
Based on above results, CSO-SA is both biocompatible and safe carrier. CSO-SA/EMO in this study utilizes a new and effective dosage formulation for the treatment of cancer and exhibits good passive targeting effect in vivo.
データと資料の可用性
この調査中に生成または分析されたすべてのデータは、この公開された記事に含まれています。
略語
- CSO-SA:
-
Chitosan oligosaccharide-stearic acid
- EMO:
-
Emodin
- FITC:
-
Fluorescein isothiocyanate
- MTT:
-
Thiazolyl blue tetrazolium bromide
- TEM:
-
透過型電子顕微鏡
- 1 H NMR:
-
Proton nuclear magnetic resonance
- EPR:
-
強化された透過性と保持力
- TCM:
-
Traditional Chinese medicine
- CMC:
-
Critical micelle concentration
- Log C:
-
Logarithm of concentration
ナノマテリアル
- コバルトをドープしたFeMn2O4スピネルナノ粒子の調製と磁気特性
- ポリマーナノ構造上のU2OS細胞におけるアクチンと接着斑組織の分析
- TiO2ナノ流体に向けて—パート1:準備と特性
- Sb /パリゴルスキー石(PAL)ナノ粒子の調製と強化された接触水素化活性
- In VivoCTイメージングおよび腎クリアランス特性のための新しい生体適合性AuNanostars @PEGナノ粒子
- ZnOナノ結晶の合成と逆ポリマー太陽電池への応用
- 中空構造LiNb3O8光触媒の調製と光触媒性能
- パラジウム(II)イオンインプリント高分子ナノスフェアの調製と水溶液からのパラジウム(II)の除去
- ITO / PtRh:PtRh薄膜熱電対の調製と熱電特性
- 小胞および細胞の周波数変調波誘電泳動:クロスオーバー周波数での周期的Uターン
- 新規SrTiO3 / Bi5O7Iナノコンポジットの製造と光触媒特性



