銅ナノ粒子の合成と安定化におけるグリーン熟達度:触媒、抗菌、細胞毒性、および抗酸化活性
要約
銅ナノ粒子(CuNPs)は、高い表面積対体積比、高い降伏強度、延性、硬度、柔軟性、剛性などの並外れた特性により、非常に興味深いものです。 CuNPは、多くの異なるアプリケーションで、細胞毒性および抗癌特性とともに、触媒、抗菌、抗酸化、および抗真菌活性を示します。レーザーアブレーション、マイクロ波支援プロセス、ゾルゲル、共沈殿、パルスワイヤー放電、真空蒸気堆積、高エネルギー照射、リソグラフィー、機械的粉砕、光化学還元、電気化学など、多くの物理的および化学的方法がナノ粒子の合成に使用されてきました。 、エレクトロスプレー合成、熱水反応、マイクロエマルジョン、および化学還元。ナノ粒子の植物合成は、細胞毒性が低く、経済的見通しがあり、環境に優しく、生体適合性が高く、抗酸化作用と抗菌作用が高いため、物理的および化学的方法の貴重な代替手段として提案されています。このレビューでは、CuNPの準備に使用される特性評価手法、その主な役割、制限、および感度について説明します。 CuNPの合成に使用される技術の概要、合成手順、合成されたCuNPの特性に影響を与える反応パラメーター、およびさまざまな植物の植物化学物質を特定するために使用されるスクリーニング分析は、レビューおよび要約された最近の公開文献から提示されます。 。ケルセチンによる銅イオンの還元、サンチンによる銅ナノ粒子の安定化、抗菌活性、および4-ニトロフェノールの還元の仮想的なメカニズムが図解されています。このレビューの主な目的は、CuNPの合成に使用された植物のデータを要約し、研究者が過去に使用されていない植物を調査するための新しい経路を開くことでした。
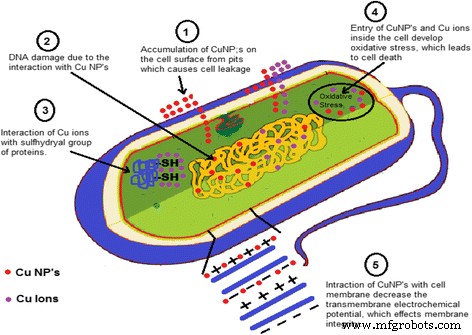
銅ナノ粒子の抗菌活性のために提案されたメカニズム。
背景
ナノ粒子(NP)は、宇宙技術、磁気、オプトエレクトロニクスおよびエレクトロニクス、化粧品、触媒、製薬、生物医学、環境、およびエネルギーのアプリケーションなど、産業分野で多くの興味深いアプリケーションを持っています[1、2]。延性、高降伏強度、硬度、柔軟性、剛性、高表面積対体積比、マクロ量子トンネリング効果、量子サイズなどのNPの並外れた特性は、同じ化学組成を持つバルク材料の特性と比較して起因します[3 ]。実際、NPの特性は、微粒子で観察される特性とはかなり異なる可能性があり、比表面積が大きく、光学特性が高く、融点が低く、磁化、機械的強度が高く、多くの産業用途があります[4]。銅ナノ粒子(CuNP)は、入手が容易で、コストが低く、貴金属と同様の特性を備えているため、非常に興味深いものです[5、6、7、8、9]。 CuNPは、センサー、熱伝達システム[10,11,12]、および電子機器(燃料電池および太陽電池)で、多くの反応の触媒として、また病院設備のコーティングに使用される殺菌剤および抗菌剤としても使用できます[13,14、 15,16,17,18,19]。
レーザーアブレーション[20]、マイクロ波支援プロセス、ゾルゲル[21]、共沈殿[22]、パルスワイヤー放電[23]、真空蒸気堆積[24]、高エネルギー照射[24]を含む多くの物理的および化学的方法。 25]、リソグラフィー[26]、機械的粉砕[27]、光化学還元、電気化学[28,29,30,31,32]、エレクトロスプレー合成[33]、熱水反応[34]、マイクロエマルジョン[35]、および化学還元ナノ粒子を合成するために使用されます。物理的および化学的方法は明確で純粋なナノ粒子を生成しますが、これらの方法は有毒な化学物質を使用しているため、費用効果も環境にも優しいものではありません。ナノテクノロジーの最も重要な基準の1つは、環境に優しく、毒性がなく、クリーンなグリーンケミストリー手順の開発です[36]。したがって、ナノ粒子の生合成には、植物[37、38]、放線菌[39、40]、真菌[41,42,43,44]、細菌[45,46、 47,48,49]、酵母[50,51,52]、およびウイルス[53,54]。生物学的実体は、さまざまなサイズ、物理化学的特性、形状、および組成を持つNPを合成するための、毒性がなく、クリーンで、環境に優しいアプローチを提供します[55]。
銅ナノ粒子は、 Euphorbia esula などのさまざまな植物を使用して合成され、文献で安定化されました。 [56]、ザクロ [57]、オシマムサンクタム [58]、イチョウ葉 [59]、 Calotropis procera [60]、 Lawsonia inermis [61]、柑橘類の医療機関 [62]、 Camellia sinensis [63]、チョウセンアサガオ [64]、 Syzygiumaromaticum [65]、ゴマのしるし [66]、柑橘類のレモン 、ターメリッククルクミン [67]、グロリオサ L. [68]、フィカスカリカ [69]、 Aegle marmelos [70]、 Caesalpinia pulcherrima [71]、カシア瘻 [72]、 Leucas aspera 、 Leucas chinensis [73]、 Delonix elata [74]、アロエベラ ミラー[75]、 Thymus vulgaris [76]、フィランサスエンブリカ [77]、マグノリアコブシ [78]、ユーカリ [79]、 Artabotrys odoratissimus [80]、 Capparis zeylanica [81]、 Vitis vinifera [82]、 Hibiscus rosa-sinensis [83]、 Zingiber officinale [84]、チョウセンアサガオ [85]、 Zea mays [86]、 Urtica 、カモミール 、 Glycyrrhiza glabra 、チョウセンゴミシ 、 Inula helenium 、シナモマム [87]、 Dodonaea viscosa [88]、 Cassia auriculata [89]、アザディラクタインディカ 、ランタナカメラ 、 Tridax procumbens [90]、 Allium sativum [91]、アスパラガスアドセンデンス 、バコパモニエリ 、 Ocimum bacilicum 、 Withania somnifera [92]、スミシアセンシティバ 、 Colocasia esculenta [93]、キョウチクトウ [94]、および Psidium guajava [95]; 褐藻などのさまざまな藻類/菌類を使用する [96]、キウロコタケ [97]、および Hypocrea lixii [98]; Pseudomonas fluorescens などの微生物を使用します [99]および Enterococcus faecalis [100]文化。
銅ナノ粒子の生合成
抽出に使用される植物の部分
葉、種子、樹皮、果実、皮、コイア、根、ガムなどの植物抽出物の調製には、植物のさまざまな部分が使用されます。葉と根は2つの方法で使用されます。第一に、新鮮な葉と根が植物抽出物の調製に使用され、第二に、乾燥した葉と根が粉末状で使用されます。
CuNPの合成手順
CuNPsの合成のために、植物抽出物は、異なる植物の異なる部分を使用して調製されました。目的の植物の抽出物部分を合成するために、葉を収集し、水道水で洗浄し、次に蒸留水で洗浄して、ほこりの粒子を除去します。洗浄した葉はさらに2つの方法で使用されます。まず、これらの葉を1〜2時間天日乾燥して、残留水分を取り除きます。これらの天日干しの葉の既知の重量は小さな部分に分割され、脱イオン水またはエタノール溶液に浸されます。この混合物をマグネチックスターラーを使用して室温で24時間撹拌し、さらに使用するためにろ過します。次に、これらの葉を4〜7日間天日乾燥するか、50°Cのオーブンで1日間乾燥させ、国産のブレンダーを使用して粉末にします。既知の重量の植物粉末を水またはエタノール溶液に混合し、攪拌してろ過します。
CuNPの合成では、硫酸銅、塩化銅、酢酸銅、硝酸銅などのさまざまな濃度の前駆体塩の水溶液を植物抽出物と混合します。水酸化ナトリウムの水溶液も調製され、pH媒体を制御するために反応混合物に添加されます。反応混合物を電気シェーカー内で異なる時間間隔で強く振とうし、オーブン内で異なる時間間隔および異なる温度で加熱する。 CuNPの形成は室温でも起こり得、反応混合物の色を変えることによって確認されます。最後に、ナノ粒子を遠心分離し、さまざまな温度で乾燥させました。反応の最適化は、混合物のpH、前駆体塩の濃度、加熱時間、および反応混合物の温度を変更することによって行われます。文献では、表1に示すように、さまざまな反応条件でさまざまな前駆体塩を使用して銅ナノ粒子を形成するためにさまざまな植物が使用されています。表から、さまざまな反応条件が銅の形状とサイズに影響を与えることがわかります。ナノ粒子。
<図>NPのプロパティに対する反応パラメータの影響
植物抽出物の濃度は、CuNPの削減と安定化に主要な役割を果たします。植物抽出物の濃度を上げることにより、粒子数が増えることが報告されています[88]。植物抽出物の濃度を上げることにより、植物化学物質の濃度が増加し、銅塩の減少も増加しました。金属塩の急速な還元により、ナノ粒子のサイズも減少しました[101]。
CuNPのサイズと構造は、銅塩の影響を大きく受けます。塩(例えば、塩化銅、酢酸銅、硝酸銅、または硫酸銅)が水酸化ナトリウムの存在下で使用されると、ナノ粒子の形態が変化します。塩化銅の場合は三角形と四面体、酢酸銅の場合は棒状、硫酸銅の場合は球形であることが報告されています[102]。前駆体塩の濃度を上げることにより、CuNPのサイズも大きくなりました。
CuNPの合成は、反応媒体のpHを好ましい範囲内で変化させることによって最良の結果をもたらします。ナノ粒子のサイズは、反応混合物のpH値を変更することによって制御されました。より高いpHでは、より小さなサイズのナノ粒子が、より低いpH値で得られたものと比較して得られた。この違いは、植物抽出物による金属塩の還元率の違いに起因する可能性があります。 pH値とナノ粒子のサイズの逆の関係は、pH値の増加により小さなサイズの球状ナノ粒子が得られ、pH値の減少により大きなサイズ(棒状および三角形)のナノ粒子が得られることを示しました。さまざまなpH値(4、6、8、10、および12)の吸収スペクトルへの影響を図1に示します[36]。 CuCl 2 への植物抽出物の添加が報告されました CuNPの形成をもたらさなかったが、代わりに、CuNPは、反応混合物のpHを塩基性媒体に変えることによって得られた。同じ振る舞いがWuとChenによって観察され、pHがCuNPの合成に重要な役割を果たしていると結論付けられました[103]。
植物抽出物の調製に使用される植物の部分
銅ナノ粒子の植物合成のメカニズム
植物化学物質のスクリーニング:定性分析
植物化学物質スクリーニング分析は、さまざまな植物の植物化学物質を検出するために実行される化学分析です。表2に示すように、この分析には化学物質または化学試薬を含む新鮮な植物抽出物が使用されます[77]。
<図>金属の還元とNPの安定化のための植物化学物質
植物化学物質を使用したCuNPのグリーン合成は、NPの形状とサイズをより柔軟に制御できます(つまり、反応温度、植物抽出物の濃度、金属塩濃度、反応時間、反応混合物のpHを変更することにより)。反応媒体の色の変化は、金属イオンの還元とNPの形成を示しています。銅塩の緑色の還元は即座に始まり、銅ナノ粒子の形成は反応混合物の色の変化によって示されます。植物化学物質は、図2に示すように、最初に金属イオンを還元し、次に金属の核をナノ粒子の形で安定化するという主な役割を果たします。植物化学物質と金属イオンの相互作用およびこれらの植物化学物質の濃度は、CuNPの形状とサイズを制御します。
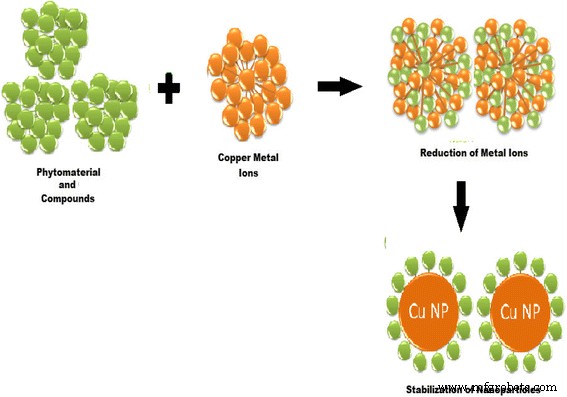
金属イオンを還元し、金属の原子核を安定化するためのプロトコル
フラボノイドには、 Ginkgo biloba などのさまざまな植物に存在するポリフェノール化合物(ケルセチン、カテキン、フラバノン、イソフラボン、サンチン、ペンデュレチン、アリザリン、ピノセムブリン、アントシアニン、フラボン、タンニン、サポニンなど)が含まれています。 [59]、柑橘類の医療機関 [62]、フィランサスエンブリカ [77]、 Hibiscus rosa-sinensis [83]、および Dodonaea viscosa [93]。これらの化合物は、金属の還元とキレート化に主要な役割を果たします。フラボノイドに存在するさまざまな官能基が銅イオンの還元に関与しています。フラボノイド中の反応性水素原子は、銅イオンを還元して銅核またはCuNPを形成することができるエノール型からケト型への互変異性体の変化の間に放出される可能性があると考えられてきた。たとえば、イチョウ葉の場合は 植物抽出物では、図3に示すように、エノール型からケト型への変化により、銅金属イオンが銅核またはCuNPに還元される主な役割を果たすのはケルセチン(フラボノイド)の変換です。
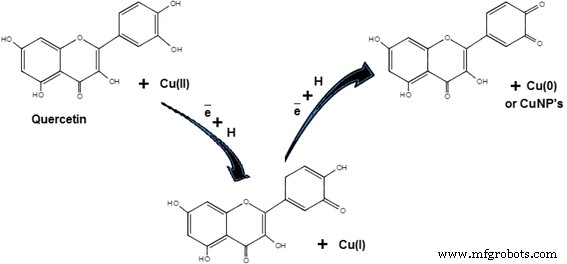
ケルセチンによる銅イオンの還元
CuNPの合成プロセス中に、一価または二価の酸化状態を持つ金属イオンがゼロ酸化銅核に変換され、これらの核が結合してさまざまな形状が得られます。核形成中に、核は凝集して、ワイヤー、球、立方体、棒、三角形、五角形、六角形などのさまざまな形状を形成します。一部のフラボノイドには、CuNPをπでキレート化する能力があります。 電子とカルボニル基。ケルセチンとサンチンは、ヒドロキシルとカルボニルを含む2つの官能基が存在するため、強力なキレート活性を持つフラボノイドです。これらのグループは、前のメカニズムに従って銅ナノ粒子とキレート化し、図4に示すようにCuNPの表面にサンチン(フラボノイド)を吸着する能力も説明します。
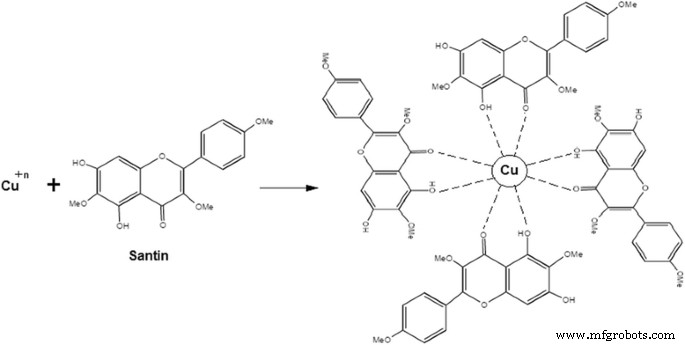
santinによる銅ナノ粒子の安定化
Hibiscus rosa-sinensis などのさまざまな植物のタンパク質分子(スーパーオキシドジスムターゼ、カタラーゼ、グルタチオン)が想定されていました。 [83]および Camellia sinensis [104]は、金属イオンからナノ粒子を形成するための高い還元活性を示しますが、それらのキレート活性は過度ではありません。 Camellia sinensis の単糖類(ブドウ糖)、二糖類(マルトースとラクトース)、多糖類などの糖 植物[63]は、還元剤または抗酸化剤として作用し、ケトンからアルデヒドへの一連の互変異性変換を行うことができます。
Hibiscus rosa-sinensis に存在するポリフェノール(エラグ酸や没食子酸など)などの他の植物化学物質 [40]、 Aegle marmelos のフェニルプロパノイド(フェニルアラニン、チロシン) [70]、 Ocimum sanctum のテルペノイド および Asparagus adscendens [58、92]、 Calotropis procera のシステインプロテアーゼ [60]、ターメリッククルクミン中のクルクミナニリンアゾメチン [67]、 Citrus Medicalinn のアスコルビン酸 [62]、 Syzygiumaromaticum のオイゲノール [65]、および Aegle marmelos のアルカロイド [70]は、銅イオンを還元し、銅ナノ粒子を安定化するのと同じ役割を果たします。 Phyllanthus emblica に含まれる炭水化物、アントラキノン、キノン、アントシアノシド [77]; Hibiscus rosa-sinensis のリグニンとキサントン [83]; Colocasia esculenta の強心配糖体、トリテルポノイド、カロテノイド配糖体、およびアントラキノン配糖体 植物[93]は、さまざまな植物の抽出物に存在し、還元剤および安定剤として作用する植物化学物質でもあります。構造を持つ特定の植物化学物質の例を図5に示します。
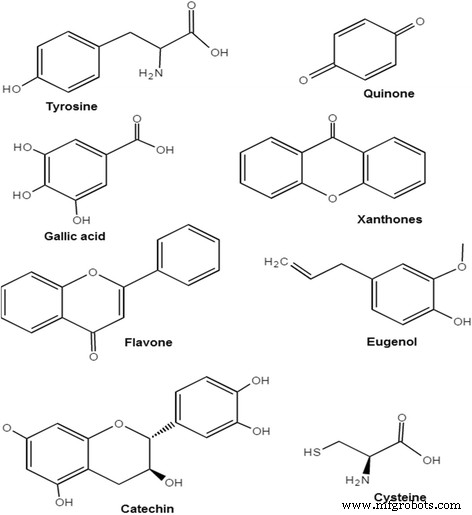
植物化学物質とその構造
特性評価手法
合成されたナノ粒子の特性評価には、紫外線可視分光法(UV-vis)、透過型電子顕微鏡(TEM)、小角X線散乱(SAXS)、フーリエ変換赤外分光法(FTIR)、X-などのさまざまな手法が使用されました。光線蛍光分光法(XRF)、X線回折(XRD)、X線光電子分光法(XPS)、走査型電子顕微鏡(SEM)、電界放出型走査電子顕微鏡(FESEM)、粒子サイズ分析(PSA)、Malvern Zetasizer( MZS)、エネルギー分散型X線分光法(EDX / EDS)、ナノ粒子追跡分析(NTA)、X線反射率測定(XRR)、Brunauer-Emmett-Teller分析(BET)、選択領域電子回折(SAED)、および原子力分光法(AFM)(表3)。
<図>銅ナノ粒子の用途
卓越した化学的および物理的特性、大きな表面積対体積比、常に再生可能な表面、低コスト、および無毒の調製により、CuNPはさまざまな分野での用途に大きな関心を集めてきました。銅ナノ粒子は、さまざまな用途で、触媒活性、抗菌活性、細胞毒性または抗癌活性、抗酸化活性、および抗真菌活性を示します。触媒活性では、銅ナノ粒子は、配位子を含まない条件下で多くの溶媒中のアルキンとアジドのホイスゲン[3 + 2]環化付加反応に使用されます[59]、1-メチル-3-フェノキシベンゼン、3,3-オキシビス(メチルベンゼン) [94]、1-置換1 H の合成 -1,2,3,4-テトラゾール[76]、二酸化窒素の吸着、および二酸化硫黄の吸着[66]。触媒作用のある遷移金属のほとんどで、ホスフィンなどのウルマンカップリング反応配位子が文献に報告されており、ほとんどの配位子は高価で、調製が難しく、湿気に敏感です。この作業では、合成された銅ナノ粒子を使用して、ジフェニルエーテルの配位子を含まないウルマンカップリングを行います。産業廃棄物に含まれるさまざまな染料や有毒な有機化合物や農薬は、環境や生物に非常に有害です。銅ナノ粒子は、メチレンブルー[73]、アトラジンの分解[86]、4-ニトロフェノールの還元[76]などのさまざまな染料の分解に使用されます。
抗菌剤の中で、銅化合物は、農業で除草剤[105]、殺藻剤[106]、殺菌剤[107]、農薬として、また畜産で消毒剤として一般的に使用されています[108](表4を参照)。生体銅ナノ粒子は、緑膿菌などのグラム陽性菌およびグラム陰性菌に対して強力な抗菌活性を示しました。 (MTCC 424)、 Micrococcus luteus (MTCC 1809)、エンテロバクターアエロゲネス (MTCC 2832)[57]、サルモネラ菌 (MTCC 1253)、 Rhizoctonia solani 、 Xanthomonas axonopodis pv。 citri 、 Xanthomonas axonopodis pv。 punicea [58]、 Escherichia coli (ATCC 14948)[62]、黄色ブドウ球菌 (ATCC 25923)、枯草菌 (ATCC 6633)、 Pediococcus acidilactici [69]、および Klebsiella pneumoniae (MTCC 4030)。抗真菌活性では、銅ナノ粒子が Alberteria carthami に対して使用されます 、 Colletotrichum gloeosporioides 、 Colletotrichum lindemuthianum 、 Drechslera sorghicola 、 Fusarium oxysporum f.sp. カルタミ 、 Rhizopus stolonifer 、 Fusarium oxysporum f.sp. ciceris 、 Macrophomina phaseolina 、 Fusarium oxysporum f.sp. udum 、 Rhizoctonia bataticola [58]、カンジダアルビカンス 、カーブラリア 、 Aspergillus niger 、および Trichophyton simii [67]。細胞毒性では、銅ナノ粒子がHeLa、A549、MCF7、MOLT4、およびBHK21細胞株(癌腫瘍)の研究に使用されます[60、104]。
<図>抗菌活性の仮説的メカニズム
CuNPは優れた抗菌活性を持っていることが観察され、文献では銅ナノ粒子の抗菌活性のメカニズムを示した報告は限られていますが、これらのメカニズムは架空のものでした。 CuNPと–SH(スルフヒドリル)基との相互作用により、細菌および酵素/タンパク質が破壊されることが観察されました[109、110]。 DNA分子のらせん構造がCuNPの相互作用によって乱されることも報告された[111]。 CuNPと細菌の細胞膜との相互作用は、膜貫通電気化学ポテンシャルを低下させ、膜貫通電気化学ポテンシャルの低下により、膜の完全性に影響を及ぼしました[112]。金属NPはそれぞれの金属イオンを放出すると想定されていました。銅ナノ粒子と銅イオンは細菌の細胞表面に蓄積し、膜に穴を形成し、細胞から細胞内への細胞成分の漏出を引き起こし、細胞死につながる酸化ストレスを引き起こします[112,113,114]。上記の可能性を表す抗菌活性の仮説的なメカニズムを図6に示します。
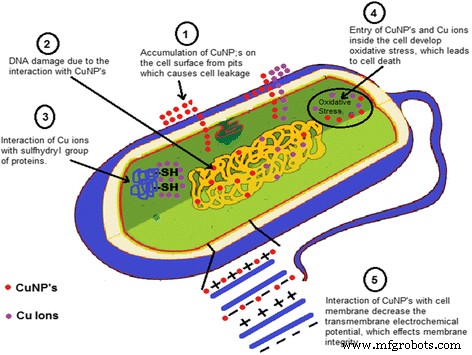
銅ナノ粒子の抗菌活性のメカニズム
4-ニトロフェノールの還元のための触媒活性
農業廃水や工業製品に通常見られる4-ニトロフェノール(4-NP)は危険であり、環境に優しいものではありません。 4-アミノフェノール(4-AP)に変換される4-NPの水素化または還元は、CuNPの存在下で行われます。 CuNPは、ドナーボロハイドレートイオンからアクセプター4-NPへの電子移動を支援することにより、反応を触媒して速度論的障壁を克服することができます。
合成されたCuNPの触媒活性は、水素化ホウ素ナトリウムの水溶液の存在下、室温で水性媒体中の4-ニトロフェノールの還元において研究されてきました[56]。 CuNPsを使用した4-NPの削減は、シンプルで環境に優しいプロセスです。 4-NPの還元のためのCuNPsの触媒効率は、UV-vis分光計を使用して調べられました。水性媒体中の4-NPの最大吸収ピークは317nmであり、4-ニトロフェノラートイオンの形成により水素化ホウ素ナトリウムを添加すると吸着ピークが403nmにシフトすることが観察されました。 403 nmのピークは、2日後も影響を受けませんでした。これは、触媒がないと4-NPの還元が起こらないことを示しています。 CuNPを追加した後、溶液の吸収ピークは300 nmにシフトし、403 nmのピークは完全に消失しました。これは、副産物なしで4-NPが4-APに還元されたことを示しています。 4-NPの還元の仮想的なメカニズムを図7に示します。このメカニズムでは、4-NPと水素化ホウ素ナトリウムがイオンの形で溶液中に存在します。水素化ホウ素イオンのプロトンは、銅ナノ粒子とBO 2 の表面に吸着しています。 生産。 4-ニトロフェノラートイオンもCuNPの表面に吸着します。プロトンと4-ニトロフェノラートイオンの両方が吸着するため、CuNPは反応物の速度論的障壁を克服し、4-ニトロフェノラートイオンは4-アミノフェノラートイオンに変換されます。変換後、4-アミノフェノールイオンの脱着が起こり、4-アミノフェノールに変換されます。
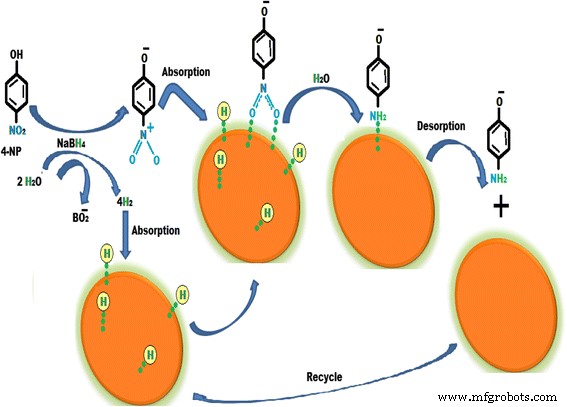
4-ニトロフェノールの還元のメカニズム
結論
この論文は、さまざまな植物を使用して銅ナノ粒子(CuNPs)を合成するために使用される生物学的方法の最近の情報をレビューして要約しました。 CuNPのグリーン合成は、細胞毒性が低く、経済的見通しがあり、環境に優しく、生体適合性が高く、実現可能性が高く、CuNPの抗酸化活性と抗菌活性が高い物理的および化学的方法の貴重な代替手段として提案されています。 NPの生合成のメカニズムはまだ不明であり、ナノ粒子の形成のメカニズムとNPの形成における植物化学物質の役割の理解に焦点を当てる必要があります。このレビューは、銅ナノ粒子の合成、合成手順、および合成されたCuNPの特性に影響を与える反応パラメーターで使用される植物のデータを提供します。植物化学物質スクリーニング分析は、さまざまな植物の炭水化物、タンニン、サポニン、フラボノイド、アルカロイド、アントラキノン、アントシアノシドなどの植物化学物質を特定するために使用される化学分析です。ケルセチンによる銅イオンの還元とサンチンによる銅ナノ粒子の安定化のメカニズムをこの論文で説明した。銅ナノ粒子の文献で使用されている特性評価手法は、UV-vis、FTIR、XRD、SEM、FESEM、TEM、PSA、MZS、EDX、NTA、SAXS、XRR、XRF、XPS、BET、SAED、およびAFMです。銅ナノ粒子は、さまざまな用途で、触媒活性、抗菌活性、細胞毒性または抗癌活性、抗酸化活性、および抗真菌活性を示します。この論文では、抗菌活性と4-ニトロフェノールの還元の仮想的なメカニズムを図で示しています。
さまざまな構造特性と効果的な生物学的効果を備えたCuNPは、今後数日間で新しいグリーンプロトコルを使用して製造できます。粒子サイズの制御、ひいてはCuNPのサイズ依存特性により、アプリケーションの新しい扉が開かれます。この研究では、植物抽出物、微生物抽出物、および天然に存在する生体分子を使用したCuNPの合成の概要を説明します。 CuNP合成のためのこれらすべてのグリーンプロトコルには独自の利点と制限がありますが、還元剤としての植物抽出物の使用は、以前のグリーン還元剤によるナノ粒子の生成速度が速いため、微生物抽出物の使用と比較してより有益です。
ナノマテリアル
- Escherichia coliに対する酸化銅ナノ粒子の生体合成、特性評価、および抗菌力の評価
- 小さなセレンナノ結晶とナノロッドの容易な合成と光学的性質
- Sb /パリゴルスキー石(PAL)ナノ粒子の調製と強化された接触水素化活性
- Agで装飾されたSnO2ミクロスフェアのワンポットグリーン合成:4-ニトロフェノールの還元のための効率的で再利用可能な触媒
- CuSナノ粒子でコーティングされた着色および導電性CuSCN複合材料の容易な合成
- 光触媒活性と安定性を強化するためのIn2O3ナノ粒子ハイブリッド双晶六角形ディスクZnOヘテロ構造の水熱合成
- 単分散二元FePt-Fe3O4ナノ粒子の合成のための後処理法
- 金および銀ナノ粒子のグリーン合成のためのPlatycodiRadix(Platycodon grandiflorum)からのPlatycodonサポニン
- 金属および金属酸化物ナノ粒子のグリーン合成と単細胞藻類Chlamydomonasreinhardtiiに対するそれらの効果
- リガンドを含まないイリジウムナノ粒子の容易な合成とそれらのinvitro生体適合性
- 単分散CoFe2O4 @ Agコアシェルナノ粒子のワンポット合成とその特性評価



