臨床イムノアッセイで使用されるPAMAMおよび量子ドットに基づく複合体のグループ
要約
臨床イムノアッセイで使用される複合体のグループを報告します。複合体には、PAMAM結合ヤギ抗ウサギIgGおよびQD結合ヤギ抗マウスIgGが含まれます。ウサギ抗原とマウス抗原を加えると、対応する抗原が検出されます。複合体を使用した実験は、単純で、便利で、時間も短く、ステップも短いです。また、FCM(フローサイトメトリー)、ICC(免疫細胞化学)、IHC(免疫組織化学)で使用してさまざまな種類の抗原を検出するなど、さまざまな実験方法にも適用できます。
はじめに
量子ドット(QD)は、蛍光量子収率が高く、光安定性が高く、光退色特性が低いため、発光体として広く使用されています。それらはまた、細胞イメージングおよびバイオテクノロジーアプリケーションにおける有機フルオロフォアとして広く使用されています。特に、カドミウムを含むQD(CdSeとCdTe)は、430〜660 nmの範囲内の同じ波長の照射下で、サイズに依存する放射電磁スペクトルを持っているため、大きな利点があります[1、2]。したがって、抗体結合QDは、分子イメージングの最も有望なプローブです。
ポリアミドアミンデンドリマー(PAMAM)は、最も広く深く研究されている樹枝状高分子の1つであり、次の特性を備えています。膨大な数の表面官能基、分子内の多数の空洞、ナノスケールサイズ、および高い生体適合性。これらのデンドリマーは、薬物や抗体と結合すると、薬物の溶解性と体循環を改善できますが、薬物の生物活性を妨げることはありません[3]。したがって、PAMAMで修飾された抗体は、臨床免疫によく使用されます。
臨床イムノアッセイには、WB、ELISA、IHC(免疫組織化学)、ICC(免疫細胞化学)、FCM(フローサイトメトリー)などの多くの方法が含まれます。その中で、特定の抗体プローブを利用するFCMは、細胞および分子レベルで単一細胞または他の生物学的粒子の迅速な分析を実行します。したがって、FCMは最も広く使用されているイムノアッセイの1つです。細胞スクリーニングを実施する場合は、対応する抗体プローブの使用で十分です。ただし、小タンパク質、ウイルス、サイトカインなどの小さな生体分子のスクリーニングが必要な場合は、FCMが小さなサイトカインを直接検出できないため、CBA(サイトメトリービーズアレイ)法を採用する必要があります。 CBA法は、表面に特異的な捕捉抗体で構築された色素標識ビーズを利用します。 CBAビーズをサンプルおよび対応する色素標識抗体と混合すると、ELISAの場合と同様にサンドイッチ複合体が形成され、FCMで小さな抗原を検出できます。
この研究では、PAMAM結合ヤギ抗ウサギIgGおよびQD結合ヤギ抗マウスIgGを含む複合体のグループを提示します。このグループの複合体は、FCM、ICC、およびIHCに使用できます。ウサギ抗原とマウス抗原を加えると、対応する抗原が検出されます。このモデルは、対応するマウスおよびウサギの抗体が存在する場合、小タンパク質、ウイルス、サイトカインなど、多くの種類の抗原を検出できます。スキーム1は、FCMで使用される複合体を示しています。例として、HSP27を取り上げます。 HSP27はHSPB1(熱ショックタンパク質ファミリーBナンバー1)としても知られており、薬剤耐性、細胞増殖、アポトーシス、腫瘍発生、転移などに関与する重要なタンパク質です[4、5]。このモデルでは、PAMAM結合ヤギ抗ウサギIgGは、CBA(サイトメトリービーズアレイ)ビーズと同様に、キャリアおよびキャプチャーとして機能し、FCMによって小分子抗原を検出できるようにします。 QD結合ヤギ抗マウスIgGは蛍光プローブとして機能します。抗原が膜タンパク質または細胞内タンパク質である場合、従来のFCM法を使用して抗原を検出できます。 QDを追加するだけで、PAMAM部分は追加できません。細胞内タンパク質や膜タンパク質の場合、細胞はFCM法で直接検出できる標的と見なすことができます。それらは、偽細胞を構成するためにPAMAM部分を必要としない。したがって、複合体を分割して個別に使用できます。
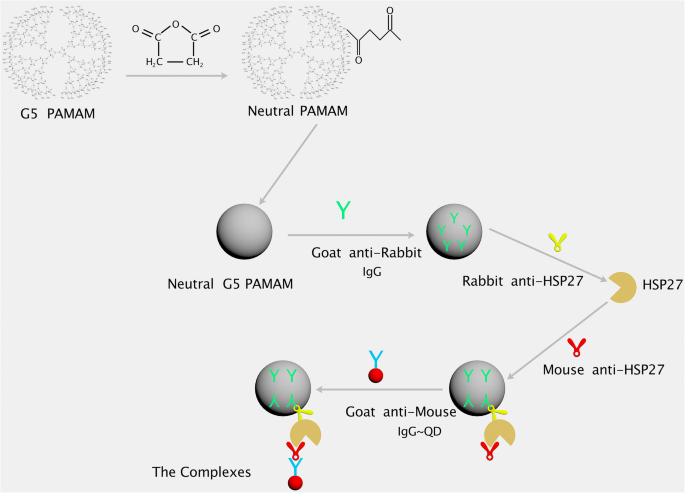
複合体がどのように形成され、HSP27を検出するためにFCMによって使用されるかの表現。まず、G5アミノPAMAMは無水コハク酸と反応して、中性のPAMAMを形成する必要があります
結果と考察
複合体のグループには、PAMAM部分とQDの部分の2つの部分が含まれます。 PAMAM部分は、PAMAM結合ヤギ抗ウサギIgGです。表面安定剤として第5世代アミノ末端PAMAMデンドリマー(G5 PAMAM)を使用し、水性環境に理想的な溶解特性を提供しましたが、このデンドリマーは抗体結合に有害な強い正電荷を持っています。正電荷を中和するために、PAMAMをDMSOに溶解し、無水コハク酸(ジヒドロ-2,5-ジケトテトラヒドロフラン)を添加してPAMAMアミノ基を中和しました。 PAMAMのアミノ基は無水コハク酸と反応してアミド結合を形成します[6,7,8,9,10]。反応後、透析、凍結乾燥、秤量、再溶解を行い、ほぼ中性となり、ヤギ抗ウサギIgGと結合できる「N-PAMAM」と名付けました。 PAMAM、特にG5 PAMAMには多数の空洞があり、IgGはG5PAMAMのボイドスペース内にカプセル化されている可能性があります[11]。ヤギ抗ウサギIgGを最初にMESバッファー(0.1 mol / L、pH 6.0)に溶解し、次にEDCとスルホ-NHS(1:1のモル比)を添加し、混合物を15分間インキュベートしました。最後に、N-PAMAM(ニュートラルPAMAM)を添加し、続いてシェーカーベッドで4℃で一晩インキュベートしました。このポリマーは水溶液中で自己組織化して、そうでなければ不溶性の低分子量ゲストをカプセル化したポリマーミセルを形成します[12]。反応後、未反応物質を除去するために透析が必要でした。次に、生成物を凍結乾燥し、秤量し、保存バッファーに再溶解し、最後に、N-PAMAM結合ヤギ抗ウサギIgGを作成しました。
MESにおけるN-PAMAM-IgG(ヤギ抗ウサギ)の蛍光およびUV-visスペクトルを図1に示します。N-PAMAM(中性PAMAM)およびIgGと比較して、N-PAMAM-IgGの蛍光発光ピーク最も強度が低かった。 UV-visスペクトルは、IgG、MESバッファー、PAMAM、およびN-PAMAMと比較して、N-PAMAM-IgGのみが200nmの波長に吸収ピークを持っていたことを示しています。蛍光スペクトルであろうとUV-visスペクトルであろうと、N-PAMAM-IgGはN-PAMAMおよびIgGと比較して異なる特性を示します。これは、N-PAMAMとIgGが単純に混合されるのではなく組み合わされていることを間接的に証明します。 N-PAMAM-IgGの抗体活性を検出するために、ELISAを実施した。図2に示すように、IgG(ヤギ抗ウサギ)抗体耐性は、N-PAMAMとのカップリング時に失われませんでした。
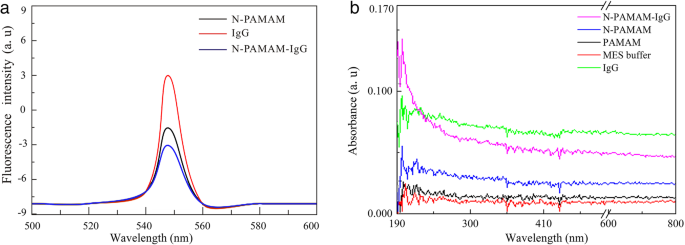
a MESにおけるPAMAM-IgG(ヤギ抗ウサギ)の蛍光スペクトル。励起波長は548nmでした。 b MESにおけるPAMAM-IgG(ヤギ抗ウサギ)のUV-visスペクトルと、ある範囲の波長にわたる発光スペクトル
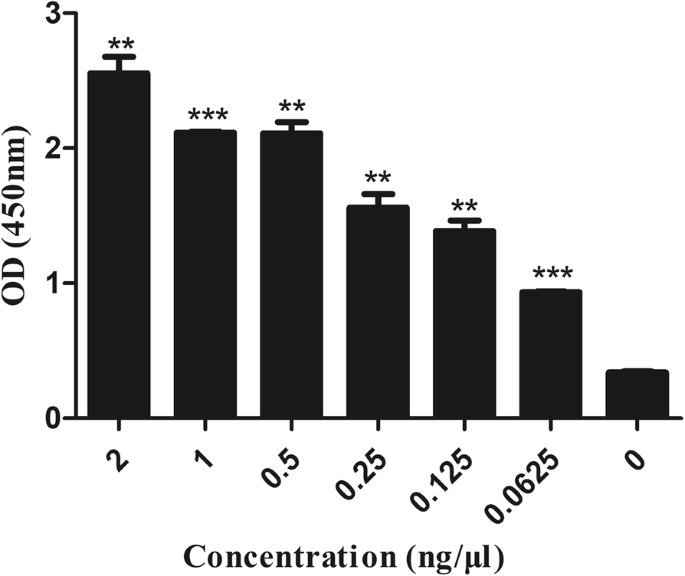
N-PAMAM-IgG(ヤギ抗ウサギ)抗体耐性を検出するためのELISA法。 N-PAMAM-IgGを抗原として使用し、さまざまな濃度に希釈しました。ウサギIgG-HRPは、N-PAMAM-IgGの耐性を検出するための抗体プローブとして使用されました。吸光度の測定は、450nmの波長で行われました
QDの部分は、QD結合ヤギ抗マウスIgGです。抗体結合QDは通常、クロスカップリング反応によって形成されます。クロスカップリング反応では、抗体分子がQDの表面のカルボキシル基やアミノ基などの官能基に結合します[13、14]。この研究では、カルボキシル配位子で安定化されたコア/シェルCdSe / ZnS水溶性量子ドットとEDC(1-エチル-3-(3-ジメチルアミノプロピル)-カルボジイミド塩酸塩)を使用したカルボジイミドカップリング反応を使用しました。この方法は、QDの表面に抗体を結合させるための最も一般的な方法の1つです[15、16、17]。 CdSe / ZnS QDのミセルは、最初にホウ酸緩衝液(5 mM BS、pH 7.2)中のEDCおよびスルホ-NHSの存在下でインキュベートされました。次に、ヤギ抗マウスIgGを添加し、混合物をシェーカーベッド内で4℃で一晩暗所でインキュベートしました。最後に、10%BSA(ウシ血清アルブミン)を添加して未反応のQDをブロックし、遠心分離と再溶解を続けて未反応の物質を除去することにより、生成物を精製しました。 QD結合IgG(ヤギ抗マウス)の抗体活性は、暗所で4°Cで保存した後、3か月間維持できます。
保存バッファー(2.5 mM BS、pH 8.0、0.1%BSA)中のQD-IgG(ヤギ抗マウス)およびQDの粒子サイズを図3aに示します。カップリング反応後、生成物の直径は明らかに大きくなり、生成物は良好な均質性と安定性を示した。これらの特性は、検出プローブとして使用するための鍵です。 QD-IgGとQDの蛍光スペクトルを図3bに示します。図3aに示すように、生成直径の増加は、IgGがQDと結合したことを示していますが、QD-IgGの蛍光発光ピークは同じでした。 QDとして。この結果は、IgGとQDのカップリングが、QDの光学特性を変化させなかったことを意味します。これは、イムノアッセイでのアプリケーションに役立ちます。 QDs-IgGの抗体活性を検出するために、PVDFメンブレンを用いたELISA法を使用しました。マウス抗AKT抗体を1μg/ ml、10μg/ ml、100μg/ ml、200μg/ mlの濃度に希釈し、4つの濃度勾配抗原をQDs-IgG(ヤギ抗マウス)とハイブリダイズさせました。 0.1 mg / mlの同じ濃度で。暗所で37℃で40分間ハイブリダイゼーションした後、PVDFメンブレンをPBST(pH 6.0、0.1%Tween 20)で3回洗浄し、PVDFメンブレンにUV光を照射しました。蛍光強度を図3cに示しました。蛍光強度は抗原濃度の増加とともに増加し、QDs-IgGが高い抗体活性を持っていることを示しています。
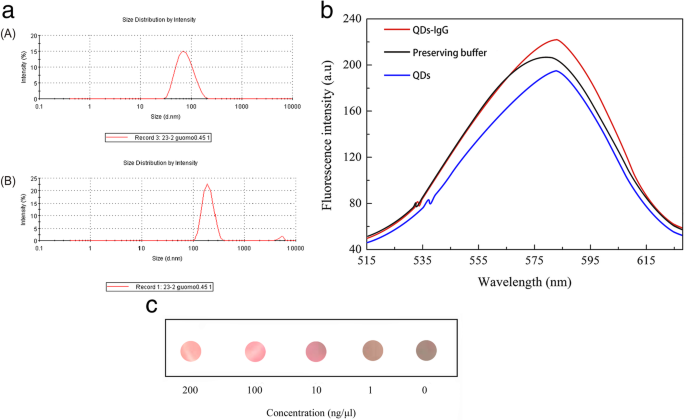
a QDおよびQD結合IgG(ヤギ抗マウス)の流体力学的直径の分布。 ( a )QDの直径と( b )QD-結合IgG(ヤギ抗マウス)。 QDの平均直径は64.87nmであり、QD-IgGの平均直径は211.4 nmであり、DLSによって検出されます。 b QD-IgG(ヤギ抗マウス)、QDおよび保存バッファー(2.5 mM BS、pH 8.0、0.1%BSA)の蛍光スペクトル。 QD-IgGの蛍光発光ピークはQDのピークと同じであり、IgGとQDのカップリングがQDの光学特性を変化させなかったことを示しています。 c QDs-IgG(ヤギ抗マウス)の抗体耐性を検出するELISA法、PVDF膜をUVで評価しました
このセクションでは、FCMでこのグループの複合体を利用する方法を紹介します。前述のように、小タンパク質、ウイルス、サイトカインなど、さまざまな種類の抗原を検出できます[18]。ここでは、HSP27タンパク質を例として使用し、プロセスを詳しく見ていきましょう。 HSP27は細胞質に存在し、腫瘍細胞、特に肺がん、膵臓がん、尿路上皮がん、腎臓がん、乳がん、メラノーマ皮膚がんに大量に分泌されます。 HSP27のごく一部が細胞外に分泌されるため、タンパク質を抽出するには細胞を溶解する必要があります。この実験では、MCF-7(ヒト乳がん細胞)をテストグループとして、L02(正常なヒト肝細胞)をコントロールグループとして2つの細胞株を選択しました。細胞を溶解して細胞内タンパク質を抽出した。総タンパク質を回収し、タンパク質濃度に応じてウサギ抗HSP27とマウス抗HSP27を添加し、37℃で50分間インキュベートしました。次に、N-PAMAM-IgGを混合物に添加し、混合物を37°Cで30分間インキュベートした後、2つの等しいグループ(テストグループとPAMAMグループ)に分けました。最後に、QDs-IgGをテストグループに追加し、37°Cで30分間暗所でインキュベートしました。図4は、フローサイトメトリーによる2つのグループの細胞の蛍光分析を示しています。テスト曲線の蛍光強度は、MCF-7グループのPAMAM曲線の蛍光強度よりもはるかに高かったのに対し、L02グループでは2つの曲線がほぼ重なっています。 HSP27が細胞抽出物に存在する場合、N-PAMAM-IgGとQDs-IgGは間接的に結合して、ウサギ抗HSP27とマウス抗HSP27の存在下でサンドイッチの組み合わせを形成します。 HSP27が存在しない場合、少量のQD-IgGのみが非特異的吸着によってN-PAMAM-IgGに結合します。したがって、テスト曲線の蛍光強度がコントロールPAMAM曲線の蛍光強度よりも高い場合、HSP27がサンプルに含まれています。図4は、MCF-7細胞がL02細胞よりも多くのHSP27タンパク質を分泌したことを示しています。
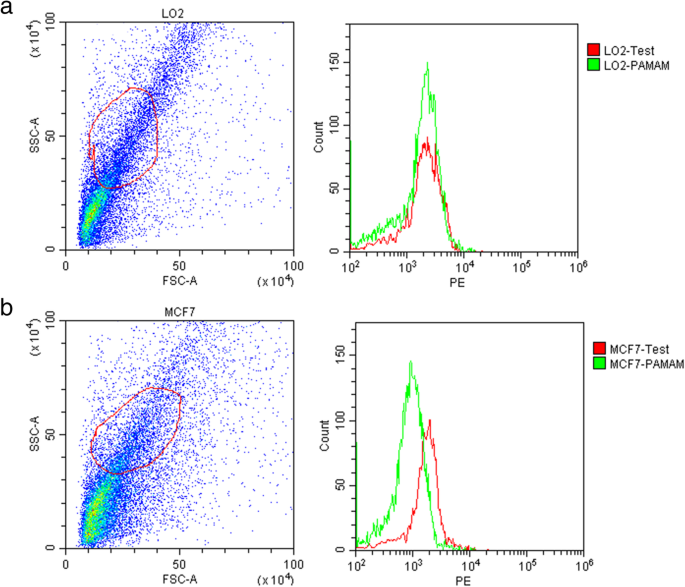
フローサイトメトリーによるHSP27の蛍光分析。 a L02セル。 b MCF-7細胞。試験群は、N-PAMAM-IgGおよびQDs-IgG、対照としてのPAMAM群とインキュベートされ、これは、FCMによって検出された微小分子タンパク質の偽細胞を形成するためにN-PAMAM-IgGとのみインキュベートされた。 2つの曲線がほぼ重なっている場合、サンプルにHSP27がないと判断できます。したがって、QDs-IgGを添加してもしなくても、蛍光強度は変化しません
上記のように、これらの複合体は、FCMによって分泌された細胞内タンパク質を検出することができます。原則として、これらの複合体はあらゆる種類の抗原に適用できます。さらに、組み合わせの2つの部分を別々に使用することができます。検出したい抗原が細胞内または細胞表面にある場合は、QDの部分しか使用できません。たとえば、β-アクチンは細胞に存在する細胞骨格の主成分の1つであり、真核細胞に広く存在します。図5aは、FCMによるHeLa細胞のβ-アクチンのQD部分のみを使用した蛍光分析を示しています。 HeLa細胞を洗浄し、メタノールで処理して細胞膜の浸透を促進し、2つの等しいグループに分けました。 β-アクチングループをマウス抗β-アクチンと37°Cで30分間インキュベートし、コントロールグループをBSAとインキュベートしました。 PBSで洗浄した後、両方のグループをQDs-IgG(ヤギ抗マウス)とともに37°Cで30分間インキュベートしました。 PBSで2回洗浄した後、両方のグループがFCMによって検出されました。 β-アクチン曲線の蛍光強度は、対照曲線の蛍光強度よりもはるかに高く、HeLa細胞にβ-アクチンタンパク質が含まれていることを示しています。
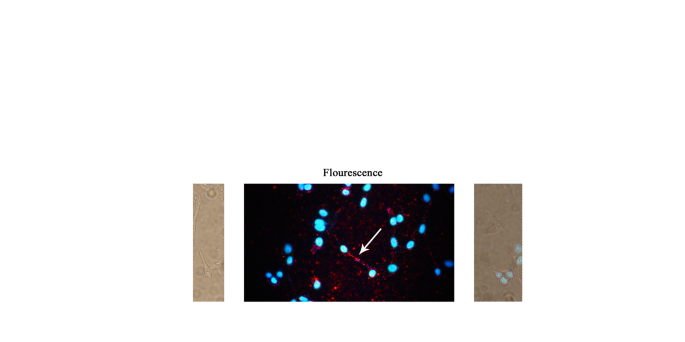
a HeLa細胞におけるβ-アクチンの蛍光分析。 β-アクチン群はマウス抗β-アクチンおよびQDs-IgG(ヤギ抗マウス)とインキュベートされ、対照群はBSAおよびQDs-IgGとインキュベートされました。対照群は、QD-IgGの非特異的吸着によって引き起こされるバックグラウンド蛍光の排除を可能にすることができます。 b UV-vis照射下でのHeLa細胞の蛍光顕微鏡画像。 DAPIは細胞核を染色し、青色の蛍光を発しました。 QDs-IgGはβ-アクチンと間接的に結合し、赤色蛍光を発しました。スケールバー20μm
さらに、これらの複合体はICCにも適用できます。ただし、ICCの場合、標的抗原は細胞内または細胞表面に存在し、大量に存在する必要があります[19]。そうしないと、実験対象を背景と区別することが困難になります。たとえば、β-アクチンタンパク質を取り、HeLa細胞を10cmの細胞板に播種し、顕微鏡のカバースリップをその中に置き、メタノールを使用して細胞を固定しました。次に、細胞をマウス抗β-アクチン(PBS、1%BSA)と37°Cで1時間インキュベートし、PBSTで2回洗浄し、QDs-IgG(ヤギ抗マウス)と37°Cでインキュベートしました。 1時間暗くします。 PBSTで2回洗浄し、細胞核をDAPIで染色した後、蛍光顕微鏡で蛍光を検出しました[20、21]。図5bは、HeLa細胞の蛍光顕微鏡画像を示しています。蛍光色素としてのQDの利点は、QDの信号とDAPI信号を紫外線チャネルの照射下で同時に観察できることです。したがって、核によれば、ターゲットは明らかに位置を特定することができます。この実験では、β-アクチンは細胞核周辺の細胞骨格タンパク質であり、明らかに観察することができます。
結論
結論として、FCMやICCなどの臨床イムノアッセイで使用される複合体のアプリケーションを示しました。複合体のグループには、PAMAM結合ヤギ抗ウサギIgGおよびQD結合ヤギ抗マウスIgGが含まれます。ウサギ抗抗原とマウス抗抗原を加えると、対応する抗原が検出されました。これらの複合体は、それらの広いスペクトル、高い生体適合性、高い光安定性、および低い生物学的毒性のために有利である。この複合体は、対応する一次抗体のみを変更する必要があるユニバーサルモデルです。この記事では、複合体を使用してHSP27とβ-アクチンを検出しましたが、理論的には、このプロセスはあらゆるタイプの抗原に適用できます。さらに、抗原の特性に応じて検出方法を選択したり、実際のニーズに応じて複合体を分割して個別に使用したりすることもできます。この方法では、小タンパク質やウイルスなどの小分子をフローサイトメトリーで検出することもできます。適切に改善すれば、免疫蛍光(IF)、ウエスタンブロット(WB)、イムノクロマトグラフィーストリップ(LCS)などの他の方法にも適用できると考えています。
メソッド/実験
資料
CdSe / ZnS量子ドット(カルボキシル基を持つ水溶性QD、cas番号N / A)は、中国のNEPQDから購入しました。 PAMAM(第5世代アミノ末端、ロット番号CYD-150A)は、中国のCYDから購入しました。ヤギ抗ウサギIgG(ab6702)およびマウス抗β-アクチン(ab8226)は、英国のアブカムから購入しました。マウス抗HSP27(BF0624)およびウサギ抗HSP27(AF6082)は、米国のAffinityから購入しました。ヤギ抗マウスIgG(bs0296G)は、中国のBiossから購入しました。 EDCとスルホNHSはThermoFisherから購入しました。 DMEMおよびウシ胎児血清はGibcoから購入しました。 PVDFメンブレン(0.2μm)はMilliporeから購入しました。他のすべての化学試薬は分析試薬グレードでした。
N-PAMAM-IgG(ヤギ抗ウサギ)の調製
- a)
N-PAMAM(中性PAMAM)の調製:PAMAM(G5アミノ末端、平均MW 28826)(60 mg、2.081 mM)をDMSO(2 ml)および無水コハク酸(ジヒドロ-2,5-ジケトテトラヒドロフラン)(0.266)に溶解しました。 g、2.66 mM)を加えてアミノ基を中和した。 1モルのG5PAMAM高分子には128モルのアミノ基があるため、60mgのPAMAMには0.266mMのアミノ基が含まれ、PAMAMアミノ基と無水コハク酸のモル比は約1:10です。次に、混合物をシェーカーベッドで100 rpmで4時間ブレンドし、その後、溶液を3500 MWCO透析膜で24時間透析し、凍結乾燥後にN-PAMAMを取得しました。
- b)
N-PAMAM-IgG(ヤギ抗ウサギ)の調製:製剤化されたMESバッファー(100 mM、pH 6.0)、次に100μlのMESバッファーをチューブに取り、20μMのEDC、および20μMのスルホ-NHSを加え、低速でボルテックスします。 35.7μlのIgG(pH、0.5μM)を加え、ボルテックスで攪拌します。その後、19μgのN-PAMAMを加え、4°Cで一晩インキュベートします。最後に、溶液を3500MWCOおよび8000MWCO透析膜で3日間透析します。凍結乾燥後、N-PAMAM-IgGが得られます。
QD-IgG(ヤギ抗マウス)の調製
- a)
BSバッファーの作成:
- 1。
ホウ砂バッファー(50 mM)を準備します。19.07gのホウ砂を量り、1Lの超純水に溶解します。
- 2。
ホウ酸緩衝液(50 mM)を準備します。ホウ酸3.09 gの重さを量り、1Lの超純水に溶解します。
- 3。
pH 8.0BSバッファーとpH7.2BSバッファーは、上記の2つの溶液を混合して調製しました。
- 4。
保存バッファーとしても使用される洗浄バッファーは、pH 8.0BSバッファーを5mMの濃度に希釈し、0.1%Tween20を添加して調製しました。
- 5。
活性化溶液は、pH 7.2BSバッファーを5mMの濃度に希釈し、0.1%Tween20を添加することによって調製しました。
- 6。
EDCバッファーは0.27gのEDCを5mlの活性化溶液に溶解して作成し、スルホ-NHSバッファーは0.378gのスルホ-NHSを5mlの活性化溶液に溶解して作成しました。
- b)
QD-IgG(ヤギ抗マウス)の調製:
まず、450μlのQD(CdSe / ZnS、5 mg / ml)を2.25 mlの活性化溶液に溶解し、次に150μlのEDCバッファーと150μlのスルホ-NHSバッファーを加え、溶液を氷上で5分間超音波処理しました。分。次に、溶液を12,000 rpmで5分間遠心分離して上清を除去し、沈殿物を1.2mlの洗浄バッファーに溶解しました。 30分間の超音波混合後、100μgのIgG抗体を添加し、溶液を4℃の温度でシェーカーベッド内で一晩インキュベートしました。第三に、150μlの10%BSAを添加した後、30°Cで30分間インキュベートし、12,000rpmで2分間遠心分離して上清を除去しました。沈殿物を1mlの洗浄バッファーに再溶解し、12,000rpmで2分間遠心分離しました。このステップを繰り返し、最後に沈殿物を1mlの保存バッファーに溶解しました。最後に、10%のBSAが追加されました。混合物を完全な超音波ショック混合で混合し、820 g / minで遠心分離して沈殿物を除去し、上澄みにQD-IgGを含めました。 QDs-IgGは、暗所で4°Cで3か月間保存する必要があります。サンプルは4°Cでしか保存できず、グリセリンを使用しても凍結できないことに注意してください。そうしないと、多数の量子ドットがクラスターに集まり、PBSTで洗い流すことができなかった沈殿物が形成され、深刻なバックグラウンド蛍光が発生します。
HSP27タンパク質のFCM分析
HSP27は細胞質に存在し、腫瘍細胞に大量に分泌されます。この実験では、MCF-7(ヒト乳がん細胞)をテストグループとして、L02(正常なヒト肝細胞)をコントロールグループとして2つの細胞株を選択しました。 2つのグループの細胞を10cmの培養皿に播種し、10%ウシ胎児血清(FBS)を含むダルベッコ改変イーグル培地(DMEM)で37℃で培養しました。細胞がプレートの80%を覆ったら、細胞をトリプシンで消化し、PBSで2回洗浄しました。次に、細胞を1mlのPBSに再懸濁しました。血球計算盤で細胞をカウントし、細胞濃度に応じてT-PER細胞溶解バッファーを加え、細胞溶解物から細胞内タンパク質を抽出しました。次に、細胞溶解物を14000rpmで10分間遠心分離して上清を収集し、タンパク質濃度をBCA法で測定し、タンパク質濃度に応じて、ウサギ抗HSP27およびマウス抗HSP27を添加し、 37°Cで50分。この実験では、L02のタンパク質濃度は約0.2 mg / ml、MCF-7は0.25 mg / ml、両方の容量は500μlでした。ウサギ抗HSP27とマウス抗HSP27の2つの抗体を細胞に添加しました(MCF-7に対して0.625μl、L02細胞に対して0.5μl)。
次に、1 mg / ml N-PAMAM-IgGを混合物に添加した後、37℃で30分間インキュベートしました。 6.25μlがMCF-7グループに追加され、5μlがL02グループに追加されました。インキュベーション後、生産は2つの等しいグループ、テストグループとPAMAMグループに分けられました。最後に、QDs-IgGをテストグループに追加し、37°Cで30分間暗所でインキュベートしました。次に、2つのグループの細胞をフローサイトメトリーで分析しました。
β-アクチンは、細胞骨格の主成分の1つであり、真核細胞に広く存在する細胞内タンパク質です。 HeLa細胞を10cmの培養皿に播種し、10%FBSを含むDMEMで37°Cで2日間培養した後、上清を除去し、細胞をPBSで2回洗浄しました。細胞をトリプシンで消化した後、細胞を800rpmで3分間遠心分離して上清を除去し、1mlの冷メタノールを加えて細胞を再懸濁しました。 5分後、細胞を800rpmで3分間遠心分離して上清を除去し、細胞を1mlのPBSに再懸濁しました。このステップを繰り返し、HeLa細胞を2つの等しいグループに分けました。試験群はマウス抗β-アクチンと37℃で30分間インキュベートし、対照群はBSA(ウシ血清アルブミン)とインキュベートしました。この実験では、マウス抗β-アクチンをPBST(1%BSA、5μg/ ml)に溶解し、100μlのIgGを300μlのテストグループに添加し、同量のBSAを対照群。 30分間のインキュベーション後、両方のグループをQDs-IgG(ヤギ抗マウス)とともに37℃で30分間インキュベートしました。 PBSで2回洗浄した後、両方のグループをFCMで評価しました。
HeLa細胞を10cmの培養皿に播種し、10%FBSを含むDMEMで37℃で1日間培養しました。次に、滅菌したカバーガラスを数枚セルディッシュに入れ、細胞をさらに2日間培養しました。カバースリップを取り外し、PBSで2回洗浄した後、カバースリップを400μlのメタノール中で20分間室温でインキュベートしました。カバースリップをPBSで3回洗浄した。次に、ブロッキングバッファーをPBST(0.1%Tween 20)、22.52 mg / mlグリシン、および10%BSAで調製しました。カバースリップをブロッキングバッファーに入れ、室温で30分間インキュベートしました。次に、ブロッキングバッファーを除去し、カバースリップをマウス抗β-アクチン(PBS、1%BSA)と37°Cで1時間インキュベートし、PBSTで2回洗浄し、QDs-IgG(ヤギ抗-マウス)37°Cで1時間暗所で。 PBSTで2回洗浄し、細胞核をDAPIで2分間染色した後、カバースリップをPBSで1回、蛍光顕微鏡で可視化するために水で1回リンスしました。
データと資料の可用性
すべてのデータは制限なしで完全に利用可能です。
略語
- CBA:
-
サイトメトリービーズアレイ
- DMEM:
-
ダルベッコの改良イーグル培地
- FBS:
-
ウシ胎児血清
- FCM:
-
フローサイトメトリー
- ICC:
-
免疫細胞化学
- N-PAMAM:
-
ニュートラルパマム
- PAMAM:
-
ポリアミドアミンデンドリマー
- QD:
-
量子ドット
ナノマテリアル
- ICM-20608-Gの仕様とアプリケーション
- BH1750 –仕様とアプリケーション
- ガラス繊維の布とマットの違い
- 再吸収抑制タイプII /タイプIZnSe / CdS / ZnSコア/シェル量子ドットの合成と免疫吸着アッセイへのそれらの応用
- マイクロピラーのInAs二重層量子ドットに基づく1.3μmの明るい単一光子源
- 効果的な酵素模倣物としてのピリジニックリッチN、S共ドープ炭素量子ドットの合成
- アニーリングされたGaAsBi / AlAs量子井戸のビスマス量子ドット
- 水溶性硫化アンチモン量子ドットの合成とそれらの光電特性
- グラフェン/ Ag3PO4量子ドット複合材料の簡単なワンステップソノケミカル合成と光触媒特性
- MBiおよびMSb(M:Ti、Zr、およびHf)ハニカムにおける量子異常ホール効果の予測
- 1.3〜1.55μmウィンドウでの変成InAs / InGaAs量子ドットのバンド間光伝導



