高炉の製鉄プロセスに及ぼすアルカリの影響
高炉の製鉄プロセスに対するアルカリの影響
高炉(BF)の運転中の主な目的の1つは、最小のコストで目的の化学組成の溶銑(HM)の生産を最大化することです。これには、高品質の原材料ベースと高炉の定期的でスムーズな運転が必要です。炉に入る不要な元素によって引き起こされるプロセスの問題を回避するために、装入物の品質は非常に重要です。この分野では、投入料金の不要な要素の内容にも注意を払う必要があります。これらの不要な要素は、BFで多くの技術的な問題を引き起こします。さらに、それらはHMの製造コストに大きく影響します。 BFの除去と性能に関して厄介な可能性のある電荷に存在する主な不要な元素は、金属カリウム(K)とナトリウム(Na)のアルカリ化合物です。
BFプロセスでは、アルカリの存在がプロセスに悪影響を与えることが知られています。アルカリは、コークスのより高い反応性、鉱石装入物の早期軟化、焼結物の分解、ペレットの膨潤を引き起こし、ライニングの摩耗を加速するBFの耐火性ライニング上の堆積物の形成に関与します。アルカリの悪影響は、コークスのガス化に対する触媒効果、アルカリの挿入による炭素(C)構造の破壊、足場の形成、および耐火性の攻撃によるものです。アルカリは原料とともに導入され、アルカリ循環(図1)により、BFの高温ゾーンに向かう途中でアルカリが吸収されます。
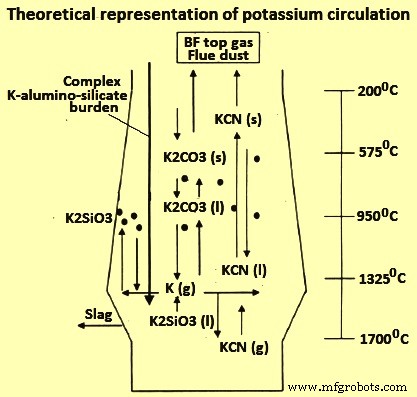
図1K循環の理論的表現
アルカリの存在は、BFでの生産量の低下とコークス消費量の増加につながり、原材料のトップチャージで添加されたkg / tHMアルカリごとにそれぞれ約4.5%と2.3%になります。アルカリは、Boudouard可逆反応のしきい値、C(s)+ CO2(g)=2CO(g)の低下、コークスガスの増加、およびコークスの強度の低下により、生産量を減少させます。コークスの劣化によりガス透過性が低下し、壁に足場ができてBFの体積が減少する可能性があります。
BFでのアルカリ反応
この記事に記載されているすべてのアルカリ反応では、KをNaに置き換えることができます。 Cによるアルカリケイ酸塩の還元は、K2SiO3(スラグ)+ C(s)=2K(g)+ SiO2(スラグ)+ CO(g)、およびK2SiO3(スラグ)+ 3C(s)の可逆反応に従って行うことができます。 =2K(g)+ Si(HM)+ 3CO(g)。発生するこれらの反応の程度は、CO(一酸化炭素)の温度と分圧に依存します。アルカリ酸化物は、可逆反応K2O + C(s)=2 K(g)+ CO(g)、およびK2O + CO(g)=2 K(g)に従って、コークス中のCまたはCOのいずれかによって還元できます。 )+ CO2(g)。
アルカリは元素として揮発するか、BFのボッシュ領域でCおよびN2(窒素)と反応して、可逆反応2K(g)+ N2(g)=2KCNに従ってシアン化カリウム(KCN)またはシアン化ナトリウム(NaCN)の蒸気を形成します。 (g)。蒸気は炉ガスと一緒に運ばれ、HMやスラグに溶解しません。 Kの融点と沸点はそれぞれ63.4℃と759℃であり、Naの対応する融点と沸点はそれぞれ97.7℃と883℃です。 KCNとNaCNの融点はそれぞれ622℃と562℃であり、沸点はそれぞれ1625℃と1530℃です。これらの化合物の状態は、温度に応じて、下部シャフトでは液体であり、レースウェイと炉床ゾーンでは気体です。ガスはBF内の高速で移動するガスによって運ばれます。
酸素(O2)電位が上昇するシャフト(約1100℃)では、KとKCNは安定しなくなり、二酸化炭素(CO2)によって酸化されてアルカリ炭酸塩(K2CO3、Na2CO3)になります。 g)+ 2CO2(g)=K2CO3 + CO(g)、および2KCN(g)+ 4CO2(g)=K2CO3(s)+ N2(g)+ 5CO(g)およびCOによるアルカリ酸化物可逆反応2KCN(g)+ CO(g)=K2O + 3C + N2(g)。生成されたアルカリ炭酸塩は白い微粉の形で残り、それは負担材の表面に分布するか、レンガの裏地に配置されます。
負荷材料とコークスに吸着されたアルカリ成分は、それらの相対的な安定性に従って新しい化合物を形成します。炭酸カリウム(K2CO3)と炭酸ナトリウム(Na2CO3)は、それぞれ891℃未満と851℃未満の温度で固体です。アルカリ含有化合物は、負荷物質とともに下降し、可逆反応K2CO3(l)+ 2C =2K(g)=3CO(g)に従って、還元されて再び気化して高温ゾーンに到達します。
アルカリの大部分はスラグとともにBFから排出されます。しかし、スラグ中のアルカリの一部が還元され、周囲のガスとともに上昇するアルカリ蒸気が発生します。アルカリ蒸気はBFの上部で凝縮し、一部は上部ガスとともに排出され、残りは内壁または供給材料で凝縮します。異なる熱ゾーンでのアルカリの揮発と凝縮のために、アルカリはBF内で循環する傾向があり、他の供給材料の蓄積と相互作用につながります。これは、アルカリが少量、一般に溶銑1トンあたり5キログラム(kg / tHM)未満で充填されている場合でも、プロセスに大きな影響を与える可能性があります。 BF内のアルカリ循環の簡略図を図2に示します。掘削されたBFの研究では、温度が1000℃を超えるとアルカリレベルが最も高くなることが示されています。これは、下部のアルカリ濃度が増加していることを意味します。 BF。
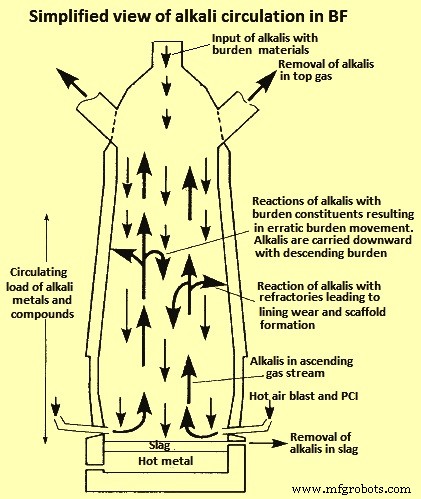
図2BF内のアルカリ循環の簡略図
BFのアルカリサイクル
アルカリは通常、鉄材料とケイ酸塩の形のコークスとともにBFに入ります。スムーズで効率的なBF運転のためには、アルカリの量を約1.5 kg/tHMから5kg/ tHMに制限することが望ましいですが、通常、さまざまなプラントで2.5 kg/tHMから7.5kg/tHMの範囲です。 2つのアルカリ物質NaとKのうち、Kは通常BFに入る主な化合物です。ほとんどのアルカリはスラグとともに出て行きますが、一部はトップガスの一部になり、炉からトップガスとともに出ます。再循環アルカリは、スラグまたはガスのいずれかによって除去できます。 Kは、スラグとともに排出されるNaに比べて揮発性が高いため、トップガスへの移行度が高くなります。
アルカリはケイ酸塩(K2SiO3)の形でBFに入ります。アルカリサイクルの研究は、ケイ酸塩が負荷とともに下降し、サイクルは、式K2SiO3 + C(s)=2K(g)+に従って、溶融ゾーンのコークスのCによってアルカリケイ酸塩が還元されることから始まることを示しています。 SiO2 + CO(g)。反応の熱力学的データによると、反応は約1550℃で起こります。 BFに入る、またはBFに形成されるアルカリ酸化物は、安定していないため、式K2O + CO(g)=2K(g)+ CO2(g)に従って、低温でBF内でさらに反応します。 K2Oは一次スラグに溶解することもあります。
さらに、BFの炉床レベルで生成されたK蒸気は、式2K(g)+ 2C(s)+ N2(g)=2KCN(g)に従って、注入された微粉炭および熱風のN2と反応します。 、l)。 KCNの沸点は1625℃であるため、シアン化カリウム(KCN)は羽口からの熱風から上昇し、温度が下がると液相に変化します。ガスの流れが多いため、羽口ゾーンでの時間は非常に短いため、シアン化アルカリは液相に変化する前にBFを上昇する時間があります。 BFのさらに上では、アルカリシアン化物がCO2(二酸化炭素)と反応して、式2KCN(l)+ 4CO2(g)=K2CO3 + N2(g)+ 5CO( g)。炭酸塩は、上部のガスをガスとして追い出すか、900℃未満で凝縮し始めると重荷に堆積します。
アルカリケイ酸塩と比較して、アルカリシアン化物は不安定であるため、BFの炉床部分に存在するSiO2は、アルカリシアン化物と反応して再びアルカリケイ酸塩を形成する可能性があります。アルカリケイ酸塩がアルカリ蒸気に還元され、BFで上昇し、トップガスとともに放出されるか、CO2と反応して炭酸塩を形成するプロセスは、アルカリサイクルとして知られています。発生する反応を正確に変えることにより、プロセスの要約がわずかに異なるいくつかの異なるビューがあります。 BFの発掘中に炭酸塩が見つからないため、BFの上部に実際に炭酸塩が形成されているかどうかは疑問です。ただし、アルカリシアン化物が形成され、アルカリがBF内を循環する主なプロセスは、すべての見解で合意されています。
図3は、BF内のアルカリの循環を示しています。帯電した物質は、アルカリケイ酸塩がアルカリ蒸気に分解するか、K2OまたはNa2Oの形で一次スラグ相に吸収される前に、高温ゾーンに降下します。このサイクルは、アルカリ蒸気がケイ酸塩と反応して再びケイ酸塩を形成する時期も示しています。 BFを通るアルカリ蒸気の分布は、ガス流路と中央ガス流の範囲に依存します。ガスの流れは、BF内の熱の分配方法に大きな影響を及ぼします。より中心的な流れは、BFの中央でより多くの融解を意味し、BFの周辺でより少ないことを意味します。
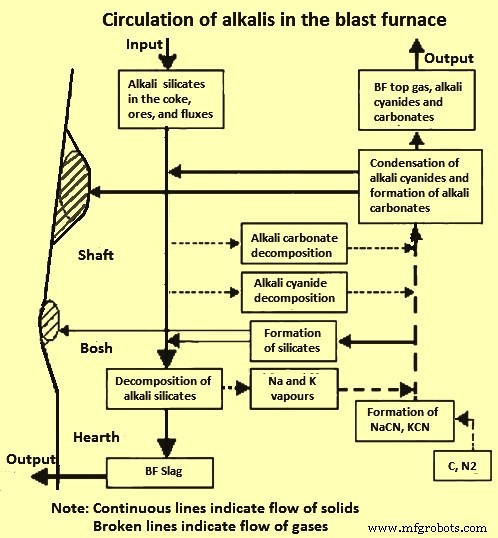
図3BF内のアルカリの循環
BFでのアンモニアとシアン化水素の生成
アンモニア(NH3)はBFで形成されると考えられています。 BFでのNH3およびシアン化水素(HCN)形成の背後にある基本的な反応は、2KCN + 3H2O =K2CO3 + 2NH3 + C、およびNH3 + CO =HCN+H2Oです。これらの反応の比率は、(i)利用可能な水分の量、(ii)上部の利用可能なKCNの量、(ii)反応中の温度などのいくつかのパラメーターに依存します。 NH3の温度しきい値は約600℃であり、NH3の形成は500℃まで指数関数的に減少し続け、その後は検出されません。さらに、形成されるNH3は、Fe2O3またはCO2のいずれかによって酸化され、形成されるNH3の量が減少します。 Fe2O3またはMnO2によるNH3の酸化は、温度に依存します。低温ではMnO2がより強力な酸化剤であり、高温ではFe2O3がより強力な酸化剤です。
HCNとNH3はトップガスに含まれているため、NH3の酸化速度は、完全に除去するのに十分な速さではありません。トップガスに含まれる水分が多いということは、上記の反応に従って発生する可能性のあるNH3の生成が多いことを意味します。 BFでのNH3の形成は、以下に示すいくつかのパラメーターがその形成に影響を与えるため、複雑です。
最高ガス温度 –最高ガス温度は、BFの吸熱/発熱反応の比率によって異なります。温度は水分含有量に影響します。温度が低いと、NH3の水への溶解度が高くなり、HCNは水と混和するため、水の存在によってトップガス中の存在が減少する可能性があります。
火炎温度 –火炎温度は、生成されるアルカリ蒸気の量と総アルカリ負荷にわずかな影響を及ぼします。アルカリケイ酸塩をアルカリガスに還元してアルカリ循環を開始するには、高温が必要です。したがって、火炎温度を下げると、スラグからBFを離れるアルカリが増えます。
基本性 –塩基度が低いと、スラグへのアルカリの取り込みが多くなるため、BFでの循環アルカリが少なくなり、生成されるNH3が少なくなります。
水分含有量 – BFにチャージまたは他の方法で導入される水分が少ないと、NH3形成反応が発生する水が少なくなります。
アルカリと除去の効果
近年、高品質の原料炭の入手可能性が低下しているため、原料中のアルカリ濃度が上昇しています。アルカリは、溶液損失反応(ブドゥアール反応)への触媒効果によりコークスの反応性を高めるため、BF操作に悪影響を及ぼします。
アルカリの主な悪影響の1つは、Boudouardの可逆反応を触媒し、反応の温度を900℃から950℃から約750℃から850℃に下げ、それに応じてコークスの反応性を高めることです。コークスの品質。また、コークス構造にも悪影響を及ぼします。 Boudouard反応のしきい値が低いということは、強い吸熱反応でBFでより多くのCが消費されていることを意味します。したがって、使用する供給源に応じて、アルカリ1kgあたり2kgから10kgのコークス、または6kgから11kgのコークスで安定した運転を維持するには、BFへのコークスの添加量を増やす必要があります。
コークス構造に入ったアルカリは、コークスの反応性が高くなり、劣化が大きくなるため、BF下部のコークス強度が低下します。羽口レベルでのコークスの見かけの反応速度は、供給コークス反応速度の10倍であることが示されています。これは、Kの総存在量に関連しています。Kは、コークスとCO2の反応性を高めることが知られており、 Kの挿入によるコークス粒子の膨潤によるコークス破壊において。反応性の増加は、BF運転温度、保温ゾーンの温度を低下させ、したがって酸化鉄の還元のための温度を低下させるので有利である可能性がある。ただし、コークスの目的は炉内の負荷サポートとしても機能することであるため、コークスの破壊を最小限に抑える必要があります。
コークスへのK蒸気の浸透に関する研究により、アルカリ化鉱物、特にカルシライトの体積膨張により、コークス鉱物の構造が破壊される可能性があることが確認されています。コークス中の鉱物が破損するため、鉱物とCマトリックスの間の表面積が増加します。これにより、鉱物とCおよびBFガスとの相互作用が促進され、コークスのガス化が促進されます。コークスの膨張は、アルカリ蒸気がコークスの結晶層に浸透して層間化合物を形成するときにも発生する可能性があります。 BF運転中のコークス強度と負担のサポートは、負担の崩壊がガスと液体の透過性を低下させ、HM生産とCO2排出量の増加の両方に関する効率を低下させるため重要です。
異なるサイズの小さなコークス粒子は、ウェットゾーンのコークス床のボイドを減少させ、コークスの表面積が増加します。コークスの破損はまた、洪水、炉床の窒息、および羽口とスラグノッチの燃焼の増加を促進し、これらはすべて炉の出力を制限します。透過性が低くなると、上昇するガスが壁の近くに輸送される傾向が高まり、ガスの利用率が低下し、コークス率が上昇します。
アルカリのもう1つの効果は、アルカリがライニングに凝縮し、微細な材料をそれに結合できるため、シャフトに足場が形成される可能性が高くなることです。足場は、炉壁に固体材料が蓄積し、炉の中心に向かって突き出ています。足場は、シャフトの中央から上部までの任意の場所で発生する可能性があります。足場形成の効果は、負担の下降が遅くなるか中断されることであり、極端な場合には、ぶら下がったり、滑ったり、制御されていない充電につながる。足場はまたBFの作業量を減らします。シャフト内の影響を受けていない部分でガス速度が増加し、その結果、上部ガス温度が上昇し、COの利用率が低下します。足場が炉壁から離れると、炉床が冷えることがよくあります。足場は、炉の温度を一時的に上げることによって削除するか、高温のガス流がその領域に到達したときに削除することができます。
装入物は、凝縮した液体シアン化物と炭酸塩によって接着することもでき、床の浸透性を低下させます。さらに、アルカリは耐火物、特に炉の下部で通常使用されるCベースの耐火物を攻撃する可能性があります。アルカリ化合物は、アルカリ蒸気を形成するために消費されるCブロックに浸透します。これにより、耐火物のライニングの寿命が短くなり、より頻繁にリライニングする必要があります。
アルカリの除去は主にスラグを使用して行われ、より低い塩基度値で実行するのが最適です。除去されたアルカリの90%以上がスラグから除去されます。ここでは、塩基性はCaO/SiO2と見なされます。いくつかの研究の結果は、スラグの塩基度が低いとスラグ中のアルカリの量が増えることを示しています。ただし、塩基度が低すぎる場合の問題は、BFスラグに存在するCaOによってSが打ち消される可能性があり、塩基度が低いとCaOが低くなるため、HMに高レベルの硫黄(S)が残ることです。 HMの品質を管理するための塩基度の下限は、プラントごとに異なります。制限は、BFパラメータと使用する原材料の品質によって異なります。アルカリを除去し、HM品質を維持する場合は、1のすぐ上または約1の塩基度値を限界と見なすことができます。
アルカリケイ酸塩のガス化を防ぐために、COの分圧を高く保つ必要があります。 1550℃での反応の高温は、より低い火炎温度も還元とガス化を遅くし、したがってアルカリ循環を低下させるために使用できることを意味します。アルカリを除去すると、アルカリがBFに再導入されるため、アルカリ含有材料のBFへの再循環を減らす必要があります。
コークスのガス化に対するアルカリの触媒効果の低下は、既存のアルカリをより安定した形で結合できるコークス灰の添加によって行うことができます。それは以前に特定のミネラル添加で試されました。アルカリがコークスを通って拡散するので、ミネラル添加のコーティングはコークスの表面でアルカリを安定させ、コークスの内部を劣化させるのを防ぎます。
アルカリ負荷の制御
BFのアルカリ負荷を制御するために、アルカリ入力を可能な限り低く保つ必要があります。流入する材料に変動がある場合は、BFの高アルカリセクションのリスクを最小限に抑えるために、鉱石混合物を十分にブレンドする必要があります。もう1つの予防策は、高レベルのアルカリによる煙道ダストの再循環を回避することです。足場形成のリスクを最小限に抑える方法は、鉄の負担とコークスの強度を高めて、微粉の形成を回避することです。
BFは中央ガス流で操作できます。そのため、中央のトップガス温度は、アルカリの一部がトップガスとともに蒸気として炉を出るレベルまで上昇します。ただし、上部ガス温度が高くなると、熱損失が増加します。
再循環アルカリを減らすことができ、代わりに酸スラグでBFを操作することにより、スラグを介してBFを離れることができます。スラグの塩基度が低いほど、石灰(CaO)とマグネシア(MgO)がアルカリ酸化物と同じシリカネットワークのサイトを占めるため、塩基性のKとNaがスラグに吸収されやすくなります。鉄分負荷とフラックス添加の塩基度を下げることにより、塩基度を下げることができます。ただし、塩基度が低いと、SがスラグのCaに結合するため、HMのS(硫黄)含有量も増加します。
アルカリ負荷を減らす別の可能性は、スラグの量を増やすことです。これにより、スラグ内のアルカリ酸化物の活性が低下し、アルカリの吸収とスラグからの排出量が増加しますが、スラグの量を増やすとコークス率も増加します。
BFの温度が低いと、アルカリの還元と気化が減少します。より低い火炎温度でBFを操作すると、アルカリ負荷が減少しますが、生産性が低下し、コークス率が高くなります。アルカリガス化反応に対抗するため、CO分圧の高いBFで運転することにより、アルカリ負荷を低減することもできます。これは、爆風のO2濃縮または高いトップ圧力によって達成できます。
製造プロセス



